理化学研究所(理研)環境資源科学研究センター細胞機能研究チームのデービッド・ファベロ訪問研究員、杉本慶子チームリーダーらの国際共同研究グループは、葉の葉柄[1]の伸長成長は、転写因子ファミリー[2]AHL[3]が別の転写因子ファミリーPIF[4]と拮抗して作用することで制御されていることを明らかにしました。
今後、有用植物の転写因子PIFやAHLの活性を人為的に制御することで、バイオマスの増大や環境に対する頑健性の向上といった農業や環境保全の発展につながると期待できます。
これまで、PIFが葉柄の伸長に関わる遺伝子群を活性化することで、成長を促進することが知られていましたが、成長を抑制するメカニズムはよく分かっていませんでした。
今回、国際共同研究グループは、胚軸[5]の成長を抑制する働きをするAHLの機能に着目しました。モデル植物であるシロイヌナズナ[6]を用いて、AHLがPIFと拮抗的に作用し、PIFの標的遺伝子(ATHB2遺伝子[7]など)への結合を妨げることにより、葉柄の成長を抑制することを明らかにしました。これは、AHLがPIFを介した遺伝子発現を制御することで、葉柄の伸長成長を厳密に調節していることを示しています。
本研究は、科学雑誌『Current Biology』の掲載に先立ち、オンライン版(3月19日付:日本時間3月20日)に掲載されます。
背景
植物の成長過程はあらかじめ決まっているわけではなく、周りの環境に適合するよう柔軟に制御されていて、その背景にはさまざまな転写因子による厳密な機構が存在しています。
植物は暗所や日陰で胚軸や葉柄などを伸長させますが、転写因子PIFには伸長成長を促す働きがあります。もともとPIFは、光受容体[8]の一つであるフィトクロムと相互作用するタンパク質として発見され、光シグナルを伝達する因子として研究が進められてきました。現在では、光シグナルだけでなく、さまざまな環境シグナルに応答する反応を統合する「ハブ」として機能することが明らかになってきています。
一方、転写因子AHLファミリーの一つであるSOB3[9]は、胚軸の伸長を抑制する因子として発見されました。2016年にデービッド・ファベロ訪問研究員(当時ワシントン州立大学院生)らは、SOB3がオーキシン[10]シグナルに関連した遺伝子の発現を抑制することで、胚軸の伸長が阻害されることを明らかにしました注1)。今回、国際共同研究グループはこれまでに得た知見から、葉柄の伸長成長において、SOB3を含むAHLがPIFと関連して機能するのではないかと考え、研究を進めました。
- 注1)Favero et al., SUPPRESSOR OF PHYTOCHROME B4-#3 Represses Genes Associated with Auxin Signaling to Modulate Hypocotyl Growth Plant Phys 2016 DOI: https://doi.org/10.1104/pp.16.00405
研究手法と成果
まず、国際共同研究グループは、AHLとPIFがどのように葉柄の伸長に作用するかを遺伝学的な手法で調べました。その結果、PIF4遺伝子の機能欠損株であるpif4-101変異株では葉柄が野生型よりも短くなったのに対し、SOB3遺伝子の機能欠損株であるsob3-6変異株では、逆に長くなりました。また、pif4-101 sob3-6二重変異株では、pif4-101変異株と同様に葉柄が短くなりました(図1)。これらの結果は、sob3-6変異株の葉柄が長くなるのは、PIF4遺伝子を介して引き起こされること、つまりSOB3の機能がPIF4依存的であることを示しています。

図1 pif4変異株とsob3変異株の葉柄における表現型
野生株(WT)と比較して、sob3機能欠損株(sob3-6)では葉柄が長く、pif4機能欠損株(pif4-101)では葉柄が短い。一方、sob3 pif4二重変異株(sob3-6 pif4-101)ではpif4変異株と同様の表現型を示し、SOB3の機能がPIF4依存的であることが分かった。
次に、PIFの標的遺伝子の発現をAHLが抑制することで、AHLが葉柄の伸長を抑えているという仮説を立てました。その仮説を検証するために、pif4変異株とahl変異株を用いたRNA次世代シーケンス解析(RNA-Seq)[11]を行い、それぞれの転写因子に制御されている遺伝子を調べました。その結果、PIFに制御される遺伝子を415個、AHLに制御される遺伝子を3,851個同定しました。さらに、PIFによって制御される遺伝子のうち、約40%はAHLによっても制御され、しかもPIFが発現を活性化する遺伝子に対してAHLは発現を抑制するというように、PIFとAHLは共通する標的遺伝子に対して逆方向の制御をすることが明らかになりました。
さらに、PIFとAHLが標的遺伝子に対して直接作用するかどうかを検証するために、クロマチン免疫沈降シーケンス法(ChIP-Seq)[12]を行いました。PIFとAHLのChIP-Seqデータを先述のRNA-Seqデータと合わせて解析した結果、PIFによって直接的に発現誘導され、かつAHLによって直接的に発現抑制される遺伝子を34個同定しました。この34の遺伝子の中には、葉柄の伸長成長に必要なことが知られている転写因子ATHB2の遺伝子が含まれており、pif変異株で葉柄が長く、sob3変異株で葉柄が短くなるという表現型とよく合致します。そして、ChIP-seqデータからは、SOB3とPIFがよく似たDNA領域に結合することが示されました(図2)。
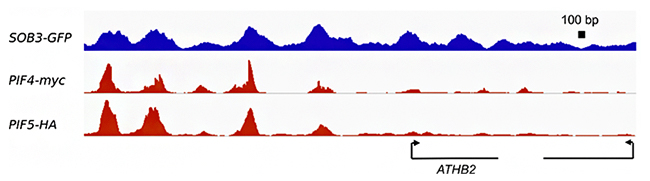
図2 転写因子SOB3、PIF4、PIF5のDNA結合領域
ChIP-seqデータから、SOB3-GFP、PIF4-myc、PIF5-HAで検出されるピークがよく似ていることが明らかになった。この結果は、SOB3とPIF4、PIF5が、よく似たDNA領域に結合することを示す。
さらに、SOB3遺伝子の発現量を改変した植物体を作出し、その組み換え植物を用いてPIF4のATHB2遺伝子に対する結合を調べたところ、SOB3遺伝子の過剰発現体では、PIF4のATHB2遺伝子プロモーター領域[13]への結合がおよそ60%程度低下するという結果が得られました。これらの結果は、AHLがPIFと拮抗的に作用し、AHLがPIFの標的遺伝子への結合を妨げることで、葉柄の成長を抑制することを示しています(図3)。つまり、AHLがPIFを介した遺伝子発現を制御することで、葉柄の伸長成長を厳密に調節していることが明らかになりました。
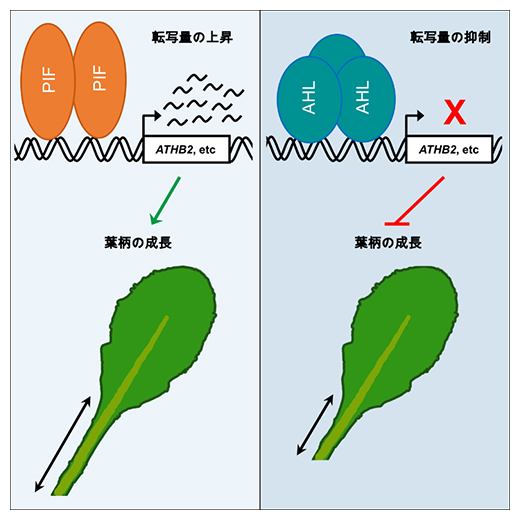
図3 AHLによる葉柄の成長制御モデル
転写因子PIFは成長に必要なATHB2遺伝子などのプロモーター領域に結合し、標的遺伝子の転写を活性化することで葉柄の伸長を促進する。一方、転写因子AHLは同じ標的遺伝子のプロモーター領域に結合することで、PIFがプロモーター領域へ結合することを阻害する。したがって、葉柄の成長に必要な遺伝子の転写レベルが下がり、葉柄の伸長が抑制される。
今後の期待
本研究では、環境に応じた葉柄の成長制御には、PIFとAHLという二つの転写因子が重要な役割を担っていることを明らかにしました。PIFとAHLは植物界に広く保存されていることから、今後は有用植物のPIFやAHLの活性を人為的に制御することで、バイオマスの増大や環境に対する頑健性の向上といった農業や環境保全への発展が期待されます。
また、本研究成果は、国際連合が2016年に定めた17項目の「持続可能な開発目標(SDGs)」のうち「2.飢餓をゼロに」と「15.陸の豊かさも守ろう」に大きく貢献するものです。
補足説明
- 1.葉柄
葉の幹のような部分。多くの植物の場合、この葉柄の成長は環境シグナルによって影響を受ける。例えばシロイヌナズナの場合、日陰条件や高温条件で葉柄の長さが長くなる。 - 2.転写因子ファミリー
特定のDNA配列に結合し、遺伝子発現を制御するタンパク質の一群。 - 3.AHL
植物にのみ存在する転写因子ファミリー。発芽時の成長や花成のタイミング、花器官の発達、老化、免疫、乾燥応答などさまざまな現象に関わる。AHLはAT-HOOK MOTIF NUCLEAR LOCALIZEDの省略形。 - 4.PIF
植物の成長制御に重要な転写因子として知られている。PIF4とPIF5には、胚軸や葉柄の伸長を促進する機能がある。胚軸や葉柄の成長は光や温度の影響を強く受けるが、PIFの活性も光や温度の影響を強く受ける。PIFは、PHYTOCHROME INTERACTING FACTORの省略形。 - 5.胚軸
幼植物の幹のような部分。葉柄同様に、胚軸の成長は外部環境の影響を強く受ける。特に、日陰条件や高温条件は胚軸の伸長成長を強く促進する。 - 6.シロイヌナズナ
アブラナ科の植物の一つで、「ぺんぺん草」で知られるナズナの近縁種である。持っている遺伝子の総量が比較的少なく、発芽から開花し種子が採れるまでの時間が比較的短いことから、被子植物の代表として世界中で研究対象になっている。2000年に植物としては初めて全遺伝子の解読が終了したことから、特に分子生物学分野で多用されている。普遍的な生命現象の解明に用いられる代表的な生物をモデル生物と呼ぶが、これらの理由によりシロイヌナズナはモデル植物となっている。 - 7.ATHB2遺伝子
胚軸や葉柄の伸長を促進する機能が知られている転写因子ATHB2をコードする遺伝子。PIFによる成長の促進作用の一部はATHB2遺伝子の転写制御を介して行われる。ATHB2は、ARABIDOPSIS THALIANA HOMEOBOX PROTEIN 2の省略形。 - 8.光受容体
光刺激によって活性化するタンパク質。植物では赤色、青色、紫外線をそれぞれ受容するための光受容体がある。光によって活性化された光受容体は、PIFをはじめとする転写因子の活性に影響を与える。 - 9.SOB3
AHLファミリーの一つであり、AHL29とも呼ばれる。これまで、SOB3は他のAHLと同じく、オーキシンシグナル伝達を阻害することで胚軸の伸長を抑制することが知られていた。SOB3は、SUPPRESSOR OF PHYTOCHROME B4-#3の省略形。 - 10.オーキシン
植物の成長を制御する植物ホルモンの一つ。一般的にオーキシンは、胚軸や葉柄の成長を促進する作用がある。PIFは、オーキシンの生合成とシグナル伝達を活性化することでも胚軸や葉柄の伸長を促進する。 - 11.RNA次世代シーケンス解析(RNA-seq)
次世代シーケンサーを用いて、ある細胞、組織で発現する遺伝子の種類と発現量を網羅的に捉える方法。RNAを抽出した後、相補的なDNAに変換したものの配列を読むことで、ゲノムのどこの配列がどれくらい転写されていたかを見積もる。 - 12.クロマチン免疫沈降シーケンス法(ChIP-seq)
クロマチン免疫沈降法は、生体内におけるタンパク質とゲノムDNAの結合部位を検出するための実験手法である。ホルムアルデヒドによってDNAとDNAに結合しているタンパク質を架橋した後に、DNAの断片化を行い、タンパク質の抗体を用いてタンパク質-DNA複合体を回収する。さらに、DNAとタンパク質の架橋を解いてDNAのみを回収し、その配列を調べることでタンパク質がどのようなDNA配列に結合していたかが分かる。次世代シーケンスと組み合わせることで、ゲノム上のどこに、どれくらいの強さで結合していたかが分かる。ChIPは、Chromatin Immunoprecipitationの略。 - 13.プロモーター領域
DNAがコードする情報(遺伝子)をmRNAに転写するには、読み取るDNAの読み始めを規定する必要がある。この転写の開始に関与する遺伝子の上流領域をプロモーター領域という。RNAポリメラーゼや転写因子などのタンパク質が結合することで、転写が調節される。
国際共同研究グループ
理化学研究所 環境資源科学研究センター 細胞機能研究チーム
チームリーダー 杉本 慶子(すぎもと けいこ)
訪問研究員 デービッド・ファベロ(David S.Favero)
(日本学術振興会特別研究員)
テクニカルスタッフⅡ 河村 彩子(かわむら あやこ)
テクニカルスタッフⅡ 竹林 有理佳(たけばやし ありか)
研究員 柴田 美智太郎(しばた みちたろう)
研究員 岩瀨 哲(いわせ あきら)
研究員(研究当時) 石田 喬志(いしだ たかし)
(現熊本大学助教)
中部大学 応用生物学部
准教授 鈴木 孝征(すずき たかまさ)
ケンブリッジ大学 センズベリー研究所
グループリーダー フィリップ・ウィッグ(Philip A Wigge)
研究員 ジェイフン ジューン(Jae-Hoon Jung)
研究員 カティア・イェーガー(Katja E Jaeger)
ワシントン州立大学 作物土壌学科
教授 マイケル・ネフ(Michael M Neff)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費補助金特別研究員奨励費「AHL転写因子を介した植物の器官成長を司る転写制御ネットワークの解明(受入研究者:杉本慶子)」、同基盤研究(B)「植物の器官再生を制御する分子機構(研究代表者:杉本慶子)」、同新学術領域研究(研究領域提案型)「植物の成長可塑性を支える環境認識と記憶の自立分散型統御システム(領域代表者:木下俊則)」による支援を受けて行われました。
原論文情報
- David S Favero, Ayako Kawamura, Michitaro Shibata, Arika Takebayashi, Jae-Hoon Jung, Takamasa Suzuki, Katja E Jaeger, Takashi Ishida, Akira Iwase, Philip A Wigge, Michael M Neff, Keiko Sugimoto, "AT-hook transcription factors restrict petiole growth by antagonizing PIFs", Current Biology, 10.1016/j.cub.2020.02.017
発表者
理化学研究所
環境資源科学研究センター 細胞機能研究チーム
訪問研究員 デービッド・ファベロ(David S.Favero)
チームリーダー 杉本 慶子(すぎもと けいこ)
報道担当
理化学研究所 広報室 報道担当
お問い合わせフォーム
