理化学研究所(理研)生命機能科学研究センター計算分子設計研究チームの小松輝久研究員、小山洋平研究員、沖本憲明上級研究員、森本元太郎技師、大野洋介上級技師、泰地真弘人チームリーダーの研究チームは、新型コロナウイルス感染症(COVID-19)の原因ウイルスである「SARS-CoV-2」のメインプロテアーゼ[1]の10マイクロ秒間(1マイクロ秒は100万分の1秒)にわたる構造動態を、分子動力学(MD)[2]シミュレーション専用計算機「MDGRAPE-4A[3]」を用いてシミュレートしました。そして、その生データ[3]を世界の創薬研究者に自由に利用してもらうため、リポジトリ[4] Mendeley Dataにて3月17日に公開しました。
本データは、ウイルス増殖に必須であるプロテアーゼ活性を効率よく阻害する阻害薬の開発、候補分子のスクリーニングなどに役立つと期待できます。
コロナウイルスは一本鎖RNAをゲノムとして持ち、宿主細胞に感染するとRNAゲノムから長いタンパク質(ポリタンパク質[5])が翻訳されます。このポリタンパク質が切断されることで、それぞれの断片がウイルスの増殖に必要な構造タンパク質や酵素として働きます。この酵素のうち、ポリタンパク質の切断を主に触媒するのがメインプロテアーゼです。メインプロテアーゼの切断活性を阻害する抗ウイルス薬の開発が進められており、既に、ヒト免疫不全ウィルス(HIV)など既存ウイルスのプロテアーゼ阻害薬とSARS-CoV-2メインプロテアーゼの複合体の立体構造(X線結晶解析[6]データ)が複数の研究機関から報告されています。MDシミュレーションは、細胞内に近い状況での分子間相互作用を解析する手法であり、水溶液中での分子の動きや溶媒効果[7]を考慮した創薬スクリーニングを高精度に進めるための情報を得ることができます。
今回、研究チームは、最近報告されたSARS-CoV-2メインプロテアーゼのX線結晶解析データをもとに、水溶液中でのプロテアーゼ2量体の構造動態をMDGRAPE-4Aでシミュレートしました。
背景
新型コロナウイルス感染症(COVID-19)は、2019年に中国・武漢で初めて報告されてから現在に至るまで全世界に広がり、世界保健機関(WHO)はパンデミック(世界的大流行)を表明しました。この新型ウイルスによる社会的影響は世界規模に達しており、COVID-19への有効な薬の開発は極めて緊急性の高い、国際的事象となっています。
コロナウイルスは一本鎖RNAをゲノムとして持ち、宿主細胞に感染するとRNAゲノムから長いタンパク質(ポリタンパク質)が翻訳されます。このポリタンパク質が切断されることで、それぞれの断片がウイルスの増殖に必要な構造タンパク質や酵素として働きます。COVID-19の原因ウイルス「SARS-CoV-2」が同定されると、複数の機関がウイルスタンパク質の立体構造解析に取り組み、その成果が公的データベースに次々と登録されています注1)。
構造解析に基づく抗ウイルス薬の開発に際して、標的となるタンパク質の一つが、ポリタンパク質の切断を主に触媒するメインプロテアーゼです。メインプロテアーゼの切断活性を阻害すれば、細胞に感染したウイルスの増殖を抑制できると考えられ、メインプロテアーゼに結合する阻害分子の探索が進められています。実際に、ヒト免疫不全ウィルス(HIV)においてはメインプロテアーゼを標的とした薬剤が複数開発され、有効性が示されています。
近年の医薬品開発においては、標的タンパク質に対する薬剤候補分子の探索・評価にスーパーコンピュータ(スパコン)を活用するインシリコ創薬[8]が注目されています。分子動力学(MD)シミュレーションは、細胞内に近い状況での分子間相互作用を解析する手法であり、水溶液中での分子の動きや溶媒効果を考慮した創薬スクリーニングを高精度に進めるための情報を得ることができます。
研究チームは、創薬専用スパコン「MDGRAPE-4A」を開発し、2019年11月より実験運用を開始しました注2)。MDGRAPE-4A は、通常の計算機よりも短時間でタンパク質の構造変化をシミュレートすることを得意とするため、標的タンパク質、薬剤候補分子、水分子の動的構造をサンプリング後、その構造データを使用して高精度な結合親和性予測を行い、現実的な計算時間で高精度なインシリコスクリーニングを実現すると期待されています。
- 注1)最新情報は、大阪大学蛋白質研究所の日本蛋白質構造データバンク(Protein Data BankJapan: PDBj)[COVID-19特集ページ]を参照。
- 注2)2019年11月18日プレスリリース「創薬専用スパコンの開発」
研究手法と成果
研究チームは、この度の新型コロナウイルス感染症の世界的危機に対し、MDGRAPE-4Aの性能を生かした速やかな貢献として、SARS-CoV-2メインプロテアーゼのMDシミュレーションデータを自由に利用できる形で公開しました。シミュレーションに用いたSARS-CoV-2メインプロテアーゼの立体構造はLiuらの報告注3)をもとにし、溶媒としての水分子数は3万弱、系の総原子数は10万弱としました。MDGRAPE-4Aで約10日間かけて計算を行い、10マイクロ秒(1マイクロ秒は100万分の1秒)にわたる構造動態をシミュレートしました(図1)。一般的には、水溶液中でのタンパク質と薬剤の分子間相互作用は、サブミリ秒(~100マイクロ秒)のタイムスケールで起きると考えられており、今回のデータは薬剤分子が結合する直前のメインプロテアーゼの構造動態を推定する基礎データになると考えられます。
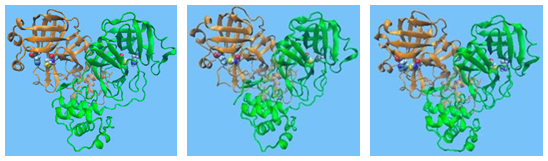
図1 MDGRAPE-4AでシミュレーションしたSARS-CoV-2のメインプロテアーゼの構造動態
2量体を構成する二つのサブユニットを色分けし、プロテアーゼ活性の中心に位置するアミノ酸部位をボールモデルで表した。この部分をはじめとしたいくつかの構造が、時間とともに揺らいでいることが分かる。
- 注3)Title: The crystal structure of COVID-19 main protease in complex with an inhibitor N3, Entry authors: Liu, X., Zhang, B., Jin, Z., Yang, H., Rao, Z., Initial deposition on: 26 January 2020
今後の期待
現在、SARS-CoV-2メインプロテアーゼに結合する分子のいくつかが抗ウイルス薬の候補として挙げられており、その複合体のX線結晶解析も行われています。実際に創薬が実現するまでには、まだ距離があり、多くの研究プロセスが必要ですが、今回公開したMDシミュレーションデータを用いて候補分子とメインプロテアーゼとの結合の強さを予測するなど、国内外の創薬研究の速やかな進展に寄与すると期待できます。
今後、研究チームは、SARS-CoV-2 メインプロテアーゼのシミュレーションを続け、薬候補分子結合状態でのシミュレーションや、類似プロテアーゼ、SARS-CoV-2中にコードされる他の潜在的創薬ターゲットタンパクのシミュレーションなどを幅広く検討していく予定です。
補足説明
- 1.メインプロテアーゼ
プロテアーゼは、タンパク質を分解する酵素の総称。コロナウイルスは二つのプロテアーゼを持ち、ポリタンパク質の切断のほとんどを担うものをメインプロテアーゼと呼ぶ。メインプロテアーゼは、二つの同じサブユニットで構成される2量体である。 - 2.分子動力学(MD)
原子間に働く力を計算し、運動方程式を繰り返し解くことで、分子の動きを追跡する方法。分子動力学法の基礎の開発について、2013年のノーベル化学賞が授与されている。MDはMolecular Dynamicsの略。 - 3.MDGRAPE-4A、生データ
1990年より開発が進められている天文学分野での重力(GRAvity)多体問題の計算に特化した専用計算機GRAPE(GRAvity PipE、重力パイプライン)の、分子動力学(Molecular Dynamics: MD)バージョン。MDGRAPE-4Aはその5作目に当たる。今回公開した生データは、溶液中の溶質(メインプロテアーゼ)と溶媒(水分子)を構成する原子1個1個の座標を2.5フェムト秒(2.5×10-15秒)ごとに計算し、10マイクロ秒間(1×10-5秒)にわたる構造動態データである。 - 4.リポジトリ
論文を共有するために整備されたサーバーを指し、大学などの研究機関が設置したものは、機関リポジトリと呼ばれる。多くのリポジトリでは、インターネットを通じて掲載論文を自由に閲覧できるようになっている。近年は、査読前の論文をリポジトリに投稿してオープンな議論を進める場合も多く、この目的のサーバーはプレプリントサーバーと呼ばれる。今回利用したMendeley Dataは、学術出版社エルゼビアが運営する研究データリポジトリである。 - 5.ポリタンパク質
コロナウイルスのRNAゲノムから翻訳される巨大なタンパク質をポリタンパク質と呼ぶ。ポリタンパク質は自らのプロテアーゼ活性により切断され、複数の断片が機能を持つタンパク質となる。 - 6.X線結晶解析
構造生物学の手法の一つ。タンパク質の結晶を作製し、その結晶にX線を照射して得られる回折データを解析することにより、タンパク質の内部の原子の立体的な配置を調べる方法。この方法によって、タンパク質の形(立体構造)や内部構造を知ることができる。 - 7.溶媒効果
生体内のタンパク質の多くは、溶媒(水)に溶けた状態で機能する。すなわち、タンパク質の周りには大多数の水分子が存在し、タンパク質の立体構造や基質との結合に影響を与えると考えられ、この効果を溶媒効果と呼ぶ。一般的なMDシミュレーションでは、水溶液中のタンパク質を、タンパク質を構成する数千個の原子と、周囲の数万個の水分子からなる10万原子系と見なす。 - 8.インシリコ創薬
細胞生物学的、生化学的な手法を主とする創薬候補物質の探索に対して、コンピュータ(シリコンチップ)の中で行う創薬をインシリコ(in silico)創薬と呼ぶ。
原論文情報
- KOMATSU, Teruhisa S.; KOYAMA, Yohei M.; OKIMOTO, Noriaki; MORIMOTO, Gentaro; OHNO, Yousuke; TAIJI, Makoto, "COVID-19 related trajectory data of 10 microseconds all atom molecular dynamics simulation of SARS-CoV-2 dimeric main protease", Mendeley Data, 10.17632/vpps4vhryg.1
発表者
理化学研究所
生命機能科学研究センター 計算分子設計研究チーム
研究員小松 輝久(こまつ てるひさ)
研究員小山 洋平(こやま ようへい)
上級研究員沖本 憲明(おきもと のりあき)
技師森本 元太郎(もりもと げんたろう)
上級技師大野 洋介(おおの ようすけ)
チームリーダー泰地 真弘人(たいじ まこと)
お問い合わせ先
理化学研究所 生命機能科学研究センター センター長室 報道担当
山岸 敦(やまぎし あつし)
Tel: 078-306-3095 / Fax: 078-306-3090
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
お問い合わせフォーム
