理化学研究所(理研)脳神経科学研究センター分子精神遺伝研究チームの江崎加代子研究員、吉川武男チームリーダーらの国際共同研究グループは、統合失調症[1]の脳内白質[2]において、スフィンゴ脂質[3]の一種でシグナル分子としても重要な「スフィンゴシン-1-リン酸(S1P)[4]」の含量が低下していることを発見しました。
本研究成果は、S1Pの代謝あるいはS1P受容体[5]を標的とした、統合失調症に対する新たな創薬の切り口になると期待できます。
今回、国際共同研究グループは、統合失調症患者の死後脳の前頭葉[6](主に灰白質[7]からなる)と脳梁[8](代表的な白質)を用いて、質量分析装置[9]によりスフィンゴ脂質の含量を網羅的に解析しました。その結果、S1Pの含量が統合失調症の脳梁で対照群と比較して有意に低下していることを見いだしました。うつ病[10]と双極性障害[11]の死後脳の前頭葉と脳梁のS1P含量には変化が見られなかったため、S1P含量の低下は統合失調症の脳内白質で生じている脂質代謝の変化であることが示されました。さらに、S1Pの合成・分解に関わる酵素をコードしている遺伝子群の発現を調べたところ、分解に関わる酵素遺伝子の発現が上昇していたことから、S1P含量の低下は分解の亢進による可能性が示されました。また、S1Pは受容体を介して生理活性を示しますが、統合失調症の脳梁ではS1P受容体の遺伝子発現が上昇していることも明らかになりました。S1P受容体の上昇は、S1P含量の低下に対する代償的反応である可能性があります。
本研究は、科学雑誌『Schizophrenia Bulletin』(4月29日付:日本時間4月29日)に掲載されます。
統合失調症脳梁でのスフィンゴシン-1-リン酸(S1P)含量の低下
背景
統合失調症は、一般人口の約100人に1人の割合で発症する比較的頻度の高い精神疾患です。思春期に好発し、適切な治療や医療を受けないと、生涯にわたって生活の質(QOL)が損なわれる可能性が高いという問題があります。
現在利用できる治療薬のほとんどは、神経伝達物質[12]の受容体をブロックするものですが、副作用に悩まされる患者も多く存在します。さらに、薬が効かない、いわゆる「治療抵抗性」の患者は3割に上るという報告もあります注1)。このような状況にもかかわらず、新たな統合失調症治療薬の開発は充分に進んでいないのが現状です。大きな理由の一つに、統合失調症の脳内でどのような分子レベルの変化が生じているのかが分かっていないことがあります。この状況を突破するためには、最新の分析装置を使い、死後脳を用いて分子を網羅的に解析することが必要です。脳組織は、神経細胞が豊富な灰白質と神経線維の束からなる白質に分けられます。統合失調症では、核磁気共鳴画像(MRI)[13]などの画像研究で、白質容積の減少や白質走行の異常、およびミエリン[14]の形成障害など、白質の異常が繰り返し報告されてきました。また、白質は脂質を豊富に含む組織ですが、統合失調症における脂質代謝異常も以前から注目されていました。ただ、具体的にどのような脂質成分が統合失調症の白質で変化しているのかは、精密に測定されたことはありませんでした。特に脳梁は、白質の中でも、左右の大脳半球をつなぐ大きな構造をしています。今回、国際共同研究グループは、質量分析装置を用いて、統合失調症における脳梁の脂質分子を網羅的に調べることで、疾患発症のメカニズム解明や治療のための新しい手掛かりが得られると考えました。
- 注1)John M. Kane et.al. Clinical Guidance on the Identification and Management of Treatment-Resistant Schizophrenia. J Clin Psychiatry 80(2):18com12123, 2019
研究手法と成果
脂質の中でもスフィンゴ脂質は、脳の発達や神経機能に特に重要な役割を果たしています。主要なスフィンゴ脂質の生合成は、セリンパルミトイルトランスフェラーゼ(SPT)によるパルミトイルCoAとアミノ酸のL‐セリンの縮合で始まり、セラミド[15]やスフィンゴシン-1-リン酸(S1P)が合成されます(図1A)。
統合失調症では、アミノ酸のセリンの含量変化も報告されているため、セリンが合成に関わるスフィンゴ脂質は脂質の中でも特に興味が持たれます。先行研究で、セラミドの含量が統合失調症患者の皮膚で低下していることが報告されていましたが、脳組織を用いてスフィンゴ脂質をセラミド以外にも広げて網羅的に測定した研究はありませんでした。そこで国際共同研究グループは、質量分析装置を用いて100種類以上のスフィンゴ脂質を、統合失調症死後脳の前頭葉(主に灰白質からなる)と脳梁(白質)に分けて定量しました(図1B)。
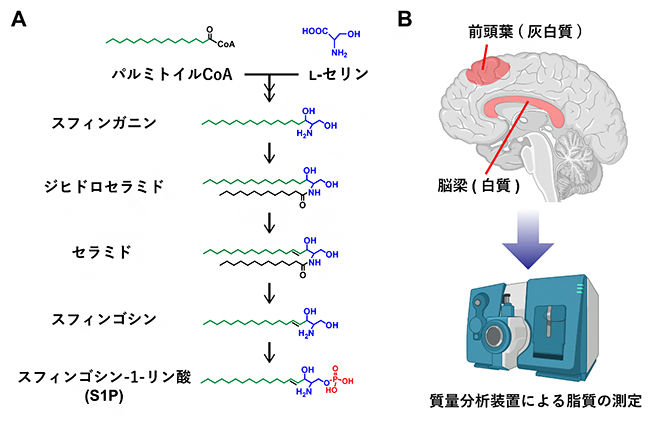
図1 スフィンゴシン-1-リン酸(S1P)の生合成経路と解析した脳部位と質量分析装置
- A:主要なスフィンゴ脂質の生合成は、パルミトイルCoAとアミノ酸のL‐セリンの縮合で始まり、セラミドやS1Pが合成される。S1Pのリン酸基を赤で示す。
- B:質量分析装置を用いて、統合失調症死後脳を前頭葉(灰白質)と脳梁(白質)に分けて、100種類以上のスフィンゴ脂質を定量した。
その結果、S1Pだけが統合失調症の脳梁のみで約30%低下していました(図2A)。この低下には、サンプルの年齢や性別、服薬歴、罹病期間など、疾患以外の因子による影響はありませんでした。
精神疾患は、複数の疾患(病名)の間で原因が重なる部分と異なる部分があることが想定されているため、S1P含量の低下が統合失調症という疾患に特異的なものであるかどうかを調べることにしました。そこで、うつ病と双極性障害の脳梁でもS1P含量を測定しましたが、対照群との違いはありませんでした(図2A)。次にS1Pの低下が脳梁という白質に特異的なものか調べるために、三つの疾患の前頭葉(主に灰白質からなる)でも測定しましたが、対照群との違いはありませんでした。よってS1P含量の低下は、統合失調症の白質に特異的なものと考えられます。なお、脳梁には、前頭葉と比較して約10倍高濃度のS1Pが存在します(図2AとBの対照群を比較)。
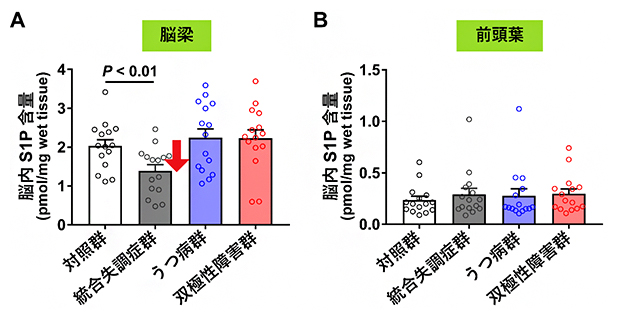
図2 死後脳におけるS1P含量
- A:脳梁でのS1P含量。統合失調症群でのみ、対照群と比較してS1P含量の低下(約30%)が見られた。
- B:前頭葉でのS1P含量。統合失調症群、うつ病群、双極性障害群とも、対照群と比較してS1P含量の違いは見られなかった。
次に、統合失調症の脳梁でS1P含量の低下が生じている原因を調べるために、S1Pの合成・分解に関わる9種類の酵素をコードする遺伝子の発現を調べました(図3A)。その結果、S1Pの分解にたずさわる脂質リン酸フォスファターゼ遺伝子(PLPP3)とS1Pリアーゼ遺伝子(SGPL1)の発現が、統合失調症で上昇していました(図3B)。PLPP3とSGPL1を比べると、①PLPP3はSGPL1に比較して脳梁での発現レベルが約5倍高い、②PLPP3レベルが高いほどS1P含量は低くなっているという結果でしたが、SGPL1レベルとS1P含量は相関していませんでした。そのため、統合失調症の脳梁でのS1P含量の低下は、主にPLPP3による分解系が亢進した結果であると考えられました。
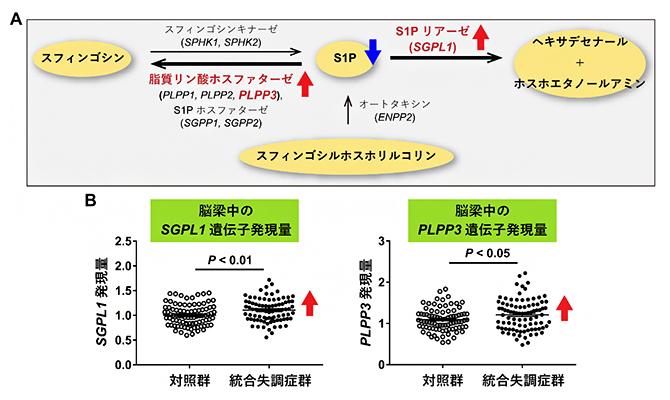
図3 S1Pの合成・分解と関連する遺伝子の発現量
- A:S1Pは、スフィンゴシンキナーゼ(SPHK1、SPHK2)でスフィンゴシンから合成されるとともに、オートタキシン(ENPP2)でスフィンゴシルホスホリルコリンから合成される。一方、脂質リン酸ホスファターゼ(SGPP1、SGPP2、PLPP1-3)およびS1Pホスファターゼ(SGPP1、SGPP2)でスフィンゴシンに分解され、S1Pリアーゼ(SGPL1)でヘキサデセナールとホスホエタノールアミンに分解される。合計9種類の酵素が関わっている。
- B:SGPL1遺伝子(左)とPLPP3遺伝子(右)の発現レベルが、対照群と比べ統合失調症群の脳梁で上昇していた。
S1Pは、S1P受容体に結合して生理作用を発揮します(図4A)。ヒトやマウスの生体内には5種類のS1P受容体(S1PR1-5)があることが知られていますが、ヒトとマウスの死後脳では1型受容体(S1PR1/S1pr1)遺伝子と5型受容体(S1PR5/S1pr5)遺伝子の発現量が多く、4型受容体(S1PR4/S1pr4)遺伝子の発現は検出されませんでした(ヒトの場合:図4B)。統合失調症の脳梁で、1型、2型、3型、5型S1P受容体遺伝子の発現レベルを調べたところ、1型(S1PR1)と5型(S1PR5)遺伝子の発現レベルが健常対照群死後脳の脳梁に比較して有意に上昇していました(図4C)。
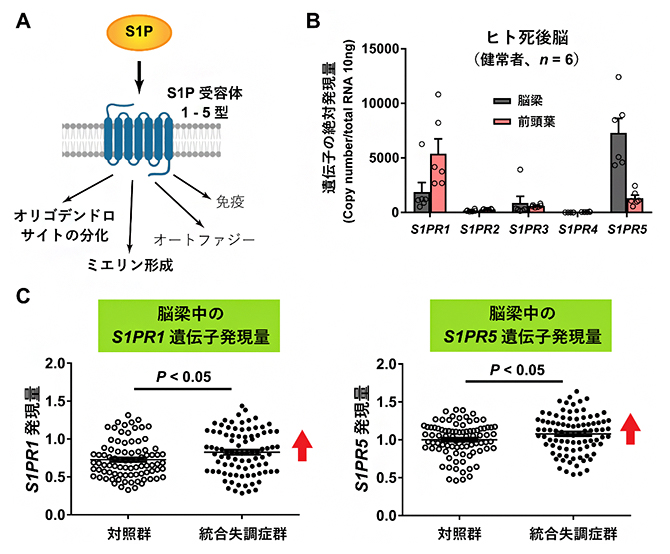
図4 S1Pの受容体および遺伝子発現
- A:S1Pの受容体には、1型から5型まであり(S1PR1-5)、S1Pが結合することで、グリア細胞のオリゴデンドロサイトの分化やミエリン形成が進み、またオートファジーや免疫反応が生じることが知られている。
- B:ヒト死後脳におけるS1P受容体1型から5型(S1PR1-5)までの遺伝子の絶対発現量。1型(S1PR1)と5型(S1PR5)の遺伝子発現量が多く、4型(S1PR4)の遺伝子の発現は、脳梁、前頭葉とも検出されなかった。
- C:S1P受容体1型(S1PR1)と5型(S1PR5)の遺伝子発現レベルが、対照群と比べ統合失調症群の脳梁で上昇していた。
また、S1P含量が低いほどS1PR1レベルが高いという関係が見られましたが、S1PR5レベルとS1P含量の間には相関関係はありませんでした。このことから、S1P含量の低下に伴って代償的にS1PR1の発現上昇が生じている可能性が考えられました。なお、マウスでS1PR1をノックアウトすると、脳の発達に異常を来たし、ミエリンの厚さが減少することが報告されています。このことからも、S1P含量の低下は統合失調症で報告されている白質異常の分子基盤の一つになっている可能性があります。
今後の期待
今回の研究から、シグナル分子として重要なスフィンゴシン-1-リン酸(S1P)が統合失調症の脳で低下している可能性がはじめて明らかになりました。S1Pはいろいろな生理活性を持つことが知られており、これまでにS1Pシグナルに対する多くの化合物が合成されています。そのうちいくつかは治療薬として使われ、未承認の化合物の多くも臨床治験の段階に入っています。例えば、フィンゴリモドという化合物はS1P受容体に作用しますが、多発性硬化症という脳神経の病気に使われています。今回解析したS1Pの分解酵素であるSPGL1に作用する化合物は、関節リウマチの治療薬として現在臨床試験が行われています。
統合失調症に対する治療薬は、神経伝達物質の受容体に作用する化合物以外にはほとんどないのが現状ですが、今回の結果から、S1Pシグナルに作用する化合物が、統合失調症の新たな治療薬として有望であることが示唆されました。
補足説明
- 1.統合失調症
代表的な精神疾患であり、人口の約1%という比較的高い生涯発症率を持つ。多くは思春期から壮年期の間に発症し、幻覚や妄想に代表される「陽性症状」、感情の平板化、うつ様症状に代表される「陰性症状」、および「認知機能の低下」を伴う。ドーパミンと呼ばれる神経伝達物質の作用を抑える薬剤の投与が治療の中心となるが、その治療効果は不十分であったり、再燃を繰り返すうちに次第に重篤化したりすることも多い。そのため、発症メカニズムの理解、それに基づく根本的な治療法や予防法の開発が長く望まれている。 - 2.白質
中枢神経系で主として有髄神経線維から成る部分。有髄神経線維のミエリンが生体膜の構成成分である脂質を豊富に含んで白色に見えることから、この名がある。 - 3.スフィンゴ脂質
脂質は、単純脂質と複合脂質(リン酸や糖、塩基などを含む脂質)、誘導脂質(脂質の加水分解産物で水に不溶のもの)に大きく分類され、スフィンゴ脂質は複合脂質に属する。スフィンゴ脂質は、スフィンゴイド塩基(スフィンゴシンなど)を骨格とした、スフィンゴ糖脂質やスフィンゴミエリンなどの脂質の総称。細胞膜や神経細胞のミエリンに豊富に含まれる。
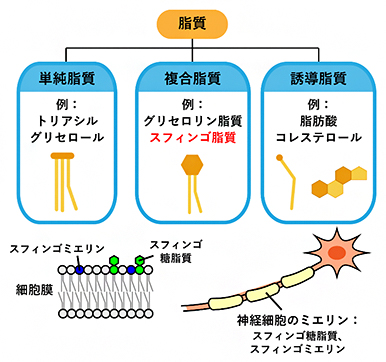
- 4.スフィンゴシン-1-リン酸(S1P)
スフィンゴ脂質の一種で、生理活性シグナル分子として知られている。近年はS1Pの合成・分解に関わる酵素やS1Pの受容体を標的として、がんや自己免疫疾患の治療薬の開発が活発に進められている。S1Pはsphingosine-1-phosphateの略。 - 5.S1P受容体
S1Pの受容体は5種類が同定されており(S1PR1-5)、S1Pは受容体を介して細胞の増殖や分化、神経機能や免疫反応に関与することが明らかになっている。 - 6.前頭葉
脳の大脳皮質のうち、大脳半球の前部の領域。灰白質で構成される。 - 7.灰白質
中枢神経系で神経細胞体の密集している部分。 - 8.脳梁
左右の大脳半球を連絡する神経線維の巨大な束で構成される白質領域。 - 9.質量分析装置
分子をイオン化し、その質量数と数を測定することにより、目的分子の同定や定量を行う装置。 - 10.うつ病
気分の落ち込みや意欲の低下などの精神的な症状や、体のだるさや不眠などといった身体的な症状が現れることのある精神疾患。 - 11.双極性障害
躁状態(気分が高ぶった状態)とうつ状態を繰り返す精神疾患。躁うつ病ともいわれる。 - 12.神経伝達物質
シナプス(神経細胞間などに形成される神経活動を伝える接合部位)で、情報伝達を介在する物質。ドーパミンやセロトニンは代表的な神経伝達物質である。 - 13.核磁気共鳴画像(MRI)
磁力と電磁波の力を使って体内の状態を断面像として描写する検査。MRIはMagnetic Resonance Imagingの略。 - 14.ミエリン
神経軸索を渦巻き状に取り巻いている膜で、絶縁体として神経興奮伝達を助けている。中枢神経系では、オリゴデンドロサイトが多くの突起を出してミエリンを形成している。 - 15.セラミド
スフィンゴ脂質の一種。構造式は図1Aを参照。セラミドに多様な側鎖が結合することで、スフィンゴ糖脂質やスフィンゴミエリンなどの複雑な構造のスフィンゴ脂質が合成される。また、皮膚の角層の細胞間における物質透過バリア構成成分としても知られ、近年は化粧品などの成分として利用されている。統合失調症患者の皮膚において、セラミド含量が低下していることが報告されている。
国際共同研究グループ
理化学研究所
脳神経科学研究センター
分子精神遺伝研究チーム
チームリーダー 吉川 武男(よしかわ たけお)
研究員 江崎 加代子(えさき かよこ)
研究員 シャビーシュ・バラン(Shabeesh Balan)
研究員 島本(光山) 知英(しまもと・みつやま ちえ)
生体物質分析支援ユニット
専門技術員 岩山 佳美(いわやま よしみ)
開拓研究本部 佐甲細胞情報研究室
客員主幹研究員 平林 義雄(ひらばやし よしお)
The Florey Institute of Neuroscience and Mental Health(オーストラリア)
教授 ブライアン・ディーン(Brian Dean)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費補助金若手研究(B)「神経毒性スフィンゴ脂質による精神疾患発症のメカニズム解明(研究代表者:江崎加代子)」、同若手研究「ヒト死後脳を用いた統合失調症の病態メカニズムとスフィンゴ脂質の関連の解明(研究代表者:江崎加代子)」、同挑戦的研究(開拓)「スフィンゴ脂質代謝変化を伴う精神疾患病態メカニズムの分子基盤の解明」(研究代表者:吉川武男)、同新学術領域研究(研究領域提案型)「マルチスケール精神病態の構成的理解(領域代表者:林(高木)朗子)」、および日本医療研究開発機構(AMED)革新的先端研究開発支援事業(AMED-CREST)『画期的医薬品等の創出をめざす脂質の生理活性と機能の解明(研究開発総括:横山信治)』の「光による脂質の同定制御観察技術すなわちオプトリピドミクスの創生(研究開発代表者:瀬藤光利)」による支援を受けて行われました。
原論文情報
- Kayoko Esaki, Shabeesh Balan, Yoshimi Iwayama, Chie Shimamoto-Mitsuyama, Yoshio Hirabayashi, Brian Dean, Takeo Yoshikawa, "Evidence for Altered Metabolism of Sphingosine-1-phosphate in the Corpus Callosum of Patients with Schizophrenia", Schizophrenia Bulletin, 10.1093/schbul/sbaa052
発表者
理化学研究所
脳神経科学研究センター 分子精神遺伝研究チーム
理化学研究所 脳神経科学研究センター 分子精神遺伝研究チーム
研究員 江崎 加代子(えさき かよこ)
チームリーダー 吉川 武男(よしかわ たけお)
 江崎 加代子
江崎 加代子
 吉川 武男
吉川 武男
報道担当
理化学研究所 広報室 報道担当
お問い合わせフォーム
産業利用に関するお問い合わせ
AMED事業に関する問合せ先
日本医療研究開発機構 シーズ開発・研究基盤事業部 革新的先端研究開発課
Tel: 03-6870-2224
Email: kenkyuk-ask [at] amed.go.jp
※[at]は@に置き換えてください。
