2020年11月24日
理化学研究所
東京大学大学院理学系研究科
科学技術振興機構
ロボットによる微生物の大規模進化実験
-薬剤耐性進化を支配する拘束条件を発見-
理化学研究所(理研)生命機能科学研究センター多階層生命動態研究チームの前田智也基礎科学特別研究員、古澤力チームリーダー(東京大学大学院理学系研究科教授)、東京大学大学院理学系研究科の岩澤諄一郎大学院生の共同研究チームは、大腸菌の進化実験データを解析し、その薬剤耐性進化を支配する拘束条件を明らかにしました。
本研究成果は、抗生物質[1]への耐性獲得を抑制する手法や新しい抗生物質の開発への貢献に加え、微生物進化の予測と制御による工学・農学分野への応用が期待できます。
今回、研究チームは、独自に開発した進化実験ロボット[2]を用い、微生物を長期に培養し薬剤耐性進化の過程をハイスループットに解析できる仕組みを構築しました。それを用いて、微生物の一種である大腸菌をさまざまな薬剤を添加した環境で進化させ、その遺伝子発現量やゲノム配列変化などのデータから機械学習[3]により、薬剤耐性進化を特徴づける状態量[4]の抽出に成功しました。その解析から、さまざまに異なる薬剤に対する進化が少数の状態量で説明できることが示され、薬剤耐性進化に対する拘束条件が明らかになりました。
本研究は、オンライン科学雑誌『Nature Communications』(11月24日付)に掲載されます。
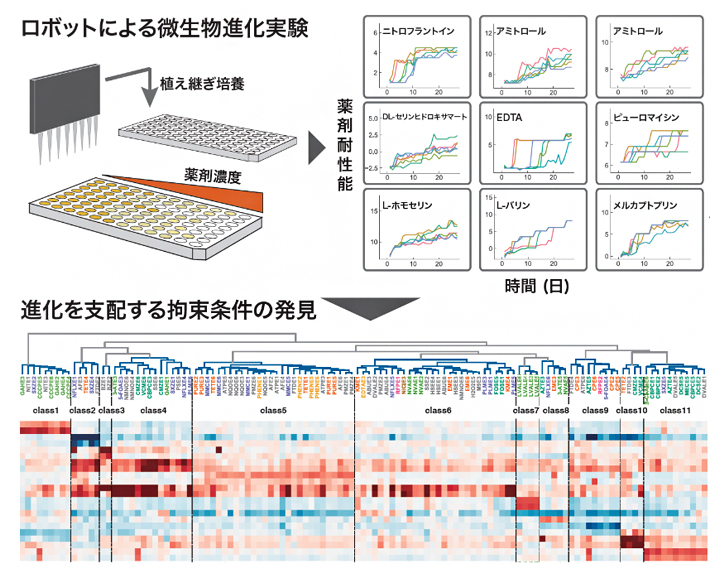
ロボットによる微生物進化実験の模式図とその結果の一部
背景
さまざまな抗生物質に耐性を持つ病原菌である多剤耐性菌[5]の出現が、世界的な問題となっています。新しい抗生物質を開発したとしても、臨床で使っているうちにその抗生物質に対する新しい耐性菌が出現してしまうため、耐性菌の対策を講じにくいのが現状です。耐性菌は、突然変異などにより薬剤に適応した病原菌が選択される、いわゆるダーウィン進化[6]によって出現すると考えられています。したがって、耐性菌の対策には、病原菌の進化メカニズムそのものを理解することが重要となります。しかし、薬剤耐性進化の過程はゲノム配列の変化に加え、細胞の状態変化といった多数の要素が絡み合う複雑な仕組みであるため、その全貌の理解にはまだ至っていません。
微生物の進化メカニズムを調べる際の有効な手法の一つに「進化実験」があります。微生物の進化実験とは、薬剤を添加した環境で微生物を長期に植え継ぎ、遺伝子への突然変異の蓄積と選択を繰り返すことで、進化の過程を実験室で再現することです。これにより、対象とする微生物のゲノム配列や遺伝子発現量などが、どのような変化を経て耐性を獲得するか詳細に調べることができます。また、特定の薬剤を添加した環境で進化し耐性を獲得した微生物が、他の薬剤に対してどのように耐性を変化させるかを調べることで、耐性株の出現抑制に効果があると期待される複数の薬剤の組み合わせを見つけることができます。そのため、進化実験に用いる薬剤を増やすと、より多くの効果的な薬剤の組み合わせを見つけられると考えられます。
しかし、人の手で行うことができる実験数の少なさなどにより、進化実験はこれまで十数種類の薬剤でしか行われてきませんでした注1)。また、薬剤への耐性が変化する際、細胞内のさまざまな状態量(4,000以上ある遺伝子の発現量の変化や、ゲノムの配列変化など)が耐性化する前と比べて大きく変化してしまうため、どのような変化が実際の薬剤耐性進化のメカニズムに本質的に関わっているのかを調べるのは困難でした。
- 注1)2014年12月17日プレスリリース「バクテリアの抗生物質耐性を予測する新手法を開発」
研究手法と成果
今回、共同研究チームは、ラボオートメーションを用いた進化実験ロボット(図1左)を開発し、95種類の薬剤をそれぞれ添加した環境で、微生物の一種である大腸菌を植え継ぎ培養するという、これまでになかったスケールで進化実験を行いました。また、それぞれの薬剤により耐性進化した大腸菌の性質を調べるため、一つの薬剤への耐性獲得により、他の薬剤への耐性がどのように変化したかを系統的に調べました。その結果、耐性菌の出現抑制に効果があると考えられる157の薬剤の組み合わせを発見しました。これらの中には新しく判明した組み合わせも多く、病原菌の耐性獲得を抑制する手法の開発に貢献すると期待できます。
次に、薬剤耐性メカニズムを調べるため、耐性進化した大腸菌それぞれについて、ゲノム変異データと遺伝子発現量データを取得しました。しかし、そこから得られたデータは大腸菌を表す多くの状態量からなり、かつノイズも多いため、そのままでは解釈が困難でした。そのため、機械学習の手法であるランダムフォレスト回帰[7]と主成分分析[8]を組み合わせて、薬剤耐性との関係を解釈しやすい少数の重要な状態量を得る手法を開発しました(図1右)。同手法により、耐性進化と関連しない情報を無視できるようになり、薬剤耐性変化の予測に重要な213の遺伝子を明らかにしました。
さらに今回の解析により、多様な薬剤下で耐性進化した大腸菌は、細胞膜に存在し薬剤を細胞外に排出するポンプが過剰に働いている状態や、薬剤を細胞内に取り込む透過孔を閉じた状態、ストレス応答遺伝子群を過剰発現させた状態など、わずか15種の細胞状態のクラスターに分かれることが明らかになりました。このことは、大腸菌はさまざまな薬剤の添加に対して変幻自在に耐性を獲得できるわけではなく、むしろあらかじめ限られた少数の耐性化戦略しか潜在的に備えていないことを意味しています。この結果は、薬剤耐性化のメカニズムが比較的少数の状態量で記述できることを示し、薬剤耐性進化に対する拘束条件が明らかになりました。この拘束条件は、耐性進化を予測する手法開発の基盤となります。

図1 進化実験ロボットと耐性株の定量データからの特徴抽出
- (左)進化実験ロボットの外観。クリーンブース内に設置された自動分注器とそれに接続されたシェーカーインキュベーター・マイクロプレートリーダーなどから構成される。16,000を超える独立培養系列を全自動で維持することが可能である。
- (右)耐性株の遺伝子発現量とさまざまな薬剤に対する耐性能から、ランダムフォレスト回帰などの機械学習の手法を用いることにより、耐性獲得に関連する遺伝子情報の抽出を行う。
今後の期待
今回の実験から得られたデータとその解析手法は、微生物の進化過程を予測・制御するための基盤になると考えられます。それによって、病原菌の抗生物質耐性進化を抑制する手法の開発や、工学・農学分野における有用微生物の育種に応用することが期待できます。
また、生物の大規模なデータはさまざまな実験系で取得されている一方で、その解釈は必ずしも容易ではありません。本研究で用いられた解析手法はこうした系にも適応可能であり、増え続ける生物データの解釈に貢献する基盤技術となると期待できます。
補足説明
- 1.抗生物質
微生物などの増殖や生理機能を阻害する化学物質のこと。感染症の治療などに広く用いられる。 - 2.進化実験ロボット
クリーンブース内に設置された自動分注器と、それに接続されたシェーカーインキュベーター・マイクロプレートリーダーなどから構成される。コンピュータ制御により、微生物の増殖の定量・植え継ぎ操作・培養の全てを自動で行うことができる。
(参考リンク:Youtube : Fully-automated culture system in Furusawa lab.) - 3.機械学習
膨大なデータをコンピュータに入力し、その中にある既知の特徴を繰り返しコンピュータに学習させるか、もしくはデータそのものからコンピュータに規則性を発見させることで、未知のデータに対する解答を自動で得る手法。 - 4.状態量
その生物の状態を表す量のこと。ここでは、遺伝子発現量や薬剤耐性能といったさまざまな定量データと、それらのデータから機械学習の手法によって計算される特徴量を指す。 - 5.多剤耐性菌
異なる作用を持つ複数の抗生物質に耐性を持つ微生物のこと。抗生物質による治療が難しい場合があるため、その出現が医学上の大きな問題となっている。 - 6.ダーウィン進化
生物がゲノム配列の変化などによってその性質の多様性を持ち、さらに環境条件に応じて選択が働くことにより、世代を経て性質が変化していく現象のこと。 - 7.ランダムフォレスト回帰
多数の状態量から目的変数(本研究では薬剤耐性の度合い)を予測するための統計的手法。本手法を通して、それぞれの状態量が目的変数の予測にどれくらい貢献しているかを計算できる。 - 8.主成分分析
遺伝子発現量データなどの多変量データから特徴的な変動を示す成分を取り出す統計的手法。相関を持つ変数をひとまとめにすることで、互いに相関の無い少数の成分でデータを説明できる。
研究支援
本研究は、日本学術振興会(JSPS)科学研究費補助金基盤研究(S)「細胞の可塑性とロバストネスの状態論(研究代表者:金子邦彦)」、同新学術領域研究(研究領域提案型)「進化の制約と方向性 ~微生物から多細胞生物までを貫く表現型進化原理の解明~(領域代表者:倉谷滋)」、科学技術振興機構(JST)戦略的創造研究推進事業 ERATO「深津共生進化機構プロジェクト(研究総括:深津武馬)」などによる支援を受けて行われました。
原論文情報
- Tomoya Maeda, Junichiro Iwasawa, Hazuki Kotani, Natsue Sakata, Masako Kawada, Takaaki Horinouchi, Aki Sakai, Kumi Tanabe, and Chikara Furusawa, "High-throughput laboratory evolution reveals evolutionary constraints in Escherichia coli", Nature Communications, 10.1038/s41467-020-19713-w
発表者
理化学研究所
生命機能科学研究センター 多階層生命動態研究チーム
基礎科学特別研究員 前田 智也(まえだ ともや)
チームリーダー 古澤 力(ふるさわ ちから)
(東京大学 大学院理学系研究科 生物普遍性研究機構 教授)
 前田 智也
前田 智也
 古澤 力
古澤 力
東京大学 大学院理学系研究科
大学院生 岩澤 諄一郎(いわさわ じゅんいちろう)
 岩澤 諄一郎
岩澤 諄一郎
報道担当
理化学研究所 広報室 報道担当
お問い合わせフォーム
東京大学大学院理学系研究科・理学部 広報室
Email:kouhou.s [at] gs.mail.u-tokyo.ac.jp
科学技術振興機構 広報課
Tel: 03-5214-8404 / Fax: 03-5214-8432
Email: jstkoho [at] jst.go.jp
産業利用に関するお問い合わせ
JST事業に関すること
科学技術振興機構 研究プロジェクト推進部
内田 信裕(うちだ のぶひろ)
Tel: 03-3512-3528 / Fax: 03-3222-2068
Email: eratowww [at] jst.go.jp
