理化学研究所(理研)生命機能科学研究センター個体パターニング研究チームの高瀬比菜子研究員、羽原興子研究パートタイマーらの国際共同研究グループは、マウスを用いて、卵巣内で休眠状態にある「原始卵胞[1]」が成長するために必要な分子機構を発見しました。
本研究成果は、女性不妊の原因の一つである原始卵胞の不十分な活性化メカニズムへの理解と、将来的な不妊治療への応用が期待できます。
哺乳類の母体内では、生殖細胞である未熟な卵子(卵母細胞)[2]が、体細胞である前顆粒膜細胞[3]に囲まれた原始卵胞という形で眠っています。性成熟後に原始卵胞は徐々に活性化し、卵母細胞の成長とともに前顆粒膜細胞が顆粒膜細胞[3]に分化して、成熟した卵胞となります。生殖サイクルの中で一度に卵子を消費し尽さないためには、原始卵胞の活性化が精密に調整される必要があります。
今回、国際共同研究グループは、前顆粒膜細胞から顆粒膜細胞への分化には、前顆粒膜細胞が分泌したWnt[4]タンパク質が自らの細胞に作用するWntシグナル経路[4]が必須であることを突き止めました。このWntシグナル経路を抑制すると原始卵胞の活性化は不完全となり、卵子の成長も間接的に阻害されます。これらの結果から、前顆粒膜細胞における自己分泌型のWntシグナルは、原始卵胞の活性化に関して「許容的な」役割[5]を果たしていることが明らかになりました。
本研究は、科学雑誌『Development』(5月号)、オンライン版(4月29日付)に掲載されました。
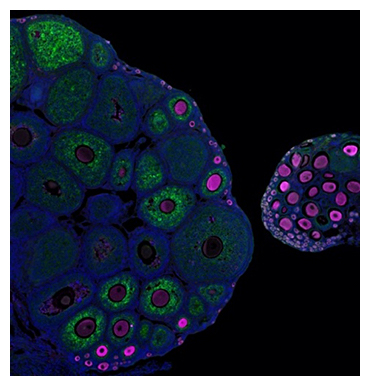
Wntシグナルが機能しない卵巣(右)は、原始卵胞が活性化せず不妊を引き起こす
背景
哺乳類の雌では、卵子のもととなる細胞(卵母細胞)は胎児期に増殖し、卵巣に蓄えられ、出生後に新しく作り出されることはありません。一つ一つの卵母細胞は、母体の体細胞である扁平な前顆粒膜細胞に包まれた「原始卵胞」と呼ばれる構造をとり、活性化されるまで休眠しています。性成熟後に原始卵胞は徐々に活性化され、卵母細胞は成長を開始し、前顆粒膜細胞は顆粒膜細胞に分化して成熟した卵胞となり、排卵に至るという周期的な生殖サイクルを支えます。卵母細胞の成長には体細胞からのサポートが必要であるため、卵母細胞と前顆粒膜細胞は同じタイミングで活性化する必要があります。原始卵胞の活性化異常は、早発卵巣不全[6]など、不妊に関わる病気の原因となり得ます。
卵母細胞については、休眠に関わる転写因子[7]FOXO3[8]が同定されるなど活性化メカニズムについて報告されていますが、前顆粒膜細胞の活性化がどのように引き起こされるのかよく分かっていませんでした。そこで、国際共同研究グループは、前顆粒膜細胞で活性化しているシグナル伝達経路を探索し、原始卵胞活性化のメカニズムを明らかにすることを目指しました。
研究手法と成果
国際共同研究グループは、さまざまな臓器の発生段階において多岐にわたる機能を発揮する分泌型の糖タンパク質Wntに着目しました。哺乳類が持つ19種類のWnt遺伝子全ての発現パターンを生後3週齢のマウスで調べたところ、Wnt4、Wnt6、Wnt11が原始卵胞の活性化と同じタイミングで、前顆粒膜細胞および顆粒膜細胞で発現していることを見いだしました。
次に、Wntシグナルを受容する細胞を調べるため、Wntシグナルを受け取った細胞が蛍光タンパク質を発現する遺伝子改変マウスを利用し、卵巣でのWntシグナルの活性化を解析しました。その結果、Wntシグナルは原始卵胞の前顆粒膜細胞で最も強く活性化し、前顆粒膜細胞の活性化後には速やかにシグナルが抑えられることが判明しました(図1)。これは、前顆粒膜細胞が分泌したWntが自分自身に作用していることを示唆します。Wntの空間的・時間的な発現パターンはその機能と密接に関わっていることから、前顆粒膜細胞の自己分泌により活性化したWntシグナル経路が原始卵胞の活性化に関与している可能性が考えられました。
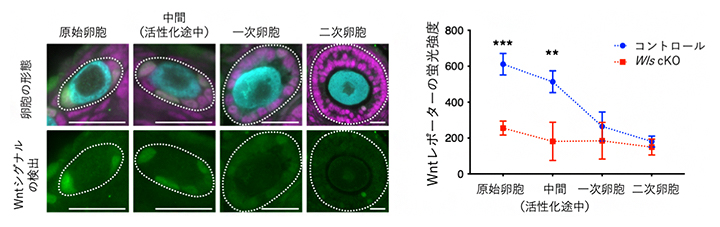
図1 前顆粒膜細胞でのWntシグナルの活動状態
- (左)卵巣でのWntシグナルの活動を検出するため、緑色蛍光タンパク質の発現を蛍光顕微鏡で観察した。卵母細胞は水色、(前)顆粒膜細胞はマゼンタで染色している。卵胞の輪郭は白い点線で示す。スケールバーは20マイクロメートル(μm、1μmは1000分の1mm)。
- (右)前顆粒膜細胞および顆粒膜細胞における、緑色蛍光タンパク質の強度を測定した。原始卵胞を構成する前顆粒膜細胞で強いWntシグナルの入力が検出され、活性化後の一次卵胞と二次卵胞では、顆粒膜細胞のWntシグナルは弱いことが明らかになった(コントロール、青)。Wntシグナルの活性化で発現する緑色蛍光タンパク質(Wntレポーター)は、Wntシグナルを抑制したWls cKOマウスではほとんど検出されない(赤)。
そこで、Wntシグナルが原始卵胞の活性化に必要であるかを検証するため、Wntの分泌に必須のWntless(Wls)[9]遺伝子を、顆粒膜細胞を含む卵巣の体細胞で特異的にノックアウトした「Wls 条件付きノックアウトマウス(Wls cKOマウス)」を作出し、卵巣でWntシグナルを抑制した場合の表現型を解析しました。Wls cKOマウスは健康に成長しましたが、卵巣のサイズは小さく、不妊となりました(図2)。また、血液中の卵胞刺激ホルモンの濃度が増加するなど、ヒトの早発卵巣不全患者と類似したホルモン動態も観察されました。
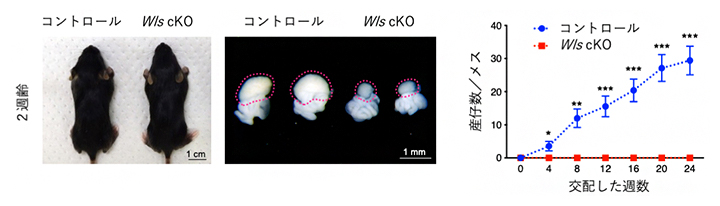
図2 Wls 条件付きノックアウトマウス(Wls cKOマウス)の表現型
- (左)Wls cKOマウスは正常な発育を示すが、卵巣は著しく小さい。卵巣の輪郭は赤点線で示した。
- (右)野生型の雄マウスと交配すると、正常マウス(コントロール)はおよそ月に1回程度の出産をするが(青)、Wls cKOマウスは不妊であり産仔が得られない(赤)。
さらに、Wls cKOマウスの原始卵胞では異常が見られませんでしたが、卵母細胞が活性化し成長を開始しても、顆粒膜細胞は扁平のままで未熟な性質を示しました(図3)。つまり、前顆粒膜細胞の活性化にはWntシグナルが必要であり、Wls cKOマウスでは卵母細胞と前顆粒膜細胞の活性化状態に乖離が起きていると考えられます。
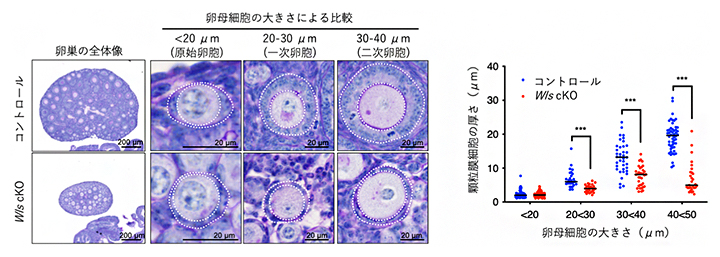
図3 Wntシグナルを抑制した場合の卵巣の表現型
- (左)扁平な前顆粒膜細胞は、卵母細胞の成長と協応して立方体状の顆粒膜細胞へ分化する(上段)。一方、Wls cKOマウスでは卵母細胞が大きくなり始めても顆粒膜細胞は正常に分化せず、扁平なままである(下段)。卵母細胞と卵胞の輪郭は白点線で示した。
- (右)Wntシグナルがない場合、原始卵胞(卵母細胞の大きさがおよそ20μm未満)では異常が見られないが、顆粒膜細胞は活性化の刺激に応答して厚くなることができない。
それでは、前顆粒膜細胞が活性化できない卵胞では、卵母細胞の成長はどうなっていくのでしょうか?Wls cKOマウスの卵母細胞は、成長を開始するものの、発育の遅延が見られました。さらには、休眠状態の維持に重要な転写因子FOXO3が核内にとどまるなど、卵母細胞が休眠状態から脱していない特徴を示しました。したがって、卵母細胞の成長にはWntシグナルによって正常に分化した顆粒膜細胞が必要であると考えられます。
最後に、Wntシグナルのみで前顆粒膜細胞の活性化を引き起こすことができるかを検証しました。Wntは細胞膜上の受容体に結合すると、細胞内のβカテニン[4]を活性化し、シグナルを伝えます。Wntシグナルを恒常的に活性化するβカテニン活性型変異遺伝子を利用して、前顆粒膜細胞でWntシグナル経路を活性化する実験を行ったところ、前顆粒膜細胞は厚くなったものの、原始卵胞の活性化を引き起こすには至りませんでした。この結果は、原始卵胞の活性化において、Wntシグナルは必要であっても十分ではなく、「許容的」な役割を果たすことを示しています(図4)。一方、卵巣培養系を用いた解析では、Wntシグナルを活性化する薬剤の投与によりWls cKOマウスの顆粒膜細胞の分化不全が正常に戻り、また、野生型マウスの卵胞においても顆粒膜細胞の分化を促進することが示されました。
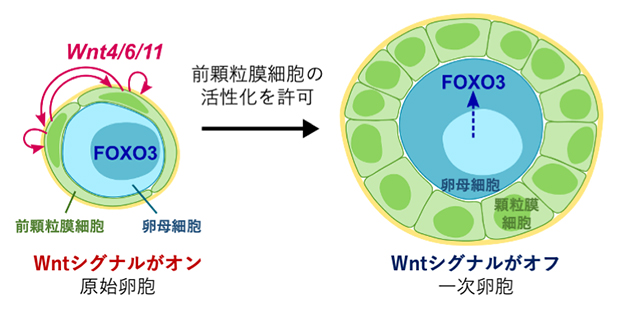
図4 原始卵胞の活性化メカニズムのモデル
本研究から示された、原始卵胞活性化におけるWntシグナルの役割を示すモデル。前顆粒膜細胞ではWnt4、Wnt6、Wnt11が発現しており、自分自身でWntシグナルを受け取っている。Wntシグナルは前顆粒膜細胞を活性化し顆粒膜細胞へと分化する際に「許可」を与え、正常な原始卵胞の活性化に至る。
今後の期待
今回、原始卵胞が正しく活性化され、発育するためには前顆粒膜細胞におけるWntシグナルが重要な役割を果たすことが明らかになりました。卵母細胞の成長には十分に活性化した顆粒膜細胞が必要と考えられるため、Wnt活性化剤により培養系における顆粒膜細胞の分化促進が確認されたことは、将来的には、ヒトや希少動物の原始卵胞を効率的に活性化する技術などへ応用できる可能性があります。
今後、前顆粒膜細胞と卵母細胞間の情報伝達を担う分子の同定などにより、原始卵胞活性化メカニズムの包括的な理解が進むことが期待できます。
補足説明
- 1.原始卵胞
卵母細胞と(前)顆粒膜細胞、莢膜(きょうまく)細胞からなる構造を卵胞と呼ぶ。原始卵胞は休眠状態の卵胞を指し、活性化すると発育卵胞(一次卵胞、二次卵胞)へと変化する。活性化後は休眠状態に戻ることはできず、卵子となるか、発育途中で閉鎖する運命にある。 - 2.卵子、卵母細胞
雌性生殖細胞のこと。卵母細胞は減数分裂と成長を経て受精可能な卵子へと分化する。 - 3.前顆粒膜細胞、顆粒膜細胞
卵母細胞を取り巻いている体細胞。顆粒膜細胞は卵母細胞の発育や閉鎖に密接に関与している。扁平な前顆粒膜細胞は、活性化により立方体状の顆粒膜細胞へと分化する。 - 4.Wnt、Wntシグナル経路、βカテニン
分泌因子が受容体に結合した刺激は、細胞内タンパク質の連鎖的なリン酸化などを介して、最終的に遺伝子の発現制御につながる。この一連の反応をシグナル伝達と呼び、Wntシグナル経路はシグナル伝達の様式の一つ。Wntは分泌型の糖タンパク質であり、細胞膜上の受容体に結合することで作用を発揮し、さまざまな臓器や発生過程において細胞の増殖、分化、未分化性の制御などに関わる。βカテニンは、Wnt受容体Frizzledの下流で機能するシグナル関連因子。なおWntシグナル伝達経路には、本研究で着目したβカテニンが関与する古典的Wntシグナル伝達経路以外にも、平面内細胞極性(PCP)経路、カルシウム経路など複数が知られている。Wntは、ショウジョウバエの遺伝子winglessとマウス乳がん遺伝子int-1から名付けられた。 - 5.許容的な役割
細胞の分化誘導には、「誘導的」または「許容的」な様式が存在する。米国の発生生物学者Howard Holtzerが提唱した。分化の方向性を決定し、さらに進行させるものを「誘導的」と呼び、分化方向を決定するが分化誘導因子とは独立したものを「許容的」と呼ぶ。 - 6.早発卵巣不全
40歳未満で、卵巣の機能低下により無月経となる疾患。40歳未満の女性の約1%が発症すると推定されている。 - 7.転写因子
DNAに結合して遺伝子の転写を促進、または抑制する働きを持つタンパク質の総称。多くの場合において、シグナル伝達は最終的に転写因子による特定の遺伝子の発現変動を引き起こす。 - 8.FOXO3
転写因子の一種。休眠中の卵母細胞では核に局在するが、原始卵胞の活性化に際して核外に移行する。FOXO3はForkhead box O3の略。 - 9.Wntless(Wls)
ゴルジ体に蓄えられたWntタンパク質が細胞外へ輸送される過程に関与する遺伝子。
国際共同研究グループ
理化学研究所 生命機能科学研究センター 個体パターニング研究チーム
研究員 高瀬 比菜子(たかせ ひなこ)
研究パートタイマーⅠ 羽原 興子(はばら おきこ)
スタンフォード大学 ハワード・ヒューズ医学研究所
教授 ローランド・ヌッセ(Roeland Nusse)
ポストドクトラルフェロー カトリーナ・ローガン(Catriona Y Logan)
東京医科歯科大学 実験動物センター 疾患モデル動物解析学分野
教授 金井 正美(かない まさみ)
研究支援
本研究は、理化学研究所運営費交付金(生命機能科学研究)で実施し、日本学術振興会(JSPS)科学研究費補助金 新学術領域研究「配偶子インテグリティの構築(領域代表者:林克彦)」、同若手研究(B)「未分化精原細胞の制御におけるWntシグナルの役割(研究代表者:高瀬比菜子)」、第7回(2017年)日本分子生物学会 若手研究助成 富澤純一・桂子基金「細胞間シグナル伝達による精子幹細胞の増殖制御機構の解明(研究代表者:高瀬比菜子)」による支援を受けて行われました。
原論文情報
- Okiko Habara, Catriona Y. Logan, Masami Kanai-Azuma, Roeland Nusse, Hinako M. Takase, "WNT signaling in pre-granulosa cells is required for ovarian folliculogenesis and female fertility", Development, 10.1242/dev.198846
発表者
理化学研究所
生命機能科学研究センター 個体パターニング研究チーム
研究員 高瀬 比菜子(たかせ ひなこ)
研究パートタイマーⅠ 羽原 興子(はばら おきこ)
 羽原 興子(左)高瀬 比菜子(右)
羽原 興子(左)高瀬 比菜子(右)
報道担当
理化学研究所 広報室 報道担当
お問い合わせフォーム
