2006年にヒトiPS細胞が初めてつくられて以来、医療への応用が少しずつ進んでいます。林洋平チームリーダー(TL)は、品質の高いiPS細胞を効率良くつくるための新しい初期化因子を開発。患者由来のiPS細胞を使った再生医療の実現に近づきつつあります。

林 洋平(はやし ようへい)
バイオリソース研究センター
iPS細胞高次特性解析開発チーム
チームリーダー
1981年愛知県生まれ。2009年東京大学大学院総合文化研究科広域科学専攻生命環境科学系修了。博士(学術)。米国グラッドストーン研究所博士研究員、筑波大学などを経て、2018年より現職。
細胞移植の理想は「My iPS細胞」
iPS細胞の大きな利点は、本人の体細胞からiPS細胞をつくり、そこから必要な細胞を分化誘導できることだ。これによって拒絶反応のない移植やオーダーメイド医療が期待できる。
だが、現在は多くの人に適合するタイプの他人由来iPS細胞をあらかじめつくって貯蔵し、必要に応じて分化させるバンク方式が採用されている。患者自身の体細胞からiPS細胞をつくることは、質の良い細胞ができにくく、検証にも手間がかかる点で、現実的ではないからだ。
「もっと効率的に良質のiPS細胞をつくることができれば、『My iPS細胞』を使って本来の利点を活かす医療が実現するはず」。林TLをはじめ、多くの関係者はそう考えている。
初期化因子をつくり変える新手法
iPS細胞を作製するには、通常4種類の初期化因子を働かせて皮膚細胞などの体細胞を初期化(リプログラミング)し、どんな細胞にも分化する能力を持つ幹細胞に戻してから、目的の細胞に分化させる。
iPS細胞の品質と収率の向上を目指して、初期化因子を加えたり、別の因子に置き換えるなどの工夫がこれまでにも行われてきた。それに対して、研究チームが開発したのは初期化因子そのものの構造をつくり変えるという画期的な方法だ。
対象は、iPS細胞誕生以来使われてきた初期化因子の一つKLF4。「この因子が細胞のDNAと結合する部分のアミノ酸19個に着目し、それらを分子の小さい別のアミノ酸、アラニンに置き換えてみました。すると、ある位置のロイシンをアラニンに置き換えたときだけ、迅速にDNAに結合し、均一で高品質なiPS細胞がたくさんできたのです(図1)」
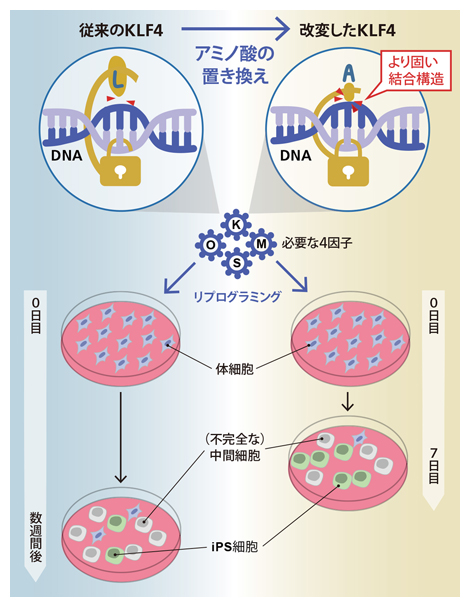
図1 KLF4改変体による高品質iPS細胞作製の効率化
KLF4のアミノ酸ロイシン(L)をアラニン(A)に置き換えた改変体を、他の初期化因子3種類とともに体細胞に導入したところ、均一で高品質なiPS細胞を効率良くつくることができた。
改変KLF4とDNAがどのように結合しているか、分子構造をコンピューターでシミュレーションしたところ、アミノ酸とDNAとの間に新しい水素結合ができて、両者がしっかり結びついていることが分かった。「いずれはコンピューター上で目的にかなう分子をデザインできるかも」と、林TLは思いを巡らす。
世界最大規模のiPS細胞バンクに期待
学生時代、林TLは発生生物学を学んだ。「生命の原理といった基礎的な関心より、実際に応用できるところに魅力を感じた」のが、専攻を選んだ理由だ。学位取得後、米国グラッドストーン研究所でiPS細胞生みの親である山中伸弥博士のもと、博士研究員を務めた。以来、iPS細胞はいつも傍らにある。
所属するバイオリソース研究センターは、生物遺伝資源を収集・保存して研究開発用に提供している。そのうち、疾患特異的iPS細胞バンクは世界最大規模で、疾患400種類の約3,400株を保存し、再生医療や薬剤開発などを行う研究機関などに提供しており、国内外から頼りにされる存在だ。その役割は今後も重みを増すことだろう。新開発の初期化因子が「My iPS細胞」実現に一歩近づくことと並んで期待される。
(取材・構成:古郡悦子/撮影:相澤正。/制作協力:サイテック・コミュニケーションズ)
関連リンク
- 2021年12月15日プレスリリース「次世代プログラミング因子KLF4改変体の開発-iPS細胞をより高効率・高品質に作製-」
この記事の評価を5段階でご回答ください
