ポイント
- 創薬研究のパートナーを目指した創薬基盤プロジェクトを始動
- 先端ライフサイエンス基盤を創薬基盤に再構築して、創薬研究を支援
- 創薬コーディネイターによる創薬コンサルティングなどの支援の実施
概要
独立行政法人理化学研究所(野依良治理事長)は、これまでライフサイエンス研究で培ってきた基盤技術を基に創薬基盤プラットフォームを構築し、外部提供を行なうことで創薬の研究開発へ貢献するため、基幹研究所(玉尾皓平所長)ケミカルバイオロジー研究領域の後藤俊男客員主管研究員をリーダーとする「創薬基盤プロジェクト」を平成22年度から開始することを予定しています。
今般、この準備の一環として、研究機関や企業などから理研の基盤技術の外部モニター利用者を募集し、実際の創薬シーズなどの研究開発についての研究支援に、試験的に取り組みます。
モニター利用を予定している技術基盤は、遺伝子情報を活用した創薬ターゲットの探索、コンピュータと化合物アレイ※1を用いたDRY/WET※2融合型スクリーニング技術、NMR※3を用いた化合物・タンパク質の相互作用解析、モデル動物を用いた疾患解析やポジトロン断層法(PET)※4による薬物動態試験など、創薬研究に有用な実効性の高い基盤技術であり、これらはモニター利用者の意見を踏まえ、平成22年度以降、創薬基盤プラットフォームとして再構築し、さらに利用価値を高めて外部提供を行ないます。
なお、モニター利用の際には、ワンストップでの創薬研究のサポートを目的として、創薬コーディネーターによる相談・企画・立案など、創薬研究のトータルソリューションを提供します。
第一次公募期間は10月31日までとし、若干数の課題選定を予定しています。
背景
人々の健康に役立つ医薬・医療技術の創出は、ライフサイエンス研究に求められている重要な課題です。医薬・医療技術は、製薬企業や医療機関が実用化を進めていきますが、その開発過程において、バイオベンチャー企業や大学など学術機関が保有する創薬シーズの役割も大きく、外部の研究成果を取り入れて創薬開発や臨床研究を進める事例も増えています。しかし、学術機関が生み出すライフサイエンス研究の成果と、医薬・医療技術の実用化の間には大きな「死の谷(ギャップ)」があり、なかなか創薬の実現に結びつかないのが現状です。医薬・医療技術の開発を活性化するためには、この「死の谷」を克服する必要があり、海外では、この「死の谷」を埋める役割はバイオベンチャー企業が担うとともに、公的研究機関の中にも、創薬分野の研究開発を支援する拠点※5が形成されています。
理研の創薬基盤の新たな取り組み
理研は、これまでにさまざまなライフサイエンス研究のプロジェクトを担当し、先端的な技術基盤を多数構築してきました。平成22年度以降、これらの技術基盤を最大限に活用して、創薬研究を効果的に推進するため、技術基盤を再構築し、創薬研究の上流から下流に至るまでの総合的な研究支援を行う「創薬基盤プロジェクト」を始動、各技術基盤を「創薬基盤プラットフォーム」として整備すべく準備を進めています(図1)。理研創薬基盤プロジェクトは、この創薬基盤プラットフォームを活用した研究開発の支援を行い、学術機関やバイオベンチャー企業が保有する「創薬シーズ」の実用化に向けてサポートを行なうことにより、製薬企業などの開発ステージに進めることを目指します。具体的には「創薬コンサルティング機能」と「創薬基盤を再構築した横断的な創薬基盤プラットフォーム」を広く社会に提供し、創薬・医療技術創出のための「仕組み」の実現に新たに取り組みます。
モニター利用者の募集について
創薬基盤プロジェクトは、新しい基盤技術の構築や外部の基盤技術とのネットワーク化により、創薬研究のトータルソリューションを目指していく研究開発拠点として、創薬・医療技術の創出に貢献していく予定です。そこで今回、創薬シーズを有する外部のモニター利用者を募り、各技術基盤・創薬コンサルティング機能を活用し、実際に創薬研究を進めながら、コメントなどの協力を得る予定です。今後は、モニター募集を行った技術基盤を軸に、広く創薬研究者などによる利用結果を反映させながら、創薬基盤プラットフォームの構築を目指します。
外部モニター利用者の募集
| 公募期間 | 2009年10月31日まで(第一次) |
|---|---|
| 対象 | 創薬シーズを有するバイオベンチャーなどの民間企業、技術移転機関(TLO)、大学、独立行政法人、大学共同利用機関、医療機関、そのほかこれに相当する法人に所属する研究者・技術者など。 |
| 応募方法 | 利用者モニター希望者は、理研創薬基盤強化プロジェクトホームページをご覧の上、メールアドレス(pharma-support [at] riken.jp)に、会社名(又は、研究機関名等)、所属部署、担当者氏名、連絡先(担当者メールアドレス、電話番号)、モニター利用の希望(又は、お問合せの内容)を記載して送付ください。必要な応募書類などをお送りいたします。 |
| 選定課題数 | 若干数を予定。 利用者モニターの選定は、秘密情報の取り扱いに留意したうえで、外部有識者を交えた審査会で決定。 |
| その他 | 技術基盤の利用に際して、実費などの負担が必要な場合があります。また、利用者モニター制度の趣旨より、コメントや情報発信について協力を求めることがあります。協力内容については事前に協議して、利用モニターに関する契約を締結する予定です。 |
利用にあたって (創薬基盤プロジェクト概要)
(1)「創薬コンサルティング機能 - まずは戦略を一緒に考えます」
創薬シーズを開発段階へと進めるにあたり、どのような課題があり、いかなる戦略で進めていくかといった計画作りが重要です。創薬コンサルティング機能では、実際に製薬企業での創薬経験を持つ専門コーディネーターが、創薬シーズについて開発担当者から話を聞き、研究戦略を一緒に考えていきます。本プロジェクトのリーダーとなる後藤俊男客員主管研究員は、日本発の免疫抑制剤(FK506)の発見、開発を主導した経験があり、創薬シーズを持つ研究者とともに一緒に創薬開発に向けて取り組んでいきます。研究戦略や創薬基盤の利用条件などの合意を経て、創薬基盤(必要に応じて外部機関も含む)を活用しながら、創薬研究の支援をしていきます(図2)。そのほか、医薬開発に関連する基礎データの取得などの要望に応えるために、医薬候補物質とタンパク質との結合様式の構造解析や、PETによる薬物動態解析なども対応します。
(2)「創薬基盤を再構築した横断的な創薬基盤プラットフォーム - 最先端の研究基盤のアクセスを容易にします」
理研の研究技術基盤は、ライフサイエンス研究で培われた独創性のある技術が結集しています。今後はさらに、創薬研究の上流から下流までを総合的に、また効果的に支援できるように、創薬基盤プラットフォームとして再構築します。今回の利用対象は、既に構築の準備状況が進んでいる技術基盤である「ケミカルバンク基盤」「インシリコスクリーニング基盤」「NMR基盤」「マウス基盤」「分子イメージング基盤」があり、創薬基盤として研究開発に活用できます。
【利用対象基盤】
- ① ケミカルバンク基盤
- 理研の天然化合物バンク「NPDepo」には、放線菌を中心とした微生物の二次代謝物のほか、天然化合物の類縁体・誘導体など、これまでに32,000種を上回る化合物を収集・保管しており、それぞれの化合物情報、化合物名、構造式、起源生物種、物性、生理活性など収録した 化合物データベース「NPEdia」を公開してきました。ケミカルバンク基盤では、この化合物ライブラリーおよび化合物情報を提供するほか、標的タンパク質と相互作用する化合物を高速で探し出すことができる、理研独自の 化合物アレイスクリーニング技術※6も利用可能です。この技術の利用により、希少な天然化合物についても、低コストでスクリーニングをすることができます。
- ② インシリコスクリーニング基盤
- 理研が、独自に構築したコンピュータシステムMDGRAPE-3は、分子動力学シミュレーションにより、標的タンパク質に対して1週間に500個~数千個の化合物を計算することができます。インシリコスクリーニング基盤ではこの能力を活用して、タンパク質-薬剤複合体形成を予測する「分子ドッキングシミュレーション」と、化合物の結合親和性を高い精度で明らかにすることができる「分子動力学シミュレーション」を組み合わせたスクリーニングを展開します。この2つのシミュレーションを組み合わせたスクリーニング技術を活用し、実際に細胞やタンパク質を使うWET系の実験結果に迫る正確性を目指しています。さらに、電子化合物ライブラリーの整備、タンパク質立体構造解析技術やWET系のスクリーニング技術を組み合わせることにより、より一層強力なインシリコスクリーニング環境を実現します。
- ③ NMR基盤
- NMRは、タンパク質と化合物の相互作用を生理的条件に近い環境で解析することができる技術です。原子レベルでの相互作用情報や立体構造情報など、ほかの解析技術では得ることが難しい情報が得られ、化合物がタンパク質のどの部位に結合しているかなどを知ることができるため、化合物の構造を最適化するうえで力を発揮します。また、弱い相互作用についても解析が可能なため、開発の初期段階での候補化合物の評価にも有効です。NMR基盤に備えた「NMR立体構造解析パイプライン」では、標的タンパク質の遺伝子を基にして、発現系の構築、タンパク質の大量精製、NMRデータの測定、さらに立体構造解析までを統合的に実施する体制を構築しています。遺伝子を利用したタンパク質の調製も含めて対応できるので、構造情報に基づく創薬研究を効率的に進めることができます。
- ④ マウス基盤
- 特定の疾患を呈するモデル動物は、疾患メカニズムの解析に役立つだけでなく、新薬候補の効果を評価する強力なツールとなります。理研では、疾患モデルマウスの開発を進め、現在、疾患の原因となるDNA変異まで同定できている62種のヒト疾患モデルマウスを保有しています。マウス基盤では、これらのリソースを有効活用するために、国際標準化された 表現型データベース※7に情報を掲載しています。さらに、 マウス表現型解析システム※8では、マウス解析のスペシャリストによる400以上の評価項目の解析技術の提供、医薬品や候補化合物の薬理効果の評価結果の提供など、最先端の非臨床試験環境を実現しています。
- ⑤ 分子イメージング基盤
- 分子イメージング基盤では、非破壊的な生体観察システムとして注目されるポジトロン断層法(PET)の性能を高め、世界最高レベルの化合物検出技術を実現しています。これまでのPETでは、大きさが3.0~4.0mmの細胞などが検出の限界でした。しかし、理研は世界最高レベルの1.0~1.5mmという空間分解能を達成し、マウスなど器官の小さなモデル生物で、より正確なデータが取得できると期待できます。PETでは、検出する化合物を放射性同位体で標識する必要がありますが、標識による化合物の特性に影響を与えないように、約5分という短時間で[11C]を候補化合物に導入する系を確立しました。最適な標識部位を可視化することで、生体内での薬物動態を的確に評価できるシステムとなります。この標識化した化合物の製造方法は、 マイクロドージング試験※9にも利用でき、安全性の高い医薬開発に貢献します。
お問い合わせ先
独立行政法人理化学研究所 研究プライオリティー会議 創薬基盤プロジェクト担当
研究政策企画員 大須賀 壮(おおすが そう)
新保 斉 (しんぼ いつき)
Tel: 048-467-9758 / Fax: 048-462-4600
pharma-support [at] riken.jp
※[at]は@に置き換えてください。
報道担当
独立行政法人理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.
- 化合物アレイ
- スライドガラス上に多数の化合物を固定化したスクリーニング用チップ。
- 2.
- DRY/WET
- DRYとはコンピュータ上で行う実験(シュミレーション)を伴う研究形態のこと。WETとは試験管などの器具や溶媒を用いた実際の実験を伴う研究形態のこと。
- 3.
- NMR
- 核磁気共鳴法(Nuclear Magnetic Resonance:NMR)。化学分析機器としては最もシェアの多い分析手法のうちの1つであり、試料の前処理が不要、不溶試料でも計測が可能といった利点があるものの、低感度という欠点も同時に有する。化学構造に応じて、磁場中での共鳴吸収が異なることを利用した分析法で、代謝混合物の構造の違いを反映して、シグナルが分離する。
- 4.
- ポジトロン断層法(PET)
- ポジトロン断層撮影法(Positron Emission Tomography:PET)。陽電子(ポジトロン)が消滅するときに放出するガンマ線を検出して、断層撮影を行う方法。陽電子崩壊する核種で標識された化合物をサンプルに投与する必要がある。
- 5.
- 創薬分野の研究開発を支援する拠点
- 欧米のさまざまな公的研究機関では、研究・実験施設、化合物の最適化やスクリーニング、臨床技術、膨大な化合物データを収容したライブラリーなどの創薬基盤を民間の創薬関連企業や学術機関に広く提供し、創薬の実現・加速化に貢献している。代表的なものとしては、米国のブロード研究所、ダナ・ファーバー/ハーバード癌研究所、アメリカ国立衛生研究所の分子ライブラリー&分子イメージング、ドイツのマックスプランク研究所の創薬開発センターが挙げられる。
- 6.
- 化合物アレイスクリーニング技術
- スライドガラス上に多数の化合物を固定化したスクリーニング用チップを用いるスクリーニング技術。
- 7.
- 表現型データベース
- 20,000個体のマウスについて、それぞれ200項目にのぼる表現型変異情報を蓄積した データベースシステム(英語)。
- 8.
- マウス表現型解析システム
- 可視的形態形質、血液・尿。成分から生理的形質、非侵襲的内部形態まで網羅的な解析システム。
- 9.
- マイクロドージング試験
- マイクロドージング試験とは、効率的な医薬品開発を促進するために、超微量(予想薬効量の1/100以下、かつ100μg以下)の標識化合物をヒトに早期に投与して、最適な薬物動態を示す開発候補化合物を選択する試験。ポジトロン核種や炭素14などでラベルした試験薬の微少量を投与し生体内の薬物動態などを測定することにより、第一相試験の開始前に開発候補化合物の評価を行う臨床試験。
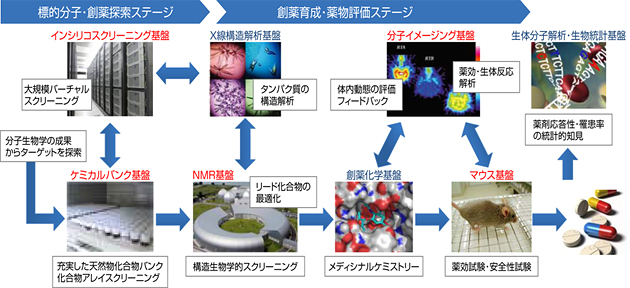
図1 理研が確立を目指す創薬基盤プラットフォーム
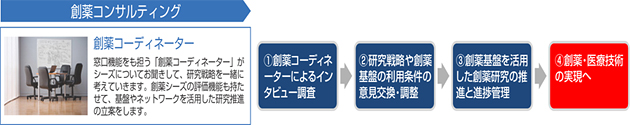
図2 創薬基盤プロジェクトの利用手順
