2013年1月4日
独立行政法人理化学研究所
独立行政法人 科学技術振興機構
がん細胞を殺すT細胞をiPS細胞化し若く元気なT細胞に再生
-がんの免疫療法を革新する可能性-
ポイント
- がん患者に由来するキラーT細胞からiPS細胞を作製
- iPS細胞から分化誘導したT細胞のほぼ全てが元のがん抗原と反応
- 現行のがん免疫療法が直面している問題の解決へ
要旨
理化学研究所(野依良治理事長)は、がん細胞を特異的に殺すT細胞からiPS細胞を作製するとともに、そのiPS細胞から同じがん抗原と反応するT細胞を大量に分化誘導することに成功しました。これは、理研免疫・アレルギー科学総合研究センター(谷口克センター長)免疫発生研究チームの河本宏チームリーダー、免疫器官形成研究グループの古関明彦グループディレクター、ラウール ビスカルド特別研究員らの研究グループの成果です。
がん患者の体内には、がんを殺す能力を持つキラーT細胞[1]が存在します。しかし、T細胞の多くはがん細胞によって無力化されていて、働ける状態のT細胞はごく少数です。現行のがん免疫療法[2]では、その少数のT細胞を刺激して働かせるという戦略を取っています。しかし、働けるT細胞の数が少ないうえに、刺激を受けた後のT細胞の寿命が短く効果が長続きしないという問題があり、これががんの免疫療法の効果を薄めています。本研究では、iPS細胞作製技術とT細胞の分化誘導技術を組み合わせることにより、そうした状況を打破しようと試みました。
研究グループは、ヒト悪性黒色腫[3]細胞に特有のがん抗原であるMART-1抗原と反応できるT細胞に山中因子[4]などを作用させてiPS細胞を作製しました。T細胞は、さまざまな抗原に対して特異的に反応できますが、どの抗原に反応するかはT細胞レセプター[5]によって決まります。T細胞レセプターの遺伝子は、ゲノム中のレセプター遺伝子の断片を切り貼りすることによってつくられたものです。T細胞からiPS細胞を作製すると、切り貼りしてつくられた遺伝子の情報も引き継がれるので、そのようなiPS細胞からT細胞を分化誘導すると、元のT細胞と同じ反応性のT細胞レセプターを発現するようになると考えました。実際に、研究グループがiPS細胞からT細胞を分化誘導したところ、生成したT細胞のほぼ全てが、元のがん抗原と反応できるT細胞レセプターを発現していました。また、これらのT細胞は元のがん抗原に反応することが確認できました。この成果は、がん免疫療法が直面するT細胞の数の少なさ、T細胞の寿命の短さという問題点を、一挙に解決できる可能性を示しています。
本研究成果は、科学技術振興機構の戦略的創造研究推進事業 チーム型研究(CREST)「ヒトiPS細胞の分化能と腫瘍化傾向を反映するマーカー遺伝子群の探索」(研究代表者:古関明彦)の助成を受けており、米国の科学雑誌『Cell Stem Cell』2013年1月4日号(オンライン版は1月3日:日本時間1月4日)に掲載されます。
背景
今回の研究では、がん抗原に反応するT細胞からiPS細胞を作製し、そのiPS細胞から元のがん抗原に反応できるT細胞を分化誘導することを目的としました(図1)。
がん患者で何が起こっているかを見て行きましょう。成熟したT細胞の中で、抗原から刺激を受ける前の段階のT細胞をナイーブT細胞と呼びますが、これは、いろいろな抗原に対して応答できる反応性をもった細胞の集団です。その中で、がん細胞に反応できるT細胞は、がん抗原の刺激によって増殖し、働くことができるエフェクターT細胞になります。しかし、がん細胞にはエフェクターT細胞を抑制し、無力化する性質があり、がん細胞に対する免疫反応が起こりにくくなっています(図2)。
現行のがん免疫療法は、がん患者の体内にあるわずかな働けるエフェクターT細胞を患者の体内、あるいは生体外で成熟T細胞を刺激して、さらに働かせようとするものです。ここで問題になるのは、刺激されて活性化されたエフェクターT細胞の寿命が短く、せいぜい1~2週間しか生きないとされている点です(図3)。このため、がんに対する免疫反応が持続せず、現行の免疫療法の最大の課題となっています。
これを解決するために、研究グループはiPS細胞技術を利用しようと考えました。この戦略を理解するには、T細胞の反応の仕組みを理解する必要があります。
T細胞は、T細胞レセプターを用いて抗原を認識し反応します(図4)。このT細胞レセプターには、いろいろな反応性をもつものがあります。T細胞レセプター遺伝子は断片化した状態でゲノム中に存在しています(図5)。T細胞は胸腺[6]という組織でつくられる過程の中で、いくつかの断片を組み合わせて遺伝子の切り貼りを行い、T細胞ごとに異なるレセプター遺伝子がつくられます。これは、遺伝子再構成[7]と呼ばれる現象です。従って、T細胞は細胞ごとに異なる構造のT細胞レセプターを発現していることになります。
そのようなT細胞のうちの1つからiPS細胞をつくると、再構成された遺伝子の情報が受け継がれます(図6)。そのiPS細胞からT細胞を分化誘導すると、元のT細胞と同じ抗原と反応するT細胞ばかりになります。この原理が実際に働くことは、マウスのNKT細胞[8]からiPS細胞を作製した研究で確認されています(Watarai H et al, J Clin Invest 120:2610, 2010*)。
さて、本研究の戦略を解説します。体細胞から作製したiPS細胞を材料としてT細胞をつくると、多様な遺伝子再構成が起き、さまざまな反応性をもつT細胞群になってしまうため、その中のごく一部のT細胞しかがん細胞を攻撃できません(図7上段)。
しかし、がん細胞を攻撃できるT細胞をあらかじめ取り出しておいて、そのT細胞からiPS細胞を作製し、そのiPS細胞を材料としてT細胞を分化誘導させると、全てのT細胞に元のT細胞と同じ反応性を持たせることが可能です(図7下段)。つまり、生成した全てのT細胞ががん細胞を攻撃できることになります。
こうした戦略により、がん細胞を攻撃できるT細胞を大量につくることができれば、前述のようながんに反応できるT細胞の少なさや寿命の短さという問題を克服できると考えました。
*2010年6月2日プレスリリース参照
研究手法と成果
1)ヒト悪性黒色腫特有の抗原に反応するキラーT細胞からiPS細胞を作製
研究グループが材料として用いた細胞は、ヒト悪性黒色腫というがんに特有のMART-1という抗原に反応できるキラーT細胞です。これは、アメリカ国立衛生研究所(NIH)でヒト悪性黒色腫の患者から分離され、培養されていた細胞で(JKF6細胞、Yang S et al, PLoS One 6, e22560)、T細胞マーカーであるCD3という分子と、キラーT細胞マーカーであるCD8という分子を発現しています。この細胞に、山中因子(Oct3/4、Klf4、Sox2、c-Myc)の遺伝子を導入し、またiPS細胞作製の効率化を図るためにSV40[9]という因子(Park IH, Nature 451:141, 2008)も用いて、iPS細胞を作製しました(図8)。これをMART-1-iPS細胞と名付けます。
MART-1-iPS細胞が十分な機能をもった質のよいiPS細胞であるかどうかは、いろいろな方法で検証しました。例えばコロニーの形状、遺伝子発現のパターン、染色体異常の有無、いろいろな組織への分化能などです。その中で最も重要なポイントである「いろいろな組織への分化能」を調べた結果を示します。MART-1-iPS細胞をヌードマウス[10]の皮下に注入し、4週間後に生成した細胞を組織学的に解析したところ、外胚葉、中胚葉、内胚葉系のいろいろな組織へ分化していることが確かめられました(図9)。すなわち、iPS細胞とみなせる細胞であることが実証されました。
2)MART-1-iPS細胞からの未成熟T細胞の分化誘導
次にMART-1-iPS細胞からT細胞を分化誘導しました。方法は、すでに報告されている手順(Timmermans F et al, 182:6879, 2009)を基に、独自の改変を少し加えました。iPS細胞をあるフィーダー細胞[11](OP9細胞)と共培養した後、培養13日目で別なフィーダー細胞(OP9/DLL1細胞)との共培養に切り替えます(図10)。その後培養を継続すると、培養35日目にはCD8(キラーT細胞マーカー)とCD4というヘルパーT細胞の分化マーカーを共に発現する細胞が出現します。これは、成熟細胞の一歩手前の未成熟なT細胞に該当します。この時点で、未成熟のT細胞が発現しているT細胞レセプターの性質を調べました。T細胞レセプターがMART-1抗原に結合できるかどうかは、MART-1テトラマー[12]という試薬を用いて染色することで調べます。結果は、生成したT細胞の多くがMART-1抗原と結合できるものでした。
3)未成熟T細胞から成熟T細胞への分化誘導
フィーダー細胞との共培養では、未成熟T細胞の段階で分化が停止してしまいます。この段階で、T細胞レセプターはすでに発現していますが、機能的には未成熟なのです。それ以上に分化させる方法は知られていませんでした。そこで、独自に開発した方法で、さらなる分化誘導を試みました。T細胞が発現しているCD3という分子に対する抗体を加えることにより、T細胞レセプターに刺激を与えるという方法です(図11)。この方法を用いた結果、抗体添加の6日後に、元のキラーT細胞と同じCD8を発現する細胞を大量に得ることができました。また、このCD8陽性細胞は、ほぼ全てがMART-1抗原を認識できるタイプ、すなわち元のキラーT細胞と同じ反応性をもつT細胞レセプターを発現していました。
4)MART-1-iPS細胞から作製した成熟T細胞の反応性
このT細胞レセプターがMART-1抗原に結合できることはテトラマー染色で検証できましたが、さらにMART-1抗原で刺激して活性化することができるかどうかをテストしました(図12)。生成したキラーT細胞と標的細胞(EBウイルスでがん化したB細胞)を混ぜただけではT細胞は活性化されないのに、MART-1抗原を添加した時には抗原の刺激を受けてガンマインターフェロン(IFNγ)を産生しました。IFNγはキラーT細胞がよく産生するサイトカインという情報伝達物質の一種で、抗腫瘍活性を持っています。この実験により、MART-1-iPS細胞から分化誘導されたT細胞がMART-1抗原に反応するT細胞であることが確認できました。
今後の期待
1)がん免疫療法の直面していた壁を突き破る可能性がある
がん免疫療法については、現在もいろいろな試みがなされています。そのほとんどはすでに体の中にあるくたびれたエフェクターT細胞を何とか励まそうというものです。得られる細胞数や寿命には限りがありました。今回の研究グループのアプローチは、体外で未成熟なT細胞から新たにエフェクターT細胞をつくろうというものであり、既存の方法と全く異なっています。実際、本研究で生成した成熟細胞は主にエフェクターT細胞にあたると考えられ、すなわち寿命自体は、それほど長くないと思われます。しかし、iPS細胞からの分化誘導を繰り返せば、大量の細胞を継続的に得ることができます。従って、現行の方法が直面している壁の突破口になる可能性があります。
なお、本研究では、試験官内でエフェクターT細胞にまで分化誘導しましたが、こうしたエフェクターT細胞をつくって生体に戻すということを、必ずしも最終的なゴールとしている訳ではありません。理想的なゴールとして想定しているのは、「胸腺で分化を始める直前、すなわち前駆細胞の段階まで生体外で分化誘導して、生体に戻す」ことです。注入された前駆細胞は、患者の胸腺に移住して、T細胞に分化するはずだと考えています。こうすれば、本来の胸腺環境で分化が起こるので、体外で分化誘導した場合と違ってナイーブT細胞が大量に胸腺でつくられるはずです。そこへがん抗原を用いて適切に免疫することで、過去の抗原情報を記憶できるメモリーT細胞を誘導することもでき、持続的な抗腫瘍免疫が期待できると考えています。
2)iPS細胞作製技術の応用範囲を大幅に拡げた
iPS細胞の臨床応用は、薬剤のスクリーニングや毒性試験などの応用も考えられていますが、第一義的には欠損した組織の再生による補完です。しかし、その対象となる疾患は、そう多くはありません。
本研究により、リンパ球の特性を活かしたiPS細胞の応用によって、がんという疾患を対象とする可能性が出てきました。実用化できれば、iPS細胞技術の恩恵を受けることができる患者の数は、一気に数十倍に広がる可能性があります。
3)iPS細胞バンクも利用できる
本研究では、原則として免疫の拒絶反応が起きないように、患者本人すなわち自己のiPS細胞から分化誘導したT細胞を利用することを想定しています。特に、前駆細胞を胸腺に移住させて持続的な抗がん免疫をつくりだすという方式では、自己細胞を使う必要があります。
しかし、生体外で分化誘導したキラーT細胞を繰り返して患者に投与する場合は、T細胞から作製したiPS細胞のバンクを確立して、それらを利用することも可能です。その場合、移植後に拒絶されないようにするためには、あらかじめいろいろな種類のT-iPS細胞を作製しておく必要があります。品質保障という点では、むしろT-iPS細胞バンクを用いる方が、実現性が高いと考えます。
発表者
理化学研究所
免疫・アレルギー科学総合研究センター 免疫発生研究チーム
チームリーダー 河本 宏(かわもと ひろし)
(京都大学 再生医科学研究所 再生免疫学分野 教授)
お問い合わせ先
横浜研究推進部 企画課
Tel: 045-503-9117 / Fax: 045-503-9113
報道担当
独立行政法人理化学研究所 広報室 報道担当
Tel:048-467-9272 / Fax:048-462-4715
独立行政法人科学技術振興機構 広報課
Tel: 03-5214-8404 / Fax: 03-5214-8432
JSTの事業に関すること
独立行政法人科学技術振興機構 戦略研究推進部
Tel: 03-3512-3524 / Fax: 03-3222-2064
補足説明
- 1.キラーT細胞
ウイルスに感染した細胞やがん細胞を殺すことのできるT細胞。 - 2.がん免疫療法
樹状細胞、T細胞などの免疫細胞を用いてがん細胞を殺すという治療法。抗原を提示する樹状細胞を取り出してがん抗原を取り込ませてから体に戻す、あるいはエフェクターT細胞を取り出してサイトカインなどを加えて活性化してから体に戻す、などの方法が用いられている。がん抗原をワクチンとして投与する方法も行われている。 - 3.悪性黒色腫
皮膚や粘膜中に存在するメラノサイト(メラニン色素を産生する細胞)に由来するがん。メラノサイトは、免疫を刺激しやすい性質を有しているので、よく免疫療法の治療対象とされる。 - 4.山中因子
分化した体細胞を初期化してiPS細胞を作製する時に用いられる因子で、Oct3/4、Klf4、Sox2、c-Mycの4因子を指す。山中伸弥(京都大学教授)らが同定したので、山中因子と呼ばれる。これらの遺伝子を体細胞に導入して発現させ、一定期間培養することにより、その細胞をiPS細胞に誘導することができる。山中はこの研究成果が評価され2012年にノーベル医学生理学賞を受賞した。 - 5.T細胞レセプター
T細胞が抗原を認識するために用いるT細胞の表面に存在する受容体。受容体とは外界や外部からの何らかの刺激を受け取り、情報として利用できるように変換する仕組みを持った構造のこと。 - 6.胸腺
T細胞がつくられる臓器である。心臓の上に位置している。骨髄から移住してきた前駆細胞が、胸腺の中で分化、成熟する。 - 7.遺伝子再構成
T細胞レセプター遺伝子やB細胞レセプター(抗体)遺伝子で起こる遺伝子の切り貼りのこと。これらのレセプター遺伝子は、もともとは断片化したものが多数ゲノム上に存在しているが、T細胞やB細胞が分化する過程で、断片同士がランダムにつなぎ合わされる。この再構成により個々の細胞が異なる形状のレセプター分子を出せるようになる。1976年に利根川進(理研脳科学総合研究センター長)が発見した現象で、利根川はこれにより1987年にノーベル医学生理学賞を受賞した。 - 8.NKT細胞
T細胞の一種で、ナチュラルキラー(NK)細胞とよく似た分子を出しているのでNKT細胞と呼ばれる。ふつうのT細胞はタンパク質の断片を抗原として認識するが、NKT細胞は糖脂質分子を抗原として認識する。NKT細胞の発見と機能の解明には谷口克(理研免疫・アレルギー科学総合研究センター長)が大きく貢献している。抗腫瘍作用を有するため、この細胞を活性化させることを利用したがん治療が千葉大などで進められている。 - 9.SV40
SV40はサルから分離された腫瘍ウイルスのことであるが、ここではSV40の主要な構成成分であるラージT抗原というタンパク質分子のことを指す。この分子は細胞をがん化する働きを持つが、本研究ではiPS細胞の作製の効率を上げるために一時的に細胞質内に導入しただけであり、SV40遺伝子自体は細胞の中には取り込まれていない。 - 10.ヌードマウス
先天的に胸腺を欠くマウス。胸腺を欠損するためにT細胞がつくられず、免疫不全を呈する。他の動物種の細胞を拒絶する力も弱いので、ヒトの組織やがん細胞の移植実験によく用いられる。 - 11.フィーダー細胞
ある細胞を維持したり分化させたりする時、その維持や分化を支持する細胞を同時に培養することが多い。そういう支持細胞を、フィーダー細胞という。通常は間葉系細胞を一層に敷き詰めたものが使われる。今回の研究では、OP9細胞とOP9/DLL1細胞を用いた。 - 12.MART-1テトラマー
MART-1抗原と結合できるT細胞レセプターを特異的に染色するための試薬。抗原分子と抗原提示分子のセットが4つ含まれているので、テトラマーという。フローサイトメーターで検出できるように、蛍光色素でラベルされている。
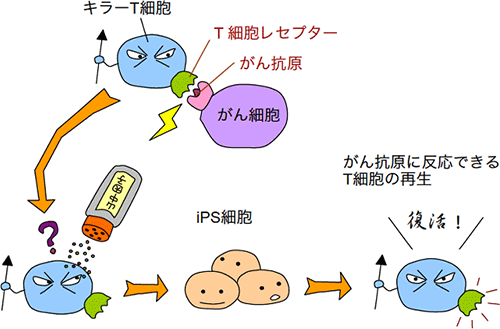
図1 研究内容全体を示す模式図
本研究では、がん細胞を攻撃できるキラーT細胞からiPS細胞を作製し、そのiPS細胞からキラーT細胞を再生するという実験を行った。
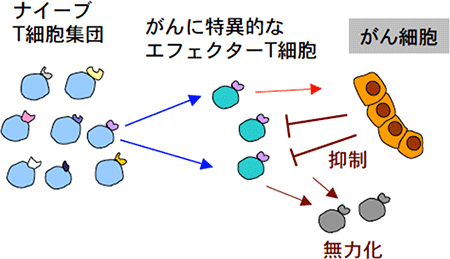
図2 がん患者にみられるT細胞の無力化
がん患者では、がん細胞を攻撃することができるエフェクターT細胞は生成するが、その多くは無力な状態になってしまっている。
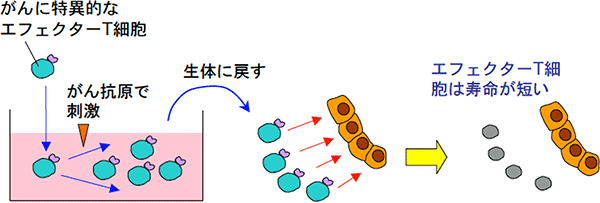
図3 現行のがん免疫療法が直面する問題点
がんに対する反応性のあるエフェクターT細胞をがん抗原で刺激し活性化させても、得られる細胞数や寿命は限られており、抗がん効果は限定的である。
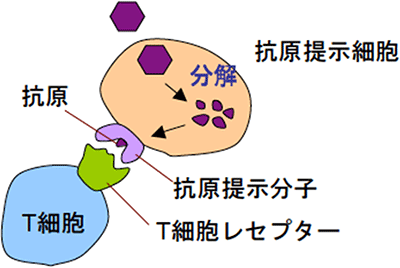
図4 T細胞はT細胞レセプターを用いて抗原を認識する
T細胞レセプターは、抗原提示細胞の上に乗せられた形で提示されている抗原提示分子に結合することにより、抗原を認識する。
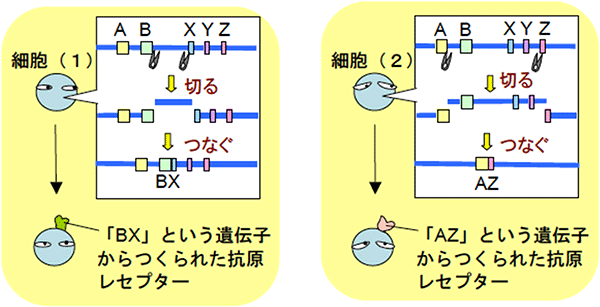
図5 細胞ごとに異なるレセプターをつくるメカニズム
それぞれの細胞のゲノム上にはT細胞レセプター遺伝子の断片(図中のA、B、X、Y、Z)が存在する。T細胞レセプター遺伝子は、切り貼りによりそれぞれの細胞ごとに異なる断片をつなぎ合わせてつくられる。これは、遺伝子再構成と呼ばれる現象である。これにより、T細胞は細胞ごとに異なる構造のT細胞レセプターを発現するようになる。
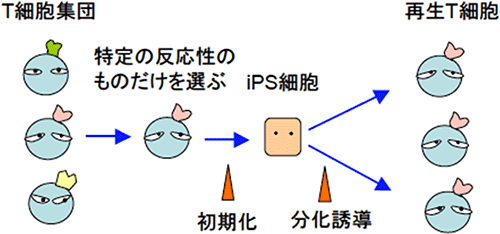
図6 T細胞からiPS細胞を作製し、そのiPS細胞からT細胞を分化誘導する様子
T細胞においては、そのレセプター遺伝子は、細胞ごとに異なっている。従って、成熟T細胞からiPS細胞を作製すると、その遺伝子の情報が受け継がれる。そのiPS細胞からT細胞を分化誘導すると、元のT細胞と同じT細胞レセプターを発現するようになる。
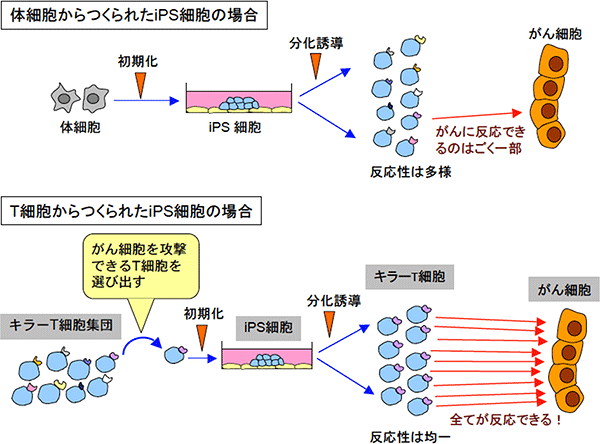
図7 T細胞からiPS細胞を作製する理由
体細胞からつくった一般的なiPS細胞からキラーT細胞を作製すると、正常なT細胞の分化過程と同じように遺伝子再構成によって多様性がつくられ、ごく一部のキラーT細胞しかがん細胞を攻撃できなくなる。一方、がん細胞を攻撃できるキラーT細胞からiPS細胞を作製すると、同じ反応性をもつキラーT細胞を大量に分化誘導できる。
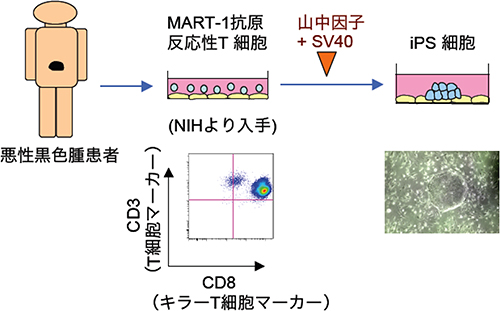
図8 がん抗原に反応するT細胞からのiPS細胞の作製
ヒト悪性黒色腫の患者から分離されたキラーT細胞を材料にしてiPS細胞を作製した。このキラーT細胞はヒト悪性黒色腫というがんに特有のMART-1抗原に反応する。T細胞マーカーであるCD3という分子と、キラーT細胞マーカーであるCD8を出している。この細胞に、山中因子(Oct3/4、Klf4、Sox2、c-Myc)とSV40の遺伝子を導入し、iPS細胞を作製した。遺伝子導入にはセンダイウイルスを用いた。センダイウイルスで導入された遺伝子は、ゲノムの中に挿入されないので、T細胞のゲノムを傷つけることはない。
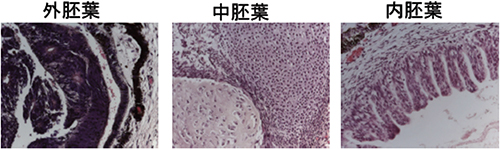
図9 MART-1-iPS細胞は三種類の胚葉全てに分化した
MART-1-iPS細胞の全能性を調べるために、ヌードマウスの皮下に注射をして、4週間後に注射部位に生じた組織を調べた。三種類の胚葉(外胚葉、中胚葉、内胚葉)の組織全てに分化する能力を持つことが示され,iPS細胞としての要件を満たしていた。
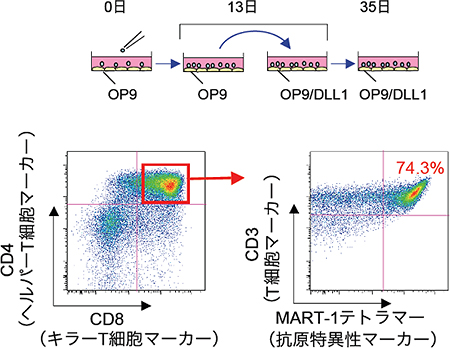
図10 MART-1-iPS細胞から未成熟T細胞を作製した
iPS細胞をフィーダー細胞(OP9細胞)と共培養した後、培養13日目で別のフィーダー細胞(OP9/DLL1細胞)との共培養に切り替え、培養を継続する。MART-1抗原に結合できるT細胞レセプターを発現している細胞は、MART-1テトラマーで染色することができる。培養35日目には、CD4とCD8をどちらも発現する未成熟T細胞が生成した。CD4はヘルパーT細胞、CD8はキラーT細胞のマーカーであるが、未成熟段階ではどちらも発現している。この中の多くがMART-1抗原に結合できるT細胞レセプターを出していた。
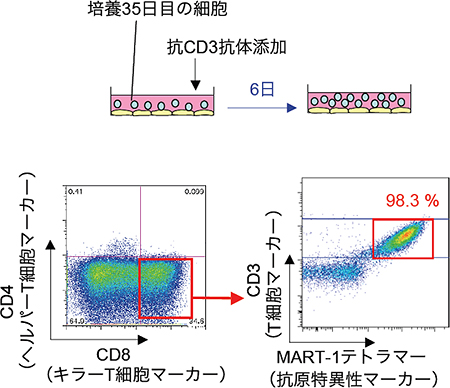
図11 未成熟T細胞から成熟T細胞の分化誘導
培養35日目前後に生成した未成熟T細胞に、T細胞が発現しているCD3に対する抗体を加えることにより、さらに成熟を誘導することに成功した。誘導6日目にCD4陰性CD8陽性の細胞が生成した。これは成熟キラーT細胞と同じ発現プロファイルある。その中で、CD3を発現する細胞のほぼ全てがMART-1抗原に結合できるT細胞レセプターを出していた。
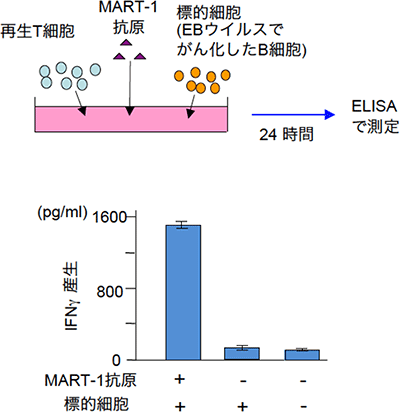
図12 MART-1-iPS細胞から生成した成熟T細胞はMART-1抗原への反応性を示した
再生したT細胞に標的細胞(EBウイルスでがん化したB細胞)およびMART-1抗原を添加し、24時間培養した。24時間後に培養上清中のガンマインターフェロン(IFNγ)をELISA法で測定した。MART-1-iPS細胞から分化誘導されたT細胞がMART-1抗原に反応するT細胞であることが確認された。
