2016年4月2日
理化学研究所
(株)オーガンテクノロジーズ
北里大学
マウスiPS細胞から皮膚器官系の再生に成功
-難治性皮膚、脱毛疾患への応用に期待-
要旨
理化学研究所(理研)多細胞システム形成研究センター器官誘導研究チームの辻孝チームリーダー(東京理科大学客員教授、北里大学医学部客員教授、東京歯科大学客員教授)、株式会社オーガンテクノロジーズの杉村泰宏社長、北里大学医学部の武田啓主任教授、佐藤明男特任教授、東北大学大学院歯学研究科の江草宏教授らの共同研究グループ※は、マウスiPS細胞(人工多能性幹細胞)[1]から、毛包や皮脂腺などの皮膚付属器を持つ「皮膚器官系」を再生する技術を開発しました。
皮膚は生体を防御するほか、汗の排せつなどの機能があり、生体の恒常性維持に重要な役割を担っています。皮膚には、毛包や皮脂腺、汗腺など複数の皮膚付属器が存在し、上皮層や真皮層、皮下脂肪層を持っており、皮膚器官系として3次元的に複雑な構造をしています。皮膚に関わる疾患は、外傷や熱傷、先天性乏毛症、脱毛症、分泌腺異常など数多く知られています。しかし、皮膚器官系が複雑なために皮膚の完全な再生はいまだに実現していません。共同研究グループは、皮膚疾患に対する新たな再生治療法を確立するため、iPS細胞から皮膚器官系を形成する技術の開発を目指しました。
共同研究グループは、マウスiPS細胞から胚葉体(EB)[2]と呼ばれる凝集塊を形成させ、この凝集塊を複数個合わせてコラーゲンゲルに埋め込み、マウス生体へ移植してさまざまの上皮組織を形成する「Clustering-Dependent embryoid Body:CDB法」を開発しました。この移植物内部には、上皮層や真皮層、皮下脂肪層、毛包や皮脂腺を持つ天然皮膚と同様の皮膚器官系が再生されていることを明らかにしました。さらに、このiPS細胞由来皮膚器官系から毛包を10~20本含む「再生皮膚器官系ユニット」を分離し、別のマウス皮下へ移植すると、移植組織はがん化することなく生着し、神経や立毛筋などの周囲組織と接続して、機能的な毛包を再生することも示しました。
開発した手法をヒトに応用するには、生体内移植を経ずに生体外で皮膚器官系を再生する手法へと発展させることが必要です。本研究は将来、皮膚の外傷や熱傷の完全な再生に加え、先天性乏毛症や深刻な脱毛症、皮膚付属器に関する疾患の治癒につながると期待できます。
本研究成果は米国のオンライン科学雑誌『Science Advances』(4月1日付:日本時間4月2日)に掲載されます。
※共同研究グループ
理化学研究所 多細胞システム形成研究センター 器官誘導研究チーム
チームリーダー 辻 孝(つじ たかし)(東京理科大学 総合研究機構 客員教授、北里大学 医学部 客員教授、東京歯科大学、客員教授)
株式会社オーガンテクノロジーズ
代表取締役社長 杉村 泰宏(すぎむら やすひろ)
研究員 小川 美帆(おがわ みほ)(理研 多細胞システム形成研究センター 器官誘導研究チーム 客員研究員)
北里大学 医学部
形成外科・美容外科学
主任教授 武田 啓(たけだ あきら)
寄附講座 再生医療形成外科学(オーガンテクノロジーズ)
特任教授 佐藤 明男(さとう あきお)
東北大学大学院 歯学研究科 口腔修復学講座 分子・再生補綴学分野
教授 江草 宏(えぐさ ひろし)
背景
皮膚は、上皮層と真皮層、皮下脂肪層の3層からなり、個体の体表面全体を覆っています。皮膚には、皮膚付属器として毛包や皮脂腺、汗腺などの複数の器官が一定の規則性を持って配置されており、体の中で最も大きく、複雑な器官系です。皮膚付属器は、それぞれ神経支配や生理活性物質を介して機能しており、生体の恒常性の維持に重要な役割を担っています。毛包は、毛幹を萌出することによって、体表の保護や保温、皮膚創傷治癒時の細胞の供給源としての役割を担っています。一方、皮脂腺は皮脂の分泌による生体の保護、汗腺は水分供給と排せつを調節していることが知られています(図1)。
皮膚は、個体の恒常性に重要であり、皮膚付属器を持った構造の複雑性のために、さまざまな疾患に関係しています。その例として、外傷や熱傷、免疫疾患をはじめ、毛包における脱毛症、皮脂腺での皮脂の分泌異常や感染症などが挙げられます。これらの疾患は薬物や外科的治療で治癒可能なものも多くありますが、重症の熱傷や外傷、先天性乏毛症、汎発性脱毛症など難治性の先天性皮膚疾患の治療には、再生医療の適用が期待されています。例えば、重度熱傷に対する治療として再生上皮細胞シートが用いられています。しかし、皮膚器官系の完全な再生は、その複雑さのためにいまだに実現していません。
ほぼすべての器官は、胎児期の上皮・間葉相互作用[3]によって誘導される器官原基から発生します。これまでに辻孝博士らは、胎児期に存在する器官誘導能のある組織幹細胞を用いて、3次元的な細胞操作技術である「器官原基法」を開発注1)し、歯注2)や毛包注3)、唾液腺注4)、涙腺注5)の器官再生が可能であることを実証してきました。しかし、器官再生の細胞シーズは毛包を除いて胎児期にしか存在せず、ES細胞(胚性幹細胞)[4]やiPS細胞からの誘導が期待されています。
そこで共同研究グループは、これまで課題であった重篤な皮膚疾患に対する新たな再生治療法の確立を目指し、iPS細胞から毛包や皮脂腺、汗腺を持つ天然皮膚と同様な皮膚器官系を再生する技術の開発を目指しました。
注1)K. Nakao, R. Morita, Y. Saji, K. Ishida, Y. Tomita, M. Ogawa, M. Saitoh, Y. Tomooka, and T. Tsuji, “The development of a bioengineered organ germ method,” Nature methods 4(3), 227-30 (2007).
注2)E. Ikeda, R. Morita, K. Nakao, K. Ishida, T. Nakamura, T. Takano-Yamamoto, M. Ogawa, M. Mizuno, S. Kasugai, and T. Tsuji,
”Fully functional bioengineered tooth replacement as an organ replacement therapy,” Proc Natl Acad Sci USA. 106(32), 13475-80 (2009).
注3)KE. Toyoshima, K. Asakawa, N. Ishibashi, H. Toki, M. Ogawa, T. Hasegawa, T. Irié, T. Tachikawa, A. Sato, A. Takeda, and T. Tsuji. ”Fully functional hair follicle regeneration through the rearrangement of stem cells and their niches,”Nature Communications. 3, 784 (2012).
注4)M. Ogawa, M. Oshima, A. Imamura, Y. Sekine, K. Ishida, K. Yamashita, K. Nakajima, M. Hirayama, T. Tachikawa, and T. Tsuji, ”Functional salivary gland regeneration by transplantation of a bioengineered organ germ,”Nature Communications. 4, 2498 (2013).
注5)M. Hirayama, M. Ogawa, M. Oshima, Y. Sekine, K. Ishida, K. Yamashita, Ikeda K, S. Shimmura, T. Kawakita, K. Tsubota, and T. Tsuji, “Functional lacrimal gland regeneration by transplantation of a bioengineered organ germ,” Nature Communications. 4, 2497 (2013).
研究手法と成果
共同研究グループは、iPS細胞から胚葉体(EB)を誘導し、そのEBから外胚葉性上皮組織を形成する技術を開発し、「Clustering-Dependent embryoid Body:CDB法」と名付けました。この方法はiPS細胞単独移植や単一のEBを移植した場合と比較して多種類の上皮組織を形成し、その内部には皮膚付属器である毛包や皮脂腺、汗腺などを持つ皮膚器官系が形成されました。この皮膚器官系が天然皮膚と同様の組織構造を持つことを明らかにするとともに、再生した皮膚器官系を生体内に移植することにより、その生理機能を再生できることを実証しました。
1)CDB法による外胚葉性上皮組織の誘導
マウス歯肉の細胞から樹立したiPS細胞株を、1週間、低接着培養することによりEBを形成させました。このEBから外胚葉性の上皮組織を形成するため、コラーゲンゲル内に30個以上のEBを立体的に配置したものを免疫不全マウスの腎皮膜下に移植しました(図2)。
移植30日後には、移植したEBはテラトーマ[5]様の組織を形成しました。この移植物を組織学的に解析したところ、移植物は外胚葉や内胚葉性の上皮組織からなる空洞構造(嚢胞)を多数持っていました。CDB法を用いると、iPS細胞単独移植や単一のEBを移植した場合と比較して、約4倍の上皮組織からなる嚢胞を形成しました(図3)。
2)CDB法による移植物における皮膚器官系の再生
CDB法による移植物内の上皮組織をより詳しく解析すると、移植物の上皮組織の一部に、天然の皮膚と同等の組織構造が形成され、毛包や皮脂腺などの皮膚付属器を持つ皮膚器官系が再生されていることが分かりました。この皮膚器官系には、毛穴を介して毛幹が萌出している様子も観察されました(図4左および中央)。これらの結果から、iPS細胞から形成させたEBをCDB法により移植した移植物には、天然皮膚の組織と同様の構造を持つ皮膚器官系が再生されていることが明らかになりました。さらに、器官発生を制御する生理活性物質であるWnt10bによって刺激したEBを用いたCDB法では、Wnt10bで刺激しない場合と比べて、形成された移植物の毛包数が多く、より成熟していました(図4右)。この結果から、皮膚器官系の再生には、Wnt10bシグナルが効果的であることが分かりました。
3)マウスiPS細胞由来皮膚器官系の組織学的解析
移植物内に形成された再生皮膚器官系に含まれる付属器官の組織構造を詳しく解析したところ、毛包器官内に毛包上皮性幹細胞や毛乳頭細胞が正常に再生され、毛包に付随する立毛筋も適切な位置に配置されていることが分かりました(図5)。このことから、iPS細胞由来再生皮膚器官系は、天然の皮膚器官系と同等の組織構造を持つことが示されました。
4)マウスiPS細胞由来皮膚器官系の分離と移植
再生皮膚器官系が正常な機能を持つかどうかを解析するため、再生皮膚器官系から毛包を10~20本含む全層組織を1つの再生皮膚器官系ユニットとして外科的に分離し、ヌードマウスの皮下へ移植しました。その結果、移植した再生皮膚器官系は、移植されたヌードマウス(レシピエント)に生着し、少なくとも3か月にわたりがん化することはありませんでした。移植14日後には、再生毛がレシピエントの皮膚表面より萌出し、その後、天然毛と同様に成長していく様子が観察されました(図6)。
再生毛が、iPS細胞から誘導した皮膚器官系由来であることを確認するため、雄マウス(性染色体:XY)由来の再生皮膚器官系ユニットを、雌マウス(性染色体:XX)に移植してY-染色体 in situハイブリダイゼーション[6]により皮膚組織の由来を解析しました。雄マウスの再生皮膚器官系ユニットを移植した部位では、Y染色体を持つ表皮や真皮、皮下脂肪、毛包や皮脂腺の細胞の局在が観察され、Y染色体を持たない雌マウスであるレシピエントの上皮組織内に生着していることからiPS細胞に由来することが確認されました(図7)。
また、毛包には立毛筋が接続し、寒さや緊張により収縮することが知られています。立毛筋が正常に機能、収縮するためには立毛筋と神経の接続が必要です。再生皮膚器官系の毛包には立毛筋が接続しており、さらに再生皮膚器官系を移植した部位では、立毛筋と神経組織が接続していることが分かりました(図8)。
これらのことから、再生皮膚器官系は分離、移植が可能であり、レシピエントの皮膚組織と適切に接続して生着し再生毛包を形成することが示されました。
5)再生毛包の機能的評価
iPS細胞から再生された皮膚器官系が、天然の皮膚を再現したかどうかを解析するために、皮膚に含まれる体毛の種類について解析しました。マウスの体毛にはZigzag、Awl/Auchene、Guardという3種類の毛種があり、それぞれが一定の割合で、一定の距離に配置されています。再生皮膚器官系ユニットの移植によって再生された毛包について詳しく調べてみると、萌出した毛種は天然の皮膚と同様に萌出していることが分かりました(図9)。この結果から、再生毛包は、正常な発生に基づく皮膚器官系として再生されたことが明らかになりました。
さらに、再生毛包の機能解析を行いました。マウスの体毛はおよそ20日間という一定の毛周期[7]で生え替わります。再生毛包の毛周期を解析したところ、マウスの天然の体毛と同様に約20日間の毛周期で生え替わることが明らかとなり、機能的な毛包再生が可能であることが示されました(図10)。
今後の期待
共同研究グループは、マウスiPS細胞から作製した複数のEBをコラーゲンゲルに埋め込み、生体へ移植してさまざまな上皮組織を誘導するCDB法を開発し、天然皮膚と同様の機能を持つ皮膚器官系を再生することに成功しました。この成果は世界に先駆けて、上皮・間葉相互作用を介して誘導される複数の器官を持つ複雑な皮膚器官系が再生可能であることを示しています。
今回の手法をヒトへの臨床応用として発展させるには、実験系を生体内移植系から生体外移植系へと発展させること、また、移植物がテラトーマ様組織を形成することなく皮膚器官系を誘導する実験系へと発展させることが必要です。本研究は将来、皮膚の重度の外傷や熱傷などの完全な再生を可能にするとともに、先天性乏毛症などの深刻な脱毛症や皮膚付属器に関する疾患の再生治癒につながると期待できます。
さらに卵巣や眼で発症するデルモイドと呼ばれる嚢腫は、嚢腫内に上皮組織や毛包、皮脂腺、歯などの器官ができることが知られています。しかし、その発症メカニズムの多くは、いまだ不明なままです。今回の研究成果を利用することによって、その発症メカニズムの解明につながる可能性があります。
原論文情報
- Ryoji Takagi, Junko Ishimaru, Ayaka Sugawara, Koh-ei Toyoshima, Kentaro Ishida, Miho Ogawa, Kei Sakakibara, Kyosuke Asakawa, Akitoshi Kashiwakura, Masamitsu Oshima, Ryohei Minamide, Akio Sato, Toshihiro Yoshitake, Akira Takeda, Hiroshi Egusa & Takashi Tsuji, "Bioengineering a 3D integumentary organ system from iPS cells using an in vivo transplantation model", Science Advances, doi: 10.1126/sciadv.1500887
発表者
理化学研究所
多細胞システム形成研究センター 器官誘導研究チーム
チームリーダー 辻 孝(つじ たかし)
(東京理科大学客員教授、北里大学医学部客員教授、東京歯科大学客員教授)
株式会社オーガンテクノロジーズ
代表取締役社長 杉村 泰宏(すぎむら やすひろ)
北里大学 医学部
形成外科・美容外科学
主任教授 武田 啓(たけだ あきら)
寄附講座 再生医療形成外科学(オーガンテクノロジーズ)
特任教授 佐藤 明男(さとう あきお)
東北大学大学院 歯学研究科 口腔修復学講座 分子・再生補綴学分野
教授 江草 宏(えぐさ ひろし)
 辻孝
辻孝
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
学校法人北里研究所 総務部広報課
Tel: 042-778-7883 / Fax: 042-778-8187
kohoh [at] kitasato-u.ac.jp(※[at]は@に置き換えてください。)
補足説明
- 1.iPS細胞(人工多能性幹細胞)
体細胞に特定の遺伝子を導入することで得られる、多様な細胞に分化できる分化多能性と自己複製能を獲得した細胞。これまでに網膜や腎臓細胞、血球細胞など、さまざまな機能細胞への分化誘導法が開発され、幅広い再生医療の実現に向けて研究開発が進められている。 - 2.胚様体(EB)
ES細胞やiPS細胞などを浮遊培養すると球体の細胞塊を形成する。この状態で2週間程度培養すると、さまざまな細胞種への分化が観察される。細胞の分化多能性を調べる一般的な方法の一つとして用いられている。EBとはEmbryoid Bodyの略。 - 3.上皮・間葉相互作用
ほとんどの器官は胎児期に、上皮細胞と間葉細胞が互いに刺激をし合うことによって誘導される器官原基(器官のもととなる細胞凝集塊)から発生する。この時の反応を「上皮・間葉相互作用」と呼ぶ。 - 4.ES細胞(胚性幹細胞)
哺乳類の着床前胚(胚盤胞=ブラストシスト)に存在する多能性幹細胞(内部細胞塊)から樹立した細胞。分化多能性と自己複製能を持つ。 - 5.テラトーマ
未分化型の細胞からなる腫瘍で、内部にさまざまな種類の組織を含む。多能性幹細胞を生体に未分化のまま移植すると、テラトーマが形成される。 - 6.Y-染色体 in situハイブリダイゼーション
ドナーが雄(染色体XY)、レシピエントが雌(染色体XX)の移植実験系において、ドナー細胞(Y染色体を持つ雄由来の細胞)を移植した後に、レシピエントにはじめから存在する組織と識別するため、組織の切片にY染色体を検出させる試薬を用いて解析する方法。Y染色体が検出された組織はドナー由来のものと分かる。 - 7.毛周期
体毛には毛周期と呼ばれるサイクルがあり、一定の周期で常に生え変わっている。毛周期は3つの段階に分かれており、成長期・退行期・休止期と進む。
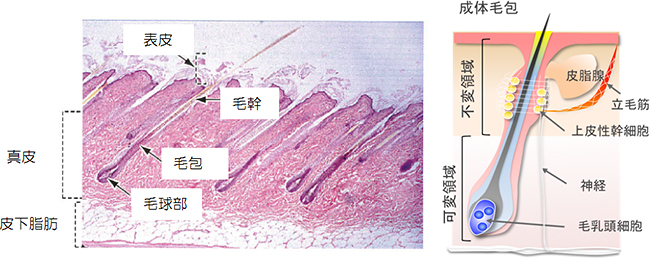
図1 皮膚の構造と機能
左:皮膚の顕微鏡画像。体表面から奥に向かって、上皮層(表皮)、真皮、皮下脂肪の3層からなる。出展は『Histology and Cell Biology, Mosby』。
右:毛包の模式図。
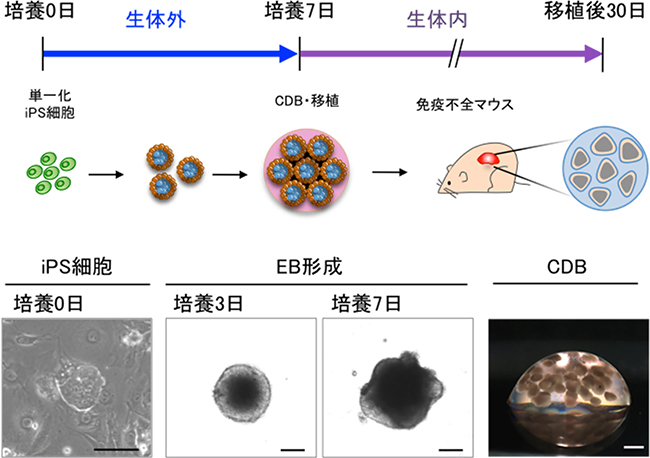
図2 CDB法によるマウスiPS細胞からの上皮性組織形成
上:実験の模式図。iPS細胞から生体外で胚葉体(EB)を作製し、コラーゲンゲルの中にEBを高密度に埋め込み(CDB法)、マウスの腎臓皮膜下に移植した。免疫学的拒絶を排除するため、免疫不全マウスに移植している。
下:培養中のiPS細胞と、EB形成過程の位相差像、CDB法によって作製した移植前のEB像。
スケールバーは位相差像:100μm、実体像:1mm(μm:1μmは、1000分の1mm)。
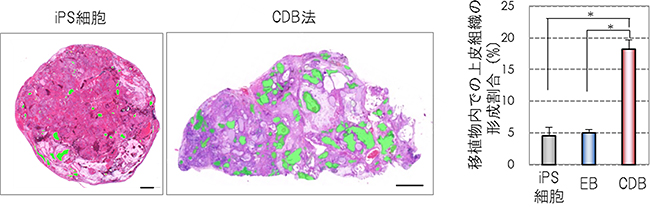
図3 CDB法により形成した移植物の上皮組織からなる嚢胞の解析
左、中央:iPS細胞移植(左)とCDB法により形成した移植物(中央)の、画像解析により可視化した上皮組織の画像。緑の部分は外胚葉性上皮組織を示す。スケールバーは100μm。
右:移植部内での上皮組織の形成割合。CDB法は他の手法と比べて約4倍の上皮組織を形成する。
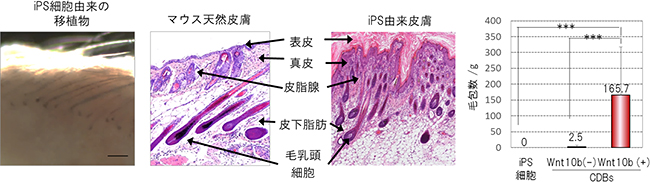
図4 CDB法による皮膚器官系の形成
左:移植後30日目に摘出したiPS細胞由来移植物の実体像。スケールバーは500μm。
中央:マウス天然皮膚(左)と生理活性物質Wnt10bで刺激したEBを用いたCDB法によって再生したiPS細胞由来の皮膚器官系のHE(ヘマトキシリン・エオジン)染色画像。
右:各条件下において、形成された移植物の単位重量あたりに再生される毛包の本数。Wnt10bで刺激したEBを用いると毛包の本数が有意に増えていることが分かる。
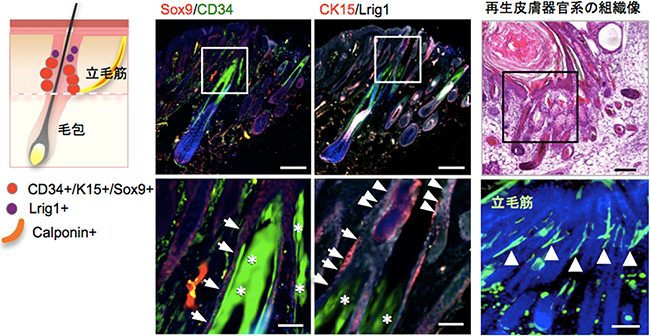
図5 iPS細胞由来皮膚器官系に含まれる再生毛包や立毛筋
左:毛包を構成する細胞、および毛包の付属器官の模式図。
中央:毛包を構成する細胞の免疫組織染色像。毛包の上部、中部を構成する細胞(矢頭および矢印)が、天然毛包と同様に、毛包に対して適切な位置に配置されている。*は毛幹部の自家蛍光によるもの。スケールバーは、上段200μm、下段50μm。
右:iPS細胞由来皮膚器官系のHE染色像、および免疫染色像。立毛筋(矢頭)が毛包に適切に接続している。スケールバーは、上段200μm、下段100μm。
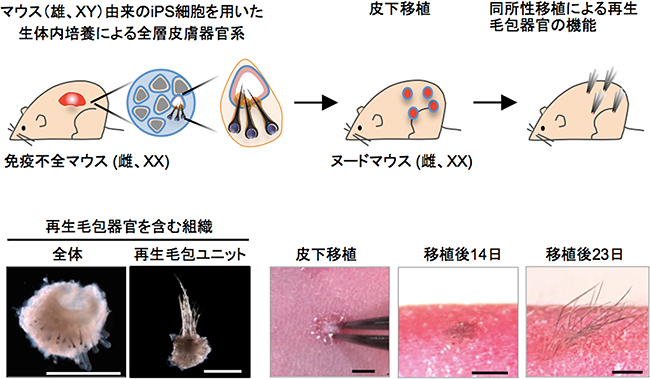
図6 再生皮膚器官系から分離した再生毛包の皮下移植
上:CDB法により得られた皮膚器官系に含まれる毛包を10~20本含んだ組織を、再生皮膚器官系ユニットとして採取し皮下移植を行った。
下左:iPS細胞由来の再生皮膚器官系と採取した再生皮膚器官系ユニット。スケールバーは500μm。
下右:再生皮膚器官系ユニットを皮下移植による毛包の萌出、成長がみられた。スケールバーは1mm。
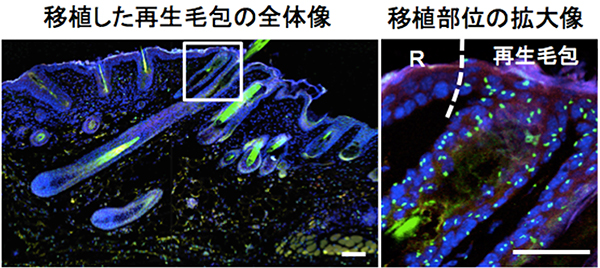
図7 皮下移植したY染色体を持つ再生毛包の組織解析
左:移植した再生毛包の全体像。スケールバーは200μm。
右:左の白い四角部分の拡大像。緑色の点状にみえるシグナルがY染色体。移植した再生毛包特異的に緑色のシグナルがみえることが分かる。R:レシピエントの組織。スケールバーは100μm。
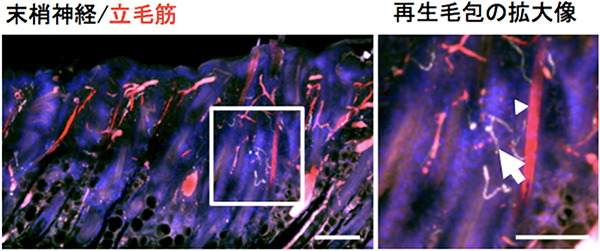
図8 再生毛包の立毛筋に接続したレシピエントの神経
再生毛包に含まれる立毛筋(矢頭)に接続したレシピエントの神経(矢印)。スケールバーは全体像が200μm、拡大像が100μm。
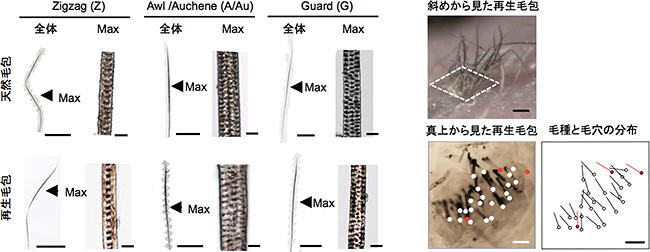
図9 天然毛包と再生毛包の毛種と毛穴間距離
左:天然および再生毛包の毛種と毛菅が最大幅になる部分の拡大図。スケールバーは全体図(左側)が2mm、拡大図(右側)が20μm。
右:移植した再生皮膚器官系ユニットから萌出した再生毛包の斜め、および真上からの写真。右下は、真上から見た再生毛包の毛種と毛穴の分布をプロットした図。白丸はZigzag、赤丸はAwl/AucheneとGuardを、丸に付属した線は、毛包の生えている向きを示す。スケールバーは50μm。
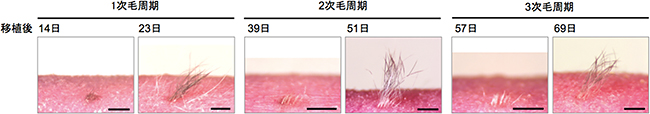
図10 移植した再生毛包の毛周期の解析
マウスに皮下移植した再生毛包ユニットから萌出した再生毛包の毛周期。およそ20日間前後の周期で毛が生え変わっている様子が分かる。スケールバーは1mm。
