要旨
理化学研究所(理研)生命システム研究センター細胞動態計測研究グループの岩城光宏上級研究員らの国際共同研究グループ※は、DNAナノテクノロジーを用いて世界最小のコイル状人工バネ「ナノスプリング」を作製し、聴覚に関わるメカノセンサータンパク質[1]ミオシンVI[2]の動きを捉え、アクチンフィラメント[3]と強固に結合するメカニズムを分子レベルで明らかにしました。
細胞内に数多く存在するメカノセンサータンパク質は、物理的な力による機能制御を受け、細胞増殖、分化、形態形成や細胞死などの細胞レベルのふるまいに関わります。一方で“力がどのようにしてメカノセンサータンパク質の機能を制御するのか”を調べる技術は乏しく、不明な点が多くあります。従来の技術では、タンパク質の機能や動態を1分子レベルで可視化すると同時にタンパク質に力を加えることは難しく、メカノセンサータンパク質を“効率よく、観ながら触る”新たな技術の開発が求められていました。
国際共同研究グループは、DNAを編む「DNAオリガミ[4]」と呼ばれる技術を用いて、タンパク質サイズの世界最小のコイル状人工バネ「ナノスプリング」を作製しました。そして、自律的に力を発生するモータータンパク質[5]でもあるミオシンVIを結合させ、ナノスプリングを引き延ばす過程を蛍光1分子イメージング[6]で超解像ナノ計測[7]し、ミオシンVIが力に応答して機能を調節する機構を可視化しました。その結果、ミオシンVIは力を受けると、細胞骨格であるアクチンフィラメントへの結合様式を変化させて強固な結合状態(アンカー結合状態)を作ることが分かりました。ミオシンVIは内耳に存在するステレオシリア[8]の形態維持を担っています。ステレオシリアが受けた音(空気の振動)による物理的な力刺激がミオシンVIに伝わり、アクチンフィラメントとアンカー結合状態を生じることで、その形態を安定に維持していることが示唆されます。
本研究で開発したナノスプリングはバネ定数のチューニングが可能でプログラム能力も高いため、さまざまなメカノセンサータンパク質への応用が可能です。電子顕微鏡や原子間力顕微鏡との併用も可能なため、力を加えながら分子構造や動態を観る手法として必須のツールとなることが期待できます。
本研究は、国際科学雑誌『Nature Communications』(12月12日付け:日本時間12月12日)に掲載されます。
※国際共同研究グループ
理化学研究所 生命システム研究センター 細胞動態計測コア
細胞動態計測研究グループ
上級研究員 岩城 光宏(いわき みつひろ)
グループディレクター 柳田 敏雄(やなぎだ としお)
ハーバード大学 医学部
博士研究員 シェリー・ウィッカム(Shelley Wickham)
准教授 ウィリアム・シー(William Shih)
東京大学 新領域創成科学研究科
助教 池崎 圭吾(いけざき けいご)
背景
細胞は、培養環境、生体内環境のさまざまな物理的な力を感知して、細胞増殖、分化、形態形成や細胞死などに利用しています。そのメカニズムで重要な役割を果たすのがメカノセンサータンパク質であり、触覚に関わる機械受容イオンチャネルや、聴覚の正常な機能に必須なミオシンVIなどが知られています。
力がどのようにしてメカノセンサータンパク質の機能を制御しているのか明らかにすることは、メカノバイオロジー[9]の中心課題の1つですが、調べるための技術が乏しく不明な点が多くあります。その原因となっていたのは、個々のメカノセンサータンパク質を“効率よく、観ながら触る”技術の不足です。1分子レベルでの研究における従来の技術では、蛍光観察などで観る、原子間力顕微鏡や光ピンセット法[10]などで触る・力を加えることを、別々に行うことがほとんどでした。
そこで国際共同研究グループは、メカノセンサータンパク質に力を加えながら、その応答を1分子レベルで効率的に観る技術の開発を行いました。
研究手法と成果
これまで、タンパク質に力を加えるためには、カンチレバーや高出力レーザーといった分子よりも格段に大きなスケールの装置が必要でした。そのため、1分子レベルで観るための蛍光1分子イメージング顕微鏡の装置や観察条件は、厳しく制約されました。そこで、大きなスケールの装置を必要としないナノスケールデバイスの作製を目指しました。
タンパク質と同程度のサイズのデバイスを作るため、DNAを材料として編み上げて束ねる「DNAオリガミ」というナノテクノロジーを応用して、世界最小のコイル状人工バネ「ナノスプリング」を作製しました(図1)。コイル直径は30ナノメートル(nm、1ナノメートルは10億分の1メートル)、長さは100~1,000nmです。DNA分子から構成されているため化学修飾が容易であり、さまざまな分子との接続が可能です。
作製したナノスプリングが、力を加えてその大きさを測るデバイスとして機能するか、光ピンセット法を用いてバネ定数[11]を評価した結果、ピコニュートン(1兆分の1ニュートン)の力を精度よく定量できることが分かりました。細胞内のメカノセンサータンパク質が受ける力はピコニュートンなので、生理的なオーダーの力を加えることができるといえます。
実際にメカノセンサータンパク質に加わる力を測るため、ミオシンVIにナノスプリングの一端を連結し、もう一端を細胞骨格であるアクチンフィラメントに連結しました(図2)。ミオシンVIはメカノセンサータンパク質であると同時に、力がかかっていない、もしくは、弱い力しかかかっていないときには自律的にアクチン上を一方向運動するモータータンパク質でもあります。そのため、始めはモータータンパク質としてミオシンVIが運動することでナノスプリングを引き延ばし、徐々に大きな力がかかっていきます。その後、ミオシンVIの生み出す最大力とバネの力が釣り合うと停止します。この過程における分子動態変化を蛍光1分子イメージングで超解像ナノ計測しました。
ミオシンVIは二量体を形成しており、モータードメインとよばれる球状部位2つがアクチンフィラメントと結合しています。そして、1ピコニュートン以下の弱い力しかかかっていない時には、人間の歩行運動のように2つのモータードメインを交互に前に出して動きます。超解像ナノ計測の結果、2ピコニュートン以上の大きな力がかかった時には、2つのモーター部位を近接させることでアクチンフィラメントと強固な結合状態(アンカー結合状態)を形成することが分かりました。2ピコニュートン前後でミオシンVIの生み出す最大力とバネの力が釣り合い、そこに留まろうとするために強い結合を形成すると考えられます。また、アクチンフィラメントとアンカー結合する現象自体は、貝柱の筋肉に存在するミオシンIIでも起こることが知られていますが、その場合、アンカー結合をサポートするタンパク質が存在し、ATPのエネルギーを消費しないと考えられています。今回の実験では、①ミオシンVIはサポートするタンパク質を必要とせずアクチンフィラメントとの結合様式を変化させるだけでアンカー結合状態を生みだすこと、②ATPのエネルギーを消費しアンカー結合状態を時々微調整している(モータードメインの位置を入れ替える)こと、が分かりました。
ミオシンVIは、聴覚器官である蝸牛内のステレオシリアの形態維持をしていることが知られています(図3)。ステレオシリアは、音(空気の振動)に揺さぶられることで脳内に信号を伝える役割をします。今回の実験により、ミオシンVIは、揺さぶりによって生じる力に応答してアクチンフィラメントにアンカー結合し、持続的な形態維持を行っていることが示唆されました。また、空気の振動はダイナミックな力の変化を生みだしますが、その変化にうまく適応できるように、ATPのエネルギーを消費して強固な結合状態を微調整していることも考えられます。
今後の期待
国際共同研究グループが開発したナノスプリングは、バネ定数のチューニングが可能でプログラム能力も高く、さまざまなメカノセンサータンパク質に応用可能です。また、電子顕微鏡や原子間力顕微鏡との併用も可能なため、力を加えながら分子構造や動態を観る手法を大きく拡張し、メカノバイオロジー分野で必須のツールとなることが期待されます。
今後、ナノスプリング発展させて能動的に力を加えるためのデバイスを作製し、細胞内の細胞骨格や細胞間接着分子に組み込むことができれば、生命の発生過程で生じる細胞内や細胞間の力の可視化や制御に応用できる可能性があります。
原論文情報
- Mitsuhiro Iwaki, Shelley F. Wickham, K. Ikezaki, T. Yanagida, William M. Shih, "A programmable DNA origami nanospring that reveals force-induced adjacent binding of myosin VI heads", Nature Communications, doi: 10.1038/ncomms13715
発表者
理化学研究所
生命システム研究センター 細胞動態計測コア 細胞動態計測研究グループ
上級研究員 岩城 光宏(いわき みつひろ)
 岩城 光宏
岩城 光宏
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.メカノセンサータンパク質
物理的な力や歪みを感じて機能を制御するタンパク質の総称。触覚や聴覚を担う機械受容器で同定されているものが多いが、様々な細胞・組織内で広範に存在し、生理機能に重要な役割を果たしている。 - 2.ミオシンVI
多様な細胞種に広く発現しているミオシンの一種。聴覚の正常な機能に必須のタンパク質でもある。ミオシンはATP加水分解酵素であり、筋肉の中で力を出すミオシンIIがよく知られている。 - 3.アクチンフィラメント
アクチンとは細胞骨格タンパク質の1つ。単量体のG-アクチンが重合して繊維状アクチン(F-アクチン)を形成する。F-アクチンから成るアクチンフィラメントは、細胞の形態や運動に深く関わる。 - 4.DNAオリガミ
DNAを材料にして編み物のように束ねることで、思い通りの2次元、3次元ナノ構造物を作り上げる技術。DNAナノテクノロジーの一種。 - 5.モータータンパク質
ATPを加水分解するときに得られるエネルギーを用いて力を発生するタンパク質の総称。 - 6.蛍光1分子イメージング
蛍光分子1個が出す光を顕微鏡観察することができる高感度蛍光観察技術。全反射蛍光顕微鏡とイメージング用超高感度カメラから構成される。 - 7.超解像ナノ計測
蛍光1分子イメージングで得られるデータに画像解析技術を併用することで、蛍光分子の位置を1ナノメートルの精度で定量することができる手法。 - 8.ステレオシリア
内耳細胞に存在する発達した微絨毛。音(空気の振動)によって揺り動かされ、その機械刺激を電気信号に変換し脳に伝える役割をする。 - 9.メカノバイオロジー
生体における”力”の役割と仕組みを解明して、発生やがん、再生医療などの臨床的課題の解決をめざす分野。 - 10.光ピンセット法
近赤外レーザーを用いて1ミクロン程度の微粒子を捕捉する技術。 - 11.バネ定数
バネにかかる力の大きさによって起きるバネの長さの変化を数値で表したもの。具体的にはバネに負荷を加えた時の荷重を伸びで割った比例定数であり、フックの法則にあらわれる。
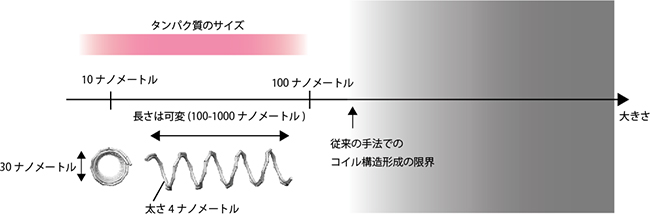
図1 DNAオリガミで作成したナノスプリング
フォトリソグラフィーやフォーカスドイオンビームなどを用いた微細加工技術の限界を超えて、タンパク質サイズのコイル状人工バネを作製した。DNA分子から構成されているため化学修飾が容易であり、様々な分子との接続が可能である。
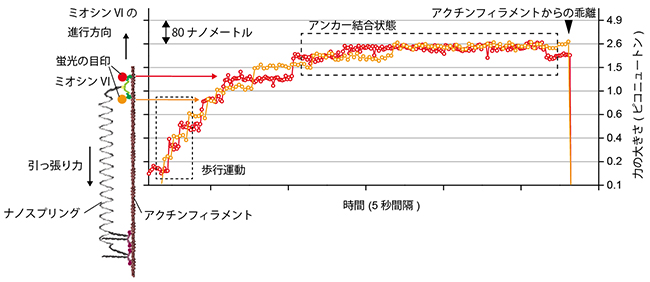
図2 力を加えた状態での1分子動態イメージング
ナノスプリングの一端にミオシンVI(緑)を連結し、もう一端にはナノスプリングをアクチンフィラメントに固定するためのタンパク質分子(NEMミオシンII)を連結した。ミオシンVIの2つのモータードメインに蛍光の目印(蛍光量子ドット)をラベルし、超解像ナノ計測することで、各ドメインの動きを、力がかかった状態で可視化することができた。歩行運動時には交互にモータードメインが動いているが、停止状態(アンカー結合状態)では、モータードメインが近接し、長く同じ位置に滞在していることが分かる。また、アンカー結合状態をとってからも2つのモータードメインが小さく前後していることから、ATPのエネルギーを消費し強固な結合状態を時々微調整していることが分かる。
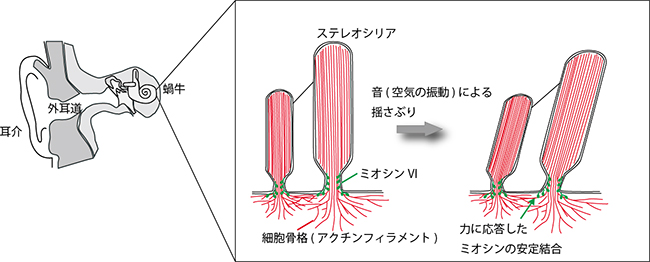
図3 聴覚器官内でのミオシンVIの役割
蝸牛内に存在する内耳有毛細胞のステレオシリアの概略図。ステレオシリア内にはアクチンフィラメント(赤線)の束が存在し、その根元にミオシンVI(緑)が局在している。空気の振動を受けるとステレオシリアが揺さぶられ根元にも大きな力が加わる。ミオシンVIはその力に応答し、強固なアンカー結合を生じていると考えられる。
