理化学研究所(理研)環境資源科学研究センター統合メタボロミクス研究グループの榊原圭子上級研究員、斉藤和季グループディレクター(環境資源科学研究センター センター長)、京都大学の山村正臣特任助教、梅澤俊明教授らの共同研究グループは、シロイヌナズナの種子に含まれる「ネオリグナン[1]」の生合成に必要な酵素とタンパク質を発見し、ネオリグナンが種皮の外来異物透過性[2]を抑制することを明らかにしました。
本研究成果は、新たな薬効成分の創出に向けたネオリグナンの代謝エンジニアリング[3]に貢献すると期待できます。
ネオリグナンは植物に含まれる化合物群であり、ヒトに有益な抗潰瘍性や抗菌活性などさまざまな生理活性を持っています。しかし、これまでネオリグナンの生合成経路や植物にとっての役割は不明でした。
今回、共同研究グループは、シロイヌナズナの種子に存在するネオリグナンの詳細な化学構造を決定しました。また、ネオリグナンの生合成に関わるディリジェントタンパク質[4]と酸化酵素ラッカーゼ[5]の遺伝子を同定し、ネオリグナンの生合成経路を明らかにしました。さらに、ネオリグナンが種皮の外来異物透過性を抑制したことから、ネオリグナンは植物の種子を乾燥や酸化、害虫や病原菌などの環境要因によるストレスから化学的に防御する役割を果たしていると考えられます。
本研究は、科学雑誌『The Plant Cell』の掲載に先立ち、オンライン版(11月27日付)に掲載されました。

シロイヌナズナの種子の走査電子顕微鏡写真(左)と本研究で決定したネオリグナンの構造(右)
背景
植物には100万種ともいわれる多様な化合物を生産する能力があり、生産された化合物の一部は医薬品などの成分として利用されています。リグナン[1]やネオリグナンと呼ばれる化合物群もその一つです。例えば、ポドフィルムの根から単離されたリグナン(ポドフィロトキシン)は抗がん薬のリード化合物[6]であり、また漢方に使われる生薬の「厚朴(こうぼく)」の原料であるホオノキの樹皮から単離されたネオリグナン(マグノロール、ホオノキオール)には、抗炎症作用、抗酸化作用、抗がん作用、神経保護作用があると報告されています。
これまでに、多様な構造のリグナン、ネオリグナンが報告されてきましたが、植物体内で生産される量が限られていることから、それらの詳細な構造決定や分析は困難でした。そのため、多くのリグナンやネオリグナンの効能や植物における役割には不明点が多く、その解明には、生合成に関わる酵素、遺伝子、生合成経路を明らかにし、微生物などで安定的に大量生産する必要があります。
近年、ポドフィロトキシンをはじめとしたリグナンの生合成酵素遺伝子の研究は盛んに行われており、いくつかの生合成系酵素遺伝子が見いだされてきました。しかし、ネオリグナンの生合成経路は全く分かっておらず、またリグナンやネオリグナンが植物にとってどのような役割を担っているのかも不明でした。
研究手法と成果
共同研究グループは、リグナンとネオリグナンの構造が似ていることに着目し、その構造構築に関わるディリジェントタンパク質に焦点を当てました。研究チームは、これまでにシロイヌナズナの種子で特異的に働くディリジェントタンパク質AtDP1/AtDIR12の遺伝子欠損変異体をメタボローム解析[7]し、ネオリグナンらしき物質が野生型に比べて減っていることを見いだしていました。今回、この物質の構造を明らかにするため、予想した化学構造のネオリグナンを有機合成して、構造比較することで、その相対的立体構造を含む詳細な構造を明らかにしました(図1)。そして、ディリジェントタンパク質AtDP1/AtDIR12が、これらのネオリグナンの生合成に必須であることを証明しました。
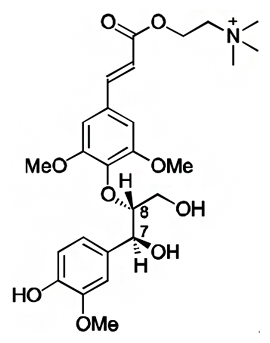
図1 本研究で決定したシロイヌナズナの種子に含まれるネオリグナンの構造の一つ
次に、ネオリグナンの生合成に関わる酸化酵素のラッカーゼを探索しました。AtDP1/AtDIR12遺伝子と発現パターンが似ているラッカーゼ遺伝子の変異体を分析したところ、AtLAC5遺伝子が欠損した植物体でネオリグナンが減少していることが分かりました。このことから、ラッカーゼの一つであるAtLAC5がネオリグナン合成に関わることが明らかになりました。驚いたことに、AtLAC5遺伝子欠損植物では、特定のネオリグナンのみが減少していました。これまで、ラッカーゼは、酸化する対象物質を選ばないと考えられていたため、この発見は大きな驚きで、酸化酵素の基質特異性の面から興味深いものです。このように、シロイヌナズナの種子におけるネオリグナンの生合成経路と生合成に関わるタンパク質と酵素の遺伝子を決定することに成功しました(図2)。
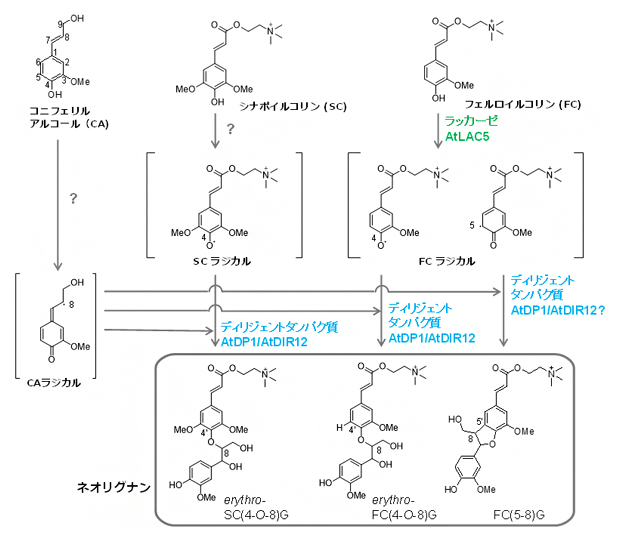
図2 シロイヌナズナの種子におけるネオリグナンの生合成経路
本研究では、図1で示したerythro-SC(4-O-8)Gのほかにerythro-FC(4-O-8)Gの構造も決定し、シロイヌナズナの種子におけるネオリグナンの生合成経路を明らかにした。酸化酵素ラッカーゼAtLAC5(緑字)は、フェルロイルコリン(FC)を酸化し、FCラジカルの生成に関わる。ディリジェントタンパク質AtDP1/AtDIR12(水色字)は、FCラジカルあるいはシナボイルコリン(SC)ラジカルの4位と別途生成したコニフェリルアルコール(CA)ラジカルの8位のカップリングに関与している。
さらに、ネオリグナンの生合成に関わるディリジェントタンパク質AtDP1/AtDIR12とラッカーゼAtLAC5が種皮に存在したことから、ネオリグナンの植物体内での役割を明らかにするために、種皮の外来異物透過性を調べました。AtDP1/AtDIR12遺伝子が機能できなくなり、ネオリグナン含量が著しく減少したatdp1変異体では、種皮の異物透過性が高いことが分かりました(図3)。この結果から、ネオリグナンは種皮において異物透過性を抑制することで、種子にダメージを与える外来の環境要因から守っていると考えられます。
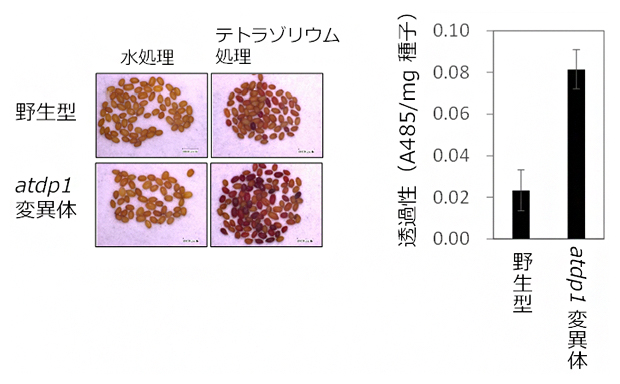
図3 ネオリグナンが減少した種子では外来異物が透過しやすくなる
テトラゾリウムは無色の薬品であるが、種皮を透過すると内在性の酵素により赤色の物質に変換される。種子をテトラゾリウム染色した場合、より赤い(A485の値が高い)ほど種皮の異物透過性が高いといえる。
今後の期待
ネオリグナンの生合成に関わる酵素、遺伝子、生合成経路を明らかにしたことで、植物や微生物を用いた代謝工学などで大量に安定的にネオリグナンを供給できる系を確立することが可能になりました。これによって、多様なネオリグナンの構造や植物での機能、ヒトに対する薬効を調べることができます。また、ネオリグナンが外敵や環境毒性物質などの外来性の障害因子から種子を保護するメカニズムの研究は、将来的に環境ストレス下での植物の生産性向上につながります。
現在、漢方薬原料の多くは、輸入に頼っており、また、その成分や品質は、生育・栽培条件、産地などによっても変わります。植物の有用成分の生合成に関わる酵素、遺伝子、生合成経路が解明されることは、有用成分を高蓄積する生薬の基原植物の育種にも役立ちます。
本研究成果は、国際連合が2016年に定めた17項目の「持続可能な開発目標(SDGs)」のうち、「2. 飢餓をゼロに」、「3. すべての人に健康と福祉を」、「13. 気候変動に具体的な対策を」、「15. 陸の豊かさも守ろう」に貢献するものです。
補足説明
- 1.ネオリグナン、リグナン
植物に含まれるフェニルプロパノイド(ベンゼン環に直鎖状プロパンが結合した構造を基本骨格とする天然芳香族化合物)の二量体のうち、それぞれのC8位同士で結合したものをリグナン、それ以外をネオリグナンという。どちらも一連の化合物群の総称である。 - 2.種皮の外来異物透過性
種子は、種皮によってさまざまな環境要因(乾燥や酸化によるストレス、害虫や病原菌によるストレス、環境からの毒性物質など)から守られている。種皮の異物透過性が高いと環境要因の影響を受けやすく、種子の寿命が短くなる場合がある。 - 3.代謝エンジニアリング
生物(植物、動物、細菌など)の代謝に関わる酵素やタンパク質、それらの遺伝子を用いて、人間の生活に役立つ新たな物質の創出を目指す技術のこと。 - 4.ディリジェントタンパク質
ディリジェントとは、ラテン語のdirigereに由来する言葉で、案内する、整列させるなどの意味がある。ディリジェントタンパク質は、ラッカーゼによって酸化されたモノリグノール(コニフェリルアルコールなど)等のカップリング様式を決定するタンパク質である。ディリジェントタンパク質が存在しないと、ランダムに反応して、さまざまな結合様式の化合物が生成されてしまう。 - 5.ラッカーゼ
分子状酸素を利用してフェノール性の基質を酸化し、フェノキシラジカルを生成する酵素。最初に、漆(英語でlacquer)から見つけられ、漆ではウルシの成分であるウルシオールを酸化する。 - 6.リード化合物
生理活性を持ち、医薬品開発の候補となり得る化合物。リード化合物を化学的に修飾することで、より薬効の高く安全性の高い化合物が開発される。 - 7.メタボローム解析
特定の化合物だけでなく、すべての化合物を対象として代謝物分析すること。着目している遺伝子の機能予測が難しい場合、メタボローム解析によって変化が見られた化合物が明らかになれば、遺伝子の機能解明の大きな手掛かりとなる。ただし、変化の見られた化合物の構造が不明なことも多い。
共同研究グループ
理化学研究所 環境資源科学研究センター 統合メタボロミクス研究グループ
上級研究員 榊原 圭子(さかきばら けいこ)
研究員 中林 亮(なかばや しりょう)
テクニカルスタッフ 菅原 聡子(すがわら さとこ)
専門技術員 森 哲哉(もり てつや)
研究員(研究当時) 松田 史生(まつだ ふみお)
(現 大阪大学大学院 情報科学研究科 教授)
グループディレクター・センター長 斉藤 和季(さいとう かずき)
京都大学 生存圏研究所
教授 梅澤 俊明(うめざわ としあき)
准教授 飛松 裕基(とびまつ ゆうき)
特任助教 山村 正臣(やまむら まさおみ)
サントリーグローバルイノベーションセンター
主任研究員 小埜 栄一郎(おの えいいちろう)
原論文情報
- Keiko Yonekura-Sakakibara, Masaomi Yamamura, Fumio Matsuda, Eiichiro Ono, Ryo Nakabayashi, Satoko Sugawara, Tetsuya Mori, Yuki Tobimatsu, Toshiaki Umezawa, Kazuki Saito, "Seed-coat protective neolignans are produced by the dirigent protein AtDP1 and the laccase AtLAC5 in Arabidopsis", The Plant Cell, 10.1093/plcell/koaa014
発表者
理化学研究所
環境資源科学研究センター 統合メタボロミクス研究グループ
上級研究員 榊原 圭子(さかきばら けいこ)
グループディレクター 斉藤 和季(さいとう かずき)
(環境資源科学研究センター センター長)
京都大学 生存圏研究所
教授 梅澤 俊明(うめざわ としあき)
特任助教 山村 正臣(やまむら まさおみ)
 榊原 圭子
榊原 圭子
 斉藤 和季
斉藤 和季
 梅澤 俊明
梅澤 俊明
 山村 正臣
山村 正臣
報道担当
理化学研究所 広報室 報道担当
お問い合わせフォーム
京都大学総務部広報課 国際広報室
Tel: 075-753-5729 / Fax: 075-753-2094
Email: comms [at] mail2.adm.kyoto-u.ac.jp
※[at]は@に置き換えてください。
