理化学研究所(理研)環境資源科学研究センターケミカルバイオロジー研究グループのイスラム・アデル・アブデルハキム研修生、本山高幸専任研究員、長田裕之グループディレクターらの研究チームは、化合物処理したカビから、新しい強力な抗マラリア化合物を発見しました。
本研究成果は、気候変動に伴い今後深刻化すると懸念されるマラリアの蔓延防止に貢献すると期待できます。
マラリアを制御する薬は、クロロキンをはじめとしてこれまで数多く開発されてきましたが、耐性菌の出現の問題があり、新たな制御薬剤の開発が望まれています。
今回、研究チームは、二次代謝[1]を制御する化合物で処理したカビから、強力な抗マラリア活性を示す新しい天然化合物ジヒドロルシラクタエン(DHLC)を取得することに成功しました。DHLCは、マラリア原虫に対する50%生育阻害濃度(IC50)[2]が1.5ナノモーラー(nM、1nMは10億分の1モーラー)であり、非常に強力な活性を示します。また、既知の抗マラリア薬として知られるクロロキンの耐性株に対しても同様に強力な効果を示すことから、新たな抗マラリア薬あるいはそのリード化合物[3]となることが期待できます。
本研究は、米国の科学雑誌『Journal of Natural Products』(2021年12月24日号)に掲載されました。
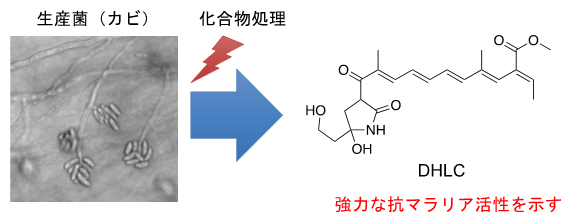
新しい抗マラリア天然化合物の化学構造と生産菌(カビ)
背景
マラリアは、マラリア原虫に感染した蚊に刺されることで感染する病気です。熱帯や亜熱帯の地域で流行しており、2018年の統計(World malaria report 2018)によると、1年で約2億2000万人が感染し、推計で43万5000人が死亡しています注1)。これまでクロロキンやアルテミシニンなど数多くの抗マラリア薬が開発されてきましたが、耐性菌の出現の問題があり、新たな制御薬剤の開発が望まれています。
カビは多様な天然化合物を生産する能力を持ち、カビが生産する化合物は、これまでもペニシリンやスタチンなどの医薬品として広く使われてきました。近年、カビの全ゲノム配列が明らかになるにつれて、カビは予想よりはるかに多くの二次代謝遺伝子を持っていることが分かってきました。本山高幸専任研究員、長田裕之グループディレクターらは2021年に、カビの隠された二次代謝産物の生産能力を引き出すため、二次代謝を活性化する化合物を探索した結果、「NPD938」を見いだしました注2)。NPD938は、いくつかのカビで二次代謝を制御することが明らかになっています。
今回、研究チームは二次代謝を制御する化合物であるNPD938で処理したカビの一種から、新しい天然化合物の単離を試みました。
- 注1)WORLD MALARIA REPORT 2018
- 注2)Motoyama, Takayuki. et al. Screening of tenuazonic acid production-inducing compounds and identification of NPD938 as a regulator of fungal secondary metabolism. BIOSCIENCE BIOTECHNOLOGY AND BIOCHEMISTRY, 85 (10): 2200-2208 OCT 2021
研究手法と成果
研究チームはまず、さまざまなカビをNPD938で処理し、生産物を解析することで二次代謝産物の生産誘導が生じるかを調べました。その結果、ルシラクタエン[4]の生産菌であるカビの一種Fusarium sp. RK97-94で、二次代謝産物が生産誘導されていることを見いだしました。
次に、NPD938の存在下でルシラクタエン生産菌を大量培養し、生産誘導される化合物を精製したところ、ルシラクタエンと類似の構造を持つ2種類の新しい化合物(ジヒドロNG391、ジヒドロルシラクタエン[DHLC])と1種類の既知化合物(13α-ヒドロキシラクタエン)が得られました(図1)。ルシラクタエン生産菌は、通常の培養条件では、ルシラクタエンおよび類似の化合物であるNG391を主に生産することから(図1左下)、NPD938処理により生産する化合物が変化したことが分かりました。
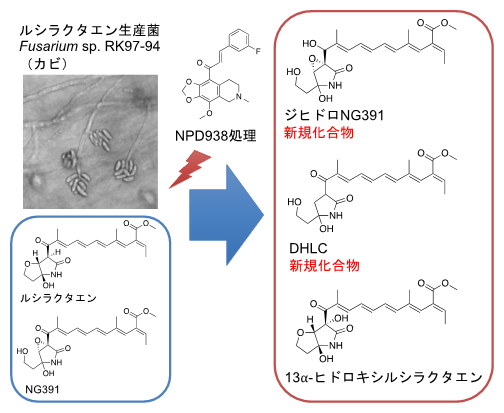
図1 NPD938で処理したカビから単離された化合物
ルシラクタエンの生産菌であるFusarium sp. RK97-94(カビ)をNPD938の存在下で大量培養し、生産誘導される化合物を単離し、構造を明らかにした。ルシラクタエンと類似の構造の2種類の新規化合物のジヒドロNG391とジヒドロルシラクタエン(DHLC)と1種の既知化合物(13⍺-ヒドロキシラクタエン)を取得した。Fusarium sp. RK97-94は、通常の培養条件ではルシラクタエンとNG391を主に生産する(左下)。
これら三つの化合物の生物活性を評価したところ、DHLCがマラリア原虫に対する50%生育阻害濃度(IC50)が1.5 ナノモーラー(nM、1nMは10億分の1モーラー)と、非常に強力な抗マラリア活性を示すことが分かりました(図2)。また、DHLCの動物細胞や微生物に対する生育阻害活性は低く、マラリアに対する特異性が高いことが明らかになりました。
さらに、得られた化合物の生物活性の比較から、抗マラリア活性に必要な構造が明らかになりました(図2)。本山高幸専任研究員、長田裕之グループディレクターらは、ルシラクタエンがIC50 0.15 マイクロモーラー(μM、1μMは100万分の1モーラー)という強力な抗マラリア活性を持つことを2020年に報告しています注3)。ルシラクタエンの5員環[5]部分が開環した構造のDHLCは、ルシラクタエンの100倍の非常に強力な活性を示しました。また、NG391と比較すると、脱エポキシ化[6]で1200倍活性が向上することが分かりました。反対に、ルシラクタエンの水酸化[7]やNG391のカルボニル基[8]の還元をした場合には、活性が低下することも分かりました。
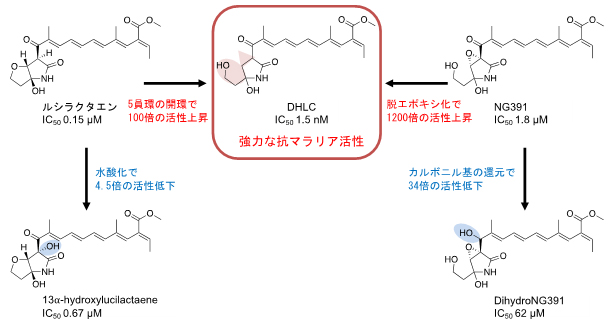
図2 取得した化合物の抗マラリア活性および構造活性相関
取得した化合物の構造及び抗マラリア活性におけるIC50(50%生育阻害濃度)を示した。また、ルシラクタエンとNG391に関するデータも対照として示し、どのような構造変化が抗マラリア活性に影響するのかについて明らかにした。
また、抗マラリア薬として実際に使われているクロロキンに対する耐性マラリア株に対しても、DHLCは同様に強力な活性(IC50 =1.5 nM)を示しました。この結果から、DHLCはクロロキンとは異なる作用メカニズムで生育阻害を引き起こしていることが明らかになり、クロロキン耐性マラリア株などにも有効な抗マラリア薬としての可能性が示されました。
- 注3)Kato, Sho; Motoyama, Takayuki,et al. Biosynthetic gene cluster identification and biological activity of lucilactaene from Fusarium sp. RK97-94. BIOSCIENCE BIOTECHNOLOGY AND BIOCHEMISTRY, 84 (6):1303-1307 JUN 2020
今後の期待
本研究では、二次代謝を制御する化合物で処理したカビの一種から、強力な抗マラリア活性を示す新しい天然化合物であるDHLCを見つけ出しました。
DHLCは、マラリア原虫に対するIC50が1.5nMであり、非常に強力な活性を示します。また、抗マラリア薬として使われているクロロキンに対する耐性株に対しても同様に強力な効果を示すことから、新たな抗マラリア薬あるいはそのリード化合物となることが期待できます。
今回の研究成果は、気候変動に伴い今後深刻化すると予想されるマラリアの制御を可能にし、2016年に国際連合が発表した「持続可能な開発目標(SDGs)[9]」のうち、「3.すべての人に健康と福祉を」や「13.気候変動に具体的な対策を」に貢献するものです。
補足説明
- 1.二次代謝
生物体を構成、維持する上で重要な代謝を一次代謝と呼ぶ。一方、生育そのものには必要とされない代謝は二次代謝と呼ばれ、抗生物質などの作製に関与する。 - 2.50%生育阻害濃度(IC50)
化合物の有効度を示す値であり、どの濃度で生育を半分(50%)阻害できるかを示す。 - 3.リード化合物
創薬過程の出発点となる新薬候補化合物のこと。 - 4.ルシラクタエン
カビが生産する二次代謝産物の一種。動物細胞の細胞周期を阻害し、生育を抑制する活性がある。 - 5.5員環
化合物中で、結合する五原子が環状になっている構造。 - 6.脱エポキシ化
酸素を含む3員環構造であるエポキシ環を除去する反応。 - 7.水酸化
水酸基(?OH)を結合して水酸化物を生じる化学反応。 - 8.カルボニル基
有機化学における置換基の一つで、-C(=O)-と表記される2価の官能基。 - 9.持続可能な開発目標(SDGs)
2015年9月の国連サミットで採択された「持続可能な開発のための2030アジェンダ」にて記載された2016年から2030年までの国際目標。持続可能な世界を実現するための17のゴール、169のターゲットから構成され、発展途上国のみならず、先進国自身が取り組むユニバーサル(普遍的)なものであり、日本としても積極的に取り組んでいる(外務省ホームページから一部改変して転載)。
研究チーム
理化学研究所 環境資源科学研究センター
ケミカルバイオロジー研究グループ
研修生 イスラム・アデル・アブデルハキム
(Islam Adel Abdelhakim)
研修生(研究当時) ファウジ・ビン・マフムード
(Fauze Bin Mahmud)
専任研究員 本山 高幸(もとやま たかゆき)
研究員 二村 友史(ふたむら ゆうし)
グループディレクター 長田 裕之(おさだ ひろゆき)
天然物生合成研究ユニット
ユニットリーダー 高橋 俊二(たかはし しゅんじ)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費補助金基盤研究(A)「人工知能を活用した抗真菌剤の開発研究(研究代表者:長田裕之)」、同新学術領域研究(研究領域提案型)「プロテオミクスをベースにした化学シグナル解析技術開発(研究代表者:長田裕之)」、およびエジプトと日本の教育パートナーシップ(EJEP)基金からの助成金などによる支援を受けて行われました。
原論文情報
- Islam A. Abdelhakim, Fauze Bin Mahmud, Takayuki Motoyama, Yushi Futamura, Shunji Takahashi, and Hiroyuki Osada, "Dihydrolucilactaene, a Potent Antimalarial Compound from Fusarium sp. RK97-94", Journal of Natural Products, 10.1021/acs.jnatprod.1c00677
発表者
理化学研究所
環境資源科学研究センター ケミカルバイオロジー研究グループ
研修生 イスラム・アデル・アブデルハキム(Islam Adel Abdelhakim)
専任研究員 本山 高幸(もとやま たかゆき)
グループディレクター 長田 裕之(おさだ ひろゆき)
 イスラム・アデル・アブデルハキム
イスラム・アデル・アブデルハキム
 本山 高幸
本山 高幸
 長田 裕之
長田 裕之
報道担当
理化学研究所 広報室 報道担当
お問い合わせフォーム
