理化学研究所(理研)生命医科学研究センター ゲノム解析応用研究チームの寺尾 知可史 チームリーダー(静岡県立総合病院 免疫研究部長、静岡県立大学 特任教授)、循環器ゲノミクス・インフォマティクス研究チームの伊藤 薫 チームリーダー、ファーマコゲノミクス研究チームの曳野 圭子 研究員、莚田 泰誠 チームリーダー、東京大学大学院新領域創成科学研究科 メディカル情報生命専攻の小井土 大 助教らの共同研究グループは、日本人の「冠攣縮性(かんれんしゅくせい)狭心症」を対象にした大規模なゲノムワイド関連解析(GWAS)[1]を行い、冠攣縮性狭心症の病態に関わる重要な疾患感受性領域(遺伝子座)[2]を同定しました。さらにその遺伝子領域の変異保有者でかつ基礎疾患として冠動脈疾患[3]がない人は、変異のない人に比べて将来的な急性心筋梗塞による死亡率上昇と関連する可能性を示しました。
本研究成果は、冠攣縮性狭心症を発症させる病態のさらなる解明と、新しい治療法や予防法の開発に貢献すると期待できます。
冠動脈疾患の中には心筋梗塞や狭心症などが含まれますが、さらに狭心症の中の一つの分類である冠攣縮性狭心症は、冠動脈が発作的に異常な収縮を起こすことで、心筋に虚血が生じてしまうものであり、発症には喫煙・飲酒などのほかに遺伝的要因も指摘されています。
今回、共同研究グループは、バイオバンク・ジャパン(BBJ)[4]に登録された約16万人のデータを対象に、世界初の冠攣縮性狭心症のGWASを行い、東アジア人に特異的でまれな疾患感受性領域を同定しました。加えて、その変異保有者は、基礎疾患として冠動脈疾患がないにもかかわらず将来的な急性心筋梗塞による死亡率の上昇と関連していました。
本研究は、科学雑誌『JAMA Cardiology』オンライン版(6月18日付:日本時間6月19日)に掲載されました。
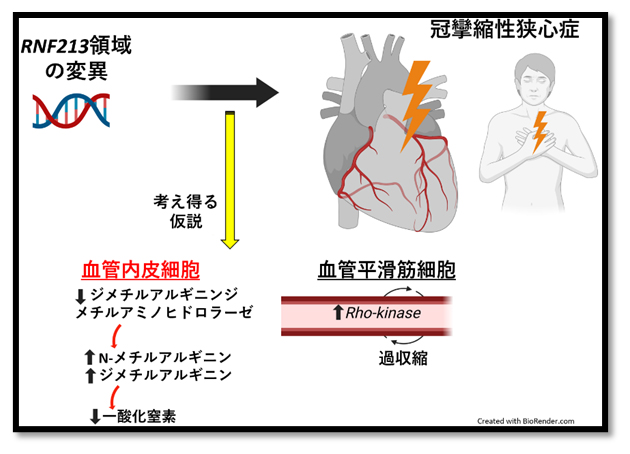
冠攣縮性狭心症の遺伝子解析で同定された領域から考え得る病態
背景
狭心症とは、心筋へ血液を供給する冠動脈が詰まりかけたり狭くなったりすることで発症します。「冠攣縮性狭心症」は、その狭心症の一種であり、冠動脈が発作的に過剰な収縮を起こしてしまう状態のことです。中には、血液の供給が途絶えることによる心筋梗塞、重症の不整脈、突然死など、重篤な合併症を引き起こすこともあります。以前は東アジア人に多いといわれていましたが、最近では、東アジア人以外でも東アジア人と同じくらいの頻度で起こっている可能性が示され、注目されています注1)。
冠攣縮性狭心症は病態がまだ完全には解明されておらず、発症には遺伝的要因も指摘されています。これまでの遺伝子解析では少人数による解析や遺伝子のターゲットを絞った解析が行われましたが、大規模なゲノムワイド関連解析(GWAS)は実施されていませんでした。
そこで共同研究グループは、バイオバンク・ジャパン(BBJ)に登録されている約16万人のデータを対象に大規模なGWASを行って、冠攣縮性狭心症の発症に関わる疾患感受性領域(遺伝子座)を探索し、さらにその変異を有する集団の長期的予後を調べました。
- 注1)Ong P, Athanasiadis A, Borgulya G, et al. Clinical usefulness, angiographic characteristics, and safety evaluation of intracoronary acetylcholine provocation testing among 921 consecutive white patients with unobstructed coronary arteries. Circulation. 2014;129:1723-30.
研究手法と成果
共同研究グループは、冠攣縮性狭心症患者に特徴的な遺伝的変異を網羅的に検出するため、BBJの登録者のうち、冠攣縮性狭心症患者群5,192人と対照群14万3,964人を対象に、世界でも最大規模となるGWASを行いました。
解析の結果、ゲノムワイド有意水準[5]を満たす、東アジア人に特異的でまれな疾患感受性領域(オッズ比[5]2.18、p=2.0×10-18)を同定しました(図1)。
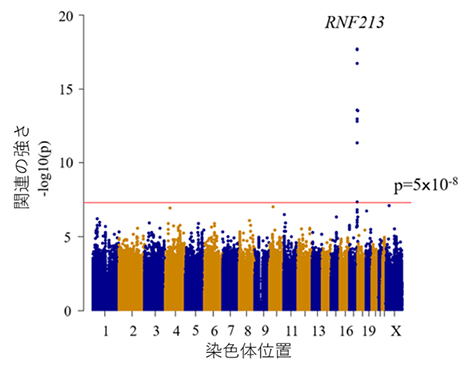
図1 冠攣縮性狭心症GWASのマンハッタンプロット
横軸は染色体位置、縦軸は解析対象となった全ゲノム領域のp値(有意確率)をプロットしたもの(「マンハッタンプロット」という)で、該当する染色体位置における関連の強さを示す。赤線がp値=5.0×10-8のゲノムワイド有意水準に該当する。冠攣縮性狭心症の疾患感受性領域として、東アジア人に特異的でまれな変異をRNF213遺伝子上に同定した。
同定した東アジア人に特異的でまれな疾患感受性領域は第17染色体におけるRNF213遺伝子上のミスセンス変異[6]であり、冠動脈疾患全体での既報のGWASでの関連性は示されていました注2)。今回、この変異が冠攣縮性狭心症に強い影響をもたらすことで、冠動脈疾患(冠攣縮性狭心症を除く)と冠攣縮性狭心症は、異なる病態を示している可能性が示唆されました(図2)。
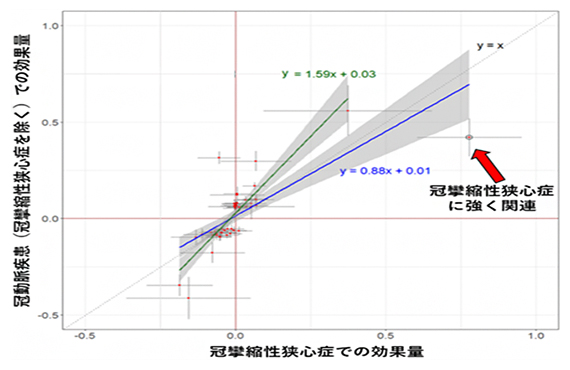
図2 冠攣縮性狭心症とそれ以外の冠動脈疾患の疾患GWASでの効果量(影響の強さ)の比較
赤点がそれぞれの冠動脈疾患関連領域を示す。赤点を横切る灰色の線は95%信頼区間を示す。円で囲まれて矢印で示した点がRNF213変異である。青線がRNF213変異を含む回帰線で、その95%信頼区間を灰色の領域で示す。緑の線がRNF213変異を含まない回帰線で、その95%信頼区間を灰色の領域で示す。RNF213変異のみが冠攣縮性狭心症に大きく影響していることが示された。
BBJ登録者の冠攣縮性狭心症患者群を二つのデータセットに分けて、GWASを行いました。それぞれのデータセットにおいて、第17染色体におけるRNF213遺伝子上に疾患感受性領域を同定しました(一つ目:オッズ比2.0、p=1.2×10-10、二つ目:オッズ比2.7、p=2.7×10-10)。さらに、追加のデータセットを用いたGWASにおいても(冠攣縮性狭心症528人と対照群9,900人)、同領域が同定されました(領域中の最小オッズ比4.0、p=1.8×10-10)。
また、RNF213遺伝子上のミスセンス変異は、性別や年齢に関係なく冠攣縮性狭心症に関連していることが分かりました。中でも、女性よりも男性に強く影響し、若いほど強く影響していました(図3)。この違いが、男女における冠攣縮性狭心症の罹患(りかん)率の差に影響している可能性や、冠攣縮性狭心症が他の冠動脈疾患と比較して低い年齢において発症することにも関係している可能性を示唆しています。
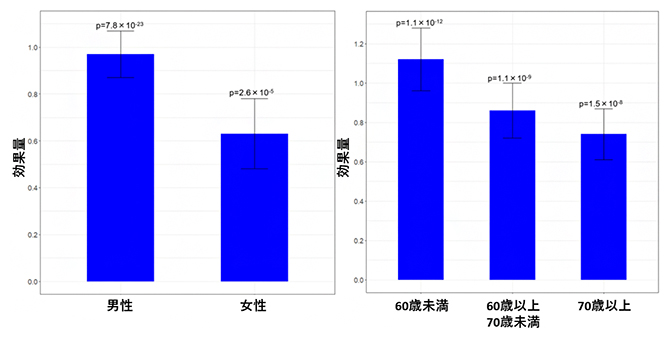
図3 RNF213遺伝子上のミスセンス変異の効果量の男女別・年齢別比較
横軸は対象群(左の図では性別ごと、右の図では年齢ごとに層別化)、縦軸はRNF213変異の効果量を示す。棒グラフ上の線は標準誤差を示し、その上にこの変異と対照群における関連を調べた解析結果のp値を示した。この変異は、男性が女性よりも大きな効果量で、低い年齢がより高い年齢層よりも大きな効果量であり、より強く影響していたことを示している。
本研究で同定されたRNF213遺伝子上のミスセンス変異は、もやもや病[7]の原因遺伝子として広く知られていることから、本研究結果に対するもやもや病の存在の影響も検討しました。その結果、冠攣縮性狭心症ともやもや病の合併症例数や、もやもや病の疾患感受性領域注3)を考慮した解析結果から、その可能性は低いことが示されました。
最後に、このRNF213遺伝子上のミスセンス変異を有する集団の長期的予後を調べたところ、ハザード比[8]が2.7の強さで、急性心筋梗塞で死亡する割合が有意に上昇していました(図4)。
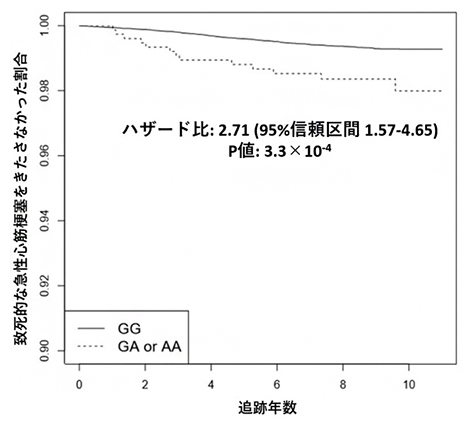
図4 RNF213遺伝子上のミスセンス変異を有する集団の急性心筋梗塞による死亡率
BBJに登録された、急性心筋梗塞により死亡した患者のうち、がんや心臓病で登録された患者を除外した、RNF213遺伝子上のミスセンス変異のリスクアレル(塩基のGがAになることで疾患のリスクが上がる遺伝子変異)を有する患者(ヘテロ型(GA)かホモ型(AA))と無い患者(野生型(GG))の生存曲線を示す。横軸は対象群の長期予後の追跡年数、縦軸は急性心筋梗塞による死亡をきたさなかった割合。Aアレルを有する群が点線で示され、有しない群が実線で示されている。Aアレルを有すると、ハザード比2.71で急性心筋梗塞による死亡率が上昇していた。
これらの結果から、RNF213遺伝子上のミスセンス変異が、それを有する集団の予後の予測因子となる可能性が示されました。
- 注2)Koyama S, Ito K, Terao C, et al. Population-specific and trans-ancestry genome-wide analyses identify distinct and shared genetic risk loci for coronary artery disease. Nat Genet. 2020;52:1169-1177.
- 注3)Duan L, Wei L, Tian Y, et al. Novel Susceptibility Loci for Moyamoya Disease Revealed by a Genome-Wide Association Study. Stroke. 2018;49:11-18.
今後の期待
今回の研究では、冠攣縮性狭心症の大規模ゲノムワイド関連解析によって、強い効果量を有する冠攣縮性狭心症の疾患感受性領域を同定しました。また、本領域と将来的な急性心筋梗塞による死亡率が大きなハザード比として関連していることが示されました。
冠攣縮性狭心症の方の中でも、本多型を持つ人は数十人に1人ですが、今後、冠攣縮性狭心症発症との関連が明らかになった遺伝子変異を介した発症メカニズムを解明することで、冠攣縮性狭心症に対する新しい治療法や予防法の開発に貢献できるものと期待できます。なお、本研究は基礎研究段階にあり、今後、臨床のエビデンスを積み重ねていく必要があります。
補足説明
- 1.ゲノムワイド関連解析(GWAS)
一つの遺伝的座位に、二つかそれ以上の頻度の高い異なるアレル(対立遺伝子)が存在する状態のことを遺伝的多型という。一つの塩基が他の塩基に変わる多型を、SNP(Single Nucleotide Polymorphism:一塩基多型)と呼ぶ。ゲノムワイド関連解析は形質に対する遺伝的関連を知るための手法であり、SNPを用いて解析するものが一般的である。形質(疾患のある/なしや検査値などの量的情報)を目的変数、SNPの量的情報や各種共変量を説明変数にしてモデル化し、SNPの関連を評価する。GWASはGenome-Wide Association Studyの略。 - 2.疾患感受性領域(遺伝子座)
疾患の発症に関連している染色体上の領域のこと。 - 3.冠動脈疾患
心臓の筋肉(心筋)に酸素や栄養を送る重要な血管である冠動脈が詰まったり狭くなったりし、酸素や栄養が届かなくなる疾患。心筋梗塞や狭心症があり、冠攣縮性狭心症は狭心症の一種。 - 4.バイオバンク・ジャパン(BBJ)
患者を対象とした生体試料のバイオバンクで、東京大学医科学研究所内に設置されている。理研が実験により取得した約20万人のゲノムデータを保有する。オーダーメイド医療の実現プログラムを通じて実施され、ゲノムDNAや血清サンプルを臨床情報とともに収集し、研究者へ試料やデータの提供を行っている。詳細はバイオバンク・ジャパンのウェブサイトを参照。 - 5.ゲノムワイド有意水準、オッズ比
GWASでは通常の有意水準である0.05を100万で割り、p値を5.0×10-8未満という厳しい判定基準を採用し、間違って有意であるという判定をしないように設定した独自の水準。オッズ比は発症リスクの大きさの指標であり、基準とするものに対して、発症するリスクが何倍に上がるかを表す。 - 6.ミスセンス変異
DNAの塩基配列が変化することでアミノ酸のコードが変化し、本来のアミノ酸ではないアミノ酸に置き換わったタンパク質が生成される変異。 - 7.もやもや病
日本で最初に発見され、日本人に多発する脳の血管に起きる疾患。脳に栄養を供給する血管が詰まることで周囲の細い血管が発達したもの。病名は、この異常な血管が、たばこの煙のようにもやもやして見えることに由来する。 - 8.ハザード比
リスクの指標の一つで、発症や死亡などのイベントが起こるまでの時間も加味したリスクの上昇を表す。
共同研究グループ
理化学研究所 生命医科学研究センター
ゲノム解析応用研究チーム
チームリーダー 寺尾 知可史(テラオ・チカシ)
(静岡県立総合病院 臨床研究部 免疫研究部長、静岡県立大学 薬学部 ゲノム病態解析講座 特任教授)
研修生(研究当時)小池 良直(コイケ・ヨシナオ)
(現 客員研究員)
上級技師 冨塚 耕平(トミヅカ・コウヘイ)
研修生(研究当時)伊藤 修司(イトウ・シュウジ)
(現 客員研究員)
上級研究員 劉 暁渓(リュウ・ギョウケイ)
研究員 石川 優樹(イシカワ・ユウキ)
循環器ゲノミクス・インフォマティクス研究チーム
チームリーダー 伊藤 薫(イトウ・カオル)
客員研究員 小山 智史(コヤマ・サトシ)
研究員 黒澤 亮(クロサワ・リョウ)
ファーマコゲノミクス研究チーム
チームリーダー 莚田 泰誠(ムシロダ・タイセイ)
研究員 曳野 圭子(ヒキノ・ケイコ)
基盤技術開発研究チーム
チームリーダー 桃沢 幸秀(モモザワ・ユキヒデ)
東京大学大学院新領域創成科学研究科 メディカル情報生命専攻
教授 鎌谷 洋一郎(カマタニ・ヨウイチロウ)
助教 小井土 大(コイド・マサル)
特任教授 森崎 隆幸(モリサキ・タカユキ)
自治医科大学分子病態治療研究センター 人類遺伝学研究部
教授 松村 貴由(マツムラ・タカヨシ)
研究支援
本研究は、日本医療研究開発機構(AMED)ゲノム医療実現バイオバンク利活用プログラム(ゲノム医療実現推進プラットフォーム・先端ゲノム研究開発)「先天的/後天的構造多型に着目した免疫/精神疾患病態解明に関する研究開発」、同ゲノム医療実現バイオバンク利活用プログラム(ゲノム研究バイオバンク)「利活用を目的とした日本疾患バイオバンクの運営・管理」、同難治性疾患実用化研究事業「シングルセル統合ゲノミクス解析が解き明かす強皮症の病態基盤の開発」、同革新的がん医療実用化研究事業「体細胞モザイクのがん発症および予後因子としての意義解明の開発」、同免疫アレルギー疾患実用化研究事業「先天的・後天的ゲノム情報と臨床情報を用いた関節リウマチの層別化基盤の構築」、同ゲノム医療実現バイオバンク利活用プログラム「炎症性関節炎の統合ゲノミクス解析」、日本学術振興会(JSPS)科学研究費助成事業基盤研究(A)「エンハンサーの遺伝的発現制御の解明による免疫疾患解析(研究開発代表者:寺尾知可史、20H00462)」、同若手研究「冠攣縮性狭心症に対する世界初のゲノムワイド関連解析による遺伝要因の同定(研究代表者:黒澤亮、22K16090)」の助成を受けて行われました。
原論文情報
- Keiko Hikino, Satoshi Koyama, Kaoru Ito, Yoshinao Koike, Masaru Koido, Takayoshi Matsumura, Ryo Kurosawa, Kohei Tomizuka, Shuji Ito, Xiaoxi Liu, Yuki Ishikawa, Yukihide Momozawa, Takayuki Morisaki, Yoichiro Kamatani, The Biobank Japan Project, Taisei Mushiroda, Chikashi Terao., "RNF213 Variants, Vasospastic Angina, and Risk of Fatal Myocardial Infarction", JAMA Cardiology, 10.1001/jamacardio.2024.1483
発表者
理化学研究所
生命医科学研究センター ゲノム解析応用研究チーム
チームリーダー 寺尾 知可史(テラオ・チカシ)
(静岡県立総合病院 免疫研究部長、静岡県立大学 特任教授)
循環器ゲノミクス・インフォマティクス研究チーム
チームリーダー 伊藤 薫(イトウ・カオル)
ファーマコゲノミクス研究チーム
研究員 曳野 圭子(ヒキノ・ケイコ)
チームリーダー 莚田 泰誠(ムシロダ・タイセイ)
東京大学大学院新領域創成科学研究科 メディカル情報生命専攻
助教 小井土 大(コイド・マサル)
 寺尾 知可史
寺尾 知可史
 伊藤 薫
伊藤 薫
 曳野 圭子
曳野 圭子
 莚田 泰誠
莚田 泰誠
 小井土 大
小井土 大
報道担当
理化学研究所 広報室 報道担当
お問い合わせフォーム
東京大学大学院新領域創成科学研究科 広報室
Tel: 04-7136-5450
Email: press [at] k.u-tokyo.ac.jp
静岡県立総合病院 総務課
Tel: 054-247-6111 / Fax: 054-247-6140
Email: sougou-soumu [at] shizuoka-pho.jp
静岡県立大学 広報・企画室
Tel: 054-264-5130
Email: koho [at] u-shizuoka-ken.ac.jp
※上記の[at]は@に置き換えてください。
