新型コロナウイルスワクチンの実用化で医薬メッセンジャーRNA(mRNA)が注目されています。これは、目的のタンパク質の情報を持つmRNAを人工的に合成し、投与することで病気の治療や予防をしようというものです。この医薬mRNAの品質を管理するためには、有効成分であるRNA分子の特性を評価する方法が求められてきました。2023年、そのための新しい方法が理研と東京都立大学の共同研究により開発されました。今後、急速に進むと考えられる医薬mRNAの普及に貢献すると期待されています。
ワクチンや医薬品に利用が期待されるmRNA
2023年のノーベル生理学・医学賞の授賞はmRNAワクチンの実用化を可能にした功績に対するものだったことは記憶に新しい。このmRNAはタンパク質の合成で働く分子で、細胞の核の中で遺伝子DNAの情報である塩基配列をコピーして合成され(転写)、核外のリボソームに遺伝子の情報を運ぶ。リボソームでは、mRNAが鋳型となってタンパク質が合成される(翻訳)。
コロナウイルスのタンパク質をつくるように設計した人工mRNAを脂質ナノ粒子にくるんだmRNAワクチンを投与すると、mRNAは体内で直接作用するのではなく、細胞に取り込まれたmRNAから合成されたタンパク質が効果を発揮する。細胞の中の遺伝子発現のメカニズムを利用した全く新しいタイプのワクチンだ。
mRNAワクチンは、塩基配列さえあればパンデミックでも迅速に対応でき、ヒトのゲノムに組み込まれることがなく安全性も高いので、感染症ワクチンとして有望と考えられている。新型コロナウイルス感染症では、最初の感染者発見からわずか1年でワクチンが実用化され、次々と登場する変異株にも対応できた。すでに感染症ワクチンのほか、がんや代謝疾患など140品目以上の医薬品の治験が行われている。
転写後の「修飾」が重要
実は、真核生物のmRNAは転写された塩基配列のままではなく、さまざまな化学反応で「修飾」された成熟型のmRNAとして働く。これらの修飾はmRNAの安定性や機能に関わる。図1に示す「キャップ」、「ポリ(A)」や「メチル化」が代表例である。
1970年代からmRNAを用いるワクチンや医薬品の研究は始まっていたが、投与したmRNAが強い炎症反応を起こすことが実用化の大きなネックだった。この問題を解決したのが2023年にノーベル賞を受賞したカリコとワイスマンによる発見だった。彼らはいくつかの人工的な修飾を導入したmRNAが炎症を抑えることを示した。修飾されたmRNAがワクチン実現の最も重要なブレークスルーの一つなのだ。
「転写後修飾が重要なことは知られていましたが、構造や動態を解析する研究はあまり進んでいませんでした。その点に着目し、研究しているところでパンデミックが起こったのです。これまでの研究の成果を基にワクチンのmRNA解析法を開発したら、短期間で社会貢献できるのではないかと考えました」と中山 洋 専任研究員は振り返る。

図1 医薬mRNAの構造
医薬mRNAは5′末端にはキャップ、3′末端にはポリ(A)と呼ばれる構造などで修飾された成熟型として設計・合成される。これらは細胞内でのmRNAの分解を防ぎ、翻訳を促進するなどの働きがある。
開発した定量法でmRNAの品質を評価
商業生産された新型コロナウイルスワクチンには、断片化したものや不完全な構造のmRNAが多く含まれていることが指摘されていた。このことは、ワクチンの薬効に直接影響し、不完全な分子や副生成物が副反応などを引き起こすこともあり得る。けれども、mRNAの複雑な構造を分析し、品質を評価する決定的な方法はなく、各構造に適した複数の手法を組み合わせて行っているのが現状だ。
「mRNAの各構造を一つ一つ別の方法で解析するので、非常に煩雑だし、定量性も低いのです」。そこで中山 専任研究員らが開発したのは、液体クロマトグラフィー質量分析を用いた品質評価法だ。この方法によって、mRNAを高感度で直接定量できるようになる。
まず、ワクチンと同じ配列の、安定同位体で標識したmRNAを合成した。そのmRNAを酵素で断片化し、液体クロマトグラフィーで分離したのち、質量分析で検出した。中山専任研究員らが開発したソフトウェアで解析したところ、このmRNAの純度が高いことや設計通りの構造を持っていることが分かり、参照mRNAとして利用できることが示された。続いて、参照mRNAと医薬mRNAを1対1で混ぜ合わせたものを、同様に解析し、比較した。
解析した結果を最終的にバブルチャートで比較すると(図2)、参照mRNAと同じ構造のmRNA断片なら、横軸では同じ位置にプロットされる。ただ、参照mRNAは、安定同位体で標識しているのでわずかに質量の差があるため、縦軸の位置もわずかにずれて、バブルが二重になる。一方、参照mRNAと異なる不完全な構造を持つ断片は単独でプロットされる。このことを利用すると、一目で、医薬mRNAと参照mRNAを比較できる。キャップ構造やポリ(A)などの解析もできるので、有効成分がどれくらい含まれているかすぐに分かり、簡単に品質を評価できるのだ。
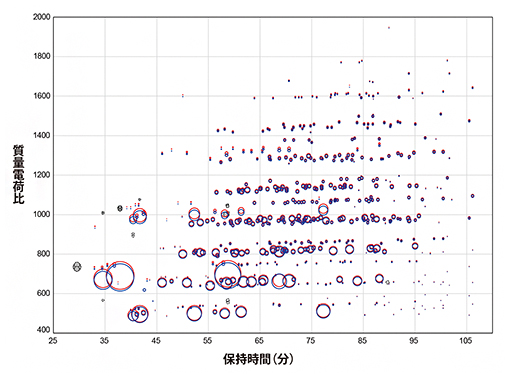
図2 安定同位体で標識した参照mRNAと医薬mRNAの比較
バブルチャートはmRNA断片の三つの異なる属性を比較できるグラフで、この場合横軸は疎水性、縦軸は質量、バブルの大きさは量を示す。青いバブルは医薬mRNAを、赤いバブルは参照mRNAから得られた断片の結果で、バブルの重なりから医薬mRNAの質や量が参照mRNAとほぼ同じことが示された。
広く使ってもらいたい
現状では実際のワクチンを入手できず、自分たちで合成したワクチンと同じ構造のmRNAで分析することになった。また、そのほかの医薬mRNAモデルも解析し、新しい方法でmRNAの品質を評価できることが示された。
「新型コロナウイルス感染症では、特例承認制度でワクチンが承認されました。この段階では、従来の方法による特性評価が認められましたが、今後はより厳密な規格とその評価が求められるでしょう。また、医薬mRNAの普及を見据えると、私たちの方法はとても有効だと思います」
この方法は、医薬mRNAの特性評価ばかりでなく、基礎から応用まで幅広い学術研究にも利用でき、基礎生物学の発展にも貢献できる。「この方法を広く使ってもらいたい」と検討を重ねている。
(取材・構成:佐藤 成美/撮影:盛 孝大/制作協力:サイテック・コミュニケーションズ)
関連リンク
- 2023年2月8日東京都立大学プレスリリース「医薬mRNAの新たな評価方法の開発 ~COVID-19などのウイルス性疾患や遺伝性疾患の予防・治療医薬の品質評価に有効~」
この記事の評価を5段階でご回答ください

