2011年6月24日
独立行政法人 理化学研究所
プロファイリングで、抗がん剤候補物質の作用機序を解明
-独自のプロテオームプロファイリングシステムで薬剤標的を迅速同定-
ポイント
- 作用既知薬剤のプロテオーム情報から、作用未知薬剤の効果をプロファイリングで予測
- 植物由来新規誘導体BNS-22がDNAトポイソメラーゼIIを標的にして働きを阻害
- BNS-22がトポ毒型と違った触媒阻害型の新抗がん剤として期待
要旨
独立行政法人理化学研究所(野依良治理事長)は、独自の薬剤プロテオーム※1プロファイリングシステムを活用して、新規抗がん剤候補物質の作用を解明することに成功しました。これは、理研基幹研究所(玉尾皓平所長)ケミカルバイオロジー研究基盤施設の長田裕之施設長、川谷誠研究員と、京都大学医学部附属病院の木村晋也講師(現佐賀大学医学部教授)、前川平教授らとの共同研究による成果です。
2005年、木村晋也講師らは、ブラジルの熱帯雨林に自生するオトギリ草※2の成分の1つに抗がん作用があることを発見しました。その後、この成分を基に60種類以上の誘導体を化学合成して、より強力なBNS-22※3の創製に成功しました。しかし、その抗がん作用の仕組みは長らく不明のままでした。
研究グループは、細胞が薬剤の作用に応じて固有のタンパク質変動を誘導する性質を利用して、作用既知薬剤の膨大なプロテオーム情報を基に、作用未知薬剤の効果をプロファイリングにより予測するプロテオームプロファイリングシステムを独自に構築し、長年蓄積してきた成果を2010年にデータベースとして公表しました(2010年5月28日プレスリリース)。
このシステムを利用して、BNS-22を処理したヒトがん細胞であるHeLa細胞※4のプロテオームデータを、抗がん剤やシグナル伝達阻害剤を含む40種類以上の既存薬のプロテオームデータベースと統合してプロファイリングした結果、BNS-22がDNAトポイソメラーゼII※5と呼ぶ酵素を標的にしていることを予測しました。実際に、試験管や細胞レベルでこの予測どおりBNS-22が、酵素の働きを特異的に阻害していることを見いだしました。
DNAトポイソメラーゼIIは、がん治療の有望な創薬ターゲットの1つであるため、今回の成果を応用することでBNS-22が新たな抗がん剤になると期待されます。また、このプロテオームプロファイリングシステムを用いることで、薬剤の作用標的・作用機序を迅速かつ高精度に予測できることから、創薬研究に広く活用されると期待されます。
本研究成果は、米国の科学雑誌『Chemistry & Biology』(6月24日号)に掲載されます。
背景
私たちは病気にかかると薬を処方されますが、その薬の候補物質はしばしば自然界から見いだされます。実際、広く活用されている抗生物質や抗がん剤には天然由来物質、あるいはその誘導体が多く含まれています。
2005年、京都大学医学部附属病院の木村晋也講師(現佐賀大学医学部教授)らは、ブラジルの熱帯雨林に自生するオトギリ草(Calophyllum brasiliense)の茎から抽出した成分の1つ、GUT-70※3(分子量382.45、図1左)に抗がん作用があることを発見しました。その後、この知見を基に60種類以上の誘導体を化学合成し、より強力な抗がん作用を有するBNS-22(分子量407.46、図1右)の創製に成功しました。しかし、その抗がん作用の仕組みは長らく不明のままでした。
薬の候補物質を実際に臨床の治療薬として開発していくには、その候補物質が生体内でどのような標的に作用し、どのような機序で効果を発揮するのかといった仕組みを明らかにすることが必要です。これは創薬研究で最も重要なステップの1つですが、同時に非常に多くの時間と労力が費やされます。
このため研究グループは、薬剤の生体内標的分子を予測するプロテオームプロファイリングシステムを独自に構築してきました。このシステムでは処理した薬剤の作用に応じて、細胞が固有のタンパク質変動を誘導する性質を利用します。具体的にはまず作用既知の多種の薬剤について、タンパク質変動を網羅的に解析したデータを取得し、データベース化します。次に、解析対象である作用未知の薬剤についてタンパク質変動データを取得後、このデータベースと統合してプロファイリング解析し、その薬剤の作用標的・作用機序を予測します。この手法は、(1)薬剤の効果を細胞内の反応の直接の担い手であるタンパク質全体の変動でとらえること、(2)プロテオーム解析で最も時間と労力が費やされる個々のスポット(タンパク質)の同定を必要とせず、各スポットのタンパク質の変動だけを専用の装置で自動的に定量化することという特徴により高精度かつ迅速に薬剤の標的を予測できることが可能になります。
今回、研究グループはこのシステムを駆使してBNS-22の作用機序の解明に挑みました。
研究手法
ヒトがん細胞であるHeLa細胞にBNS-22を添加し、37℃で18時間培養しました。その後、細胞をばらばらにして可溶化し、細胞内の全タンパク質を蛍光色素で標識した後、二次元電気泳動法でタンパク質を分離し蛍光スキャナーで読み取って定量化しました(蛍光標識二次元ディファレンス電気泳動解析法※6、図2ステップ1)。このプロテオームデータを、抗がん剤やシグナル伝達阻害剤を含む40種類以上の既存薬のプロテオームデータと統合し、階層的クラスター解析法※7でBNS-22の作用をプロファイリングしました(図2ステップ2)。また、生化学的手法や分子細胞生物学的手法を駆使して、推定した効果を試験管あるいは細胞レベルで実験的に検証しました(図2ステップ3)。
研究成果
薬剤プロテオームプロファイリングの結果、BNS-22はDNAトポイソメラーゼII阻害剤※8である既存のICRF-193と同じクラスターに分類できました(図2ステップ2)。つまり、BNS-22は、細胞内でDNAトポイソメラーゼIIをターゲットにしていることが予測できました。DNAトポイソメラーゼIIは、2本鎖DNAの両方を切断し、再結合する酵素で、複製や転写の際に生じるDNAのねじれ、染色体の凝縮や分離時におけるDNA間のもつれを解消する働きを担っています。実際に、BNS-22がこの酵素の働きを阻害するか否かを検討した結果、BNS-22はDNAトポイソメラーゼIIの2つのアイソフォームαとβの両方の酵素活性を阻害し、その結果がん細胞の増殖を抑制して細胞死を導くことが分かりました(図3)。さらに、BNS-22が、既存のICRF-193とは異なる作用機序でDNAトポイソメラーゼIIの働きを阻害していることを明らかにしました。
今後の期待
DNAトポイソメラーゼIIは、がん治療の有望な創薬ターゲットの1つです。実際、エトポシドやテニポシドなどのDNAトポイソメラーゼII阻害剤は抗がん剤として広く臨床で用いられています。しかし、これらの薬剤は骨髄抑制、二次性白血病の発症、薬剤耐性といった副作用が問題となっています。DNAトポイソメラーゼII阻害剤は、その作用機序の違いにより「トポ毒」型と「触媒阻害」型に分類されます。エトポシドやテニポシドなどは「トポ毒」型、ICRF-193やBNS-22は「触媒阻害」型です。「触媒阻害」型薬剤の抗がん剤開発研究はこれまで十分に行われていません。そのため今後研究が進んでいくと、BNS-22が作用機序の異なる新しいタイプの抗がん剤候補になると期待されます。また、独自に構築した薬剤プロテオームプロファイリングシステムは、新規有用物質の作用標的・作用機序を高精度に、かつ迅速に予測するツールとして、今後創薬研究に広く活用されることが期待されます。
発表者
理化学研究所
基幹研究所 ケミカルバイオロジー研究基盤施設
施設長 長田 裕之(おさだ ひろゆき)
研究員 川谷 誠(かわたに まこと)
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.プロテオーム(proteome)
プロテオームはタンパク質を表すproteinと全体を表す-omeを組み合わせた造語であり、細胞内で発現している(発現する可能性をもつ)全タンパク質のことを指す。 - 2.オトギリ草
オトギリソウ科オトギリソウ属の多年生植物。草本から木本まであり、熱帯地方から温帯地方に広く分布する。 - 3.GUT-70とBNS-22
GUT-70はオトギリ草( Calophyllum brasiliense)の茎から抽出された成分の1つで、抗がん作用を有する天然化合物である。BNS-22はGUT-70の合成誘導体で、GUT-70よりも強い抗がん作用を示す。 - 4.HeLa細胞
世界で初めて樹立されたヒトの細胞株(生体外で一定の性質をもって長期間培養できる細胞)。子宮頸がん由来の細胞で、世界中でさまざまな研究に利用されている。名前は、患者である黒人女性の名前(Henrietta Lacks)に由来する。 - 5.DNAトポイソメラーゼII
DNAトポイソメラーゼは、複製や転写などによるDNA内の過剰なねじれ、染色体の凝縮や分離時におけるDNA間のもつれを解消する(トポロジーを変える)酵素の総称である。2本鎖DNAの一方だけを切断する酵素をDNAトポイソメラーゼI、両方とも切断する酵素をDNAトポイソメラーゼIIという。ヒトDNAトポイソメラーゼIIにはαとβの2つのアイソフォームが存在する。DNAトポイソメラーゼIIは、細胞増殖に不可欠であり、増殖が盛んながん細胞では抗がん剤の重要な標的の1つとなる。 - 6.蛍光標識二次元ディファレンス電気泳動解析法(2D-DIGE)
プロテオーム解析を行う方法の1つで、タンパク質を蛍光色素で標識して二次元電気泳動で分離する手法である。この方法は、2種類のタンパク質試料を異なる蛍光試薬であらかじめ標識してから混合し、1枚のゲルで泳動することで、2種類の試料内の相対的タンパク質量を精密に比較できることが特長である。 - 7.階層的クラスター解析法
クラスター解析は、複数の変数を用いて類似度を計算して分類する手法。階層的クラスター解析では、試料間でどれくらい両者が似ているかを示す距離を計算して階層的にグループ化する方法で、結果は樹形図で示される。 - 8.DNAトポイソメラーゼII阻害剤
DNAトポイソメラーゼIIの機能を阻害する薬剤を指す。阻害する作用機序の違いにより、「トポ毒」型と「触媒阻害」型に分類される。「トポ毒」型は、細胞に処理するとDNAダメージを誘発するのに対し、「触媒阻害」型は、DNAダメージを誘発しないのが特徴である。「トポ毒」型にはエトポシドやテニポシドなどが知られており、抗がん剤として使用されている。「触媒阻害」型にはICRF化合物類などが知られているが、「触媒阻害」型薬剤の抗がん剤開発は十分に進んでいない。
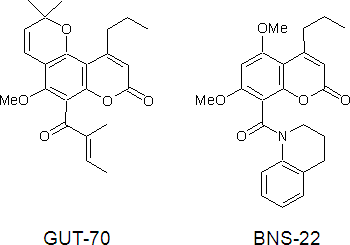
図1 GUT-70とBNS-22の化学構造
GUT-70は抗がん作用を有する植物由来天然化合物。BNS-22はGUT-70の合成誘導体の1つで、GUT-70よりも強い抗がん作用を示す。

図2 プロテオームプロファイリングによるBNS-22の作用標的同定の流れ
ステップ1:蛍光標識二次元ディファレンス電気泳動解析法(2D-DIGE)を用いて、BNS-22を処理した細胞のプロテオームデータを取得する。
ステップ2:BNS-22のプロテオームデータを参照化合物のプロテオームデータベースと統合し、階層的クラスター解析によりBNS-22の作用をプロファイリングする。BNS-22は細胞内でDNAトポイソメラーゼIIを標的にしていることが予測された。ヒートマップ中の赤色は増加したタンパク質、緑色は減少したタンパク質を示す。
ステップ3:ステップ2で得られた予測を実験的に検証する。
BNS-22は試験管および細胞レベルでDNAトポイソメラーゼIIの機能を特異的に阻害していることが判明した。
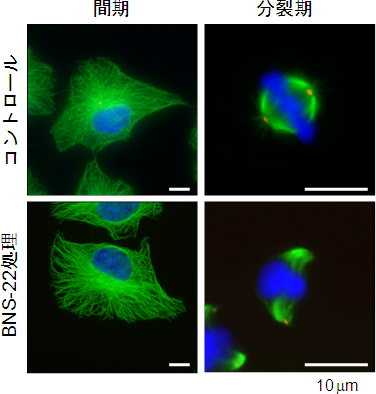
図3 BNS-22による紡錘体形成異常
(緑:β-チューブリン、赤:γ-チューブリン、青:DNA)
BNS-22(10μM)をHeLa細胞に12時間処理したときの細胞の様子。コントロールの分裂期細胞では赤道面に染色体が並び左右対称の紡錘体を観察。一方、BNS-22を処理した分裂期細胞では、染色体の凝縮や分離に重要な役割を担うDNAトポイソメラーゼIIの機能が阻害されることにより、染色体の配置が不均一で紡錘体が折れ曲がったような形成異常が誘導される。
