2014年2月7日
独立行政法人理化学研究所
独立行政法人科学技術振興機構
卵子の「異型ヒストン」がiPS細胞の作製を促す
―核移植に似たメカニズムを介しiPS細胞の作製効率を約20倍アップ―
ポイント
- 卵子に多量にある異型ヒストンTH2AとTH2BがiPS細胞作製を促進
- 異型ヒストンを用いたiPS細胞作製は、核移植に似たメカニズムを介する
- 異型ヒストンは受精後の父方遺伝子の活性化に関与
要旨
理化学研究所(理研、野依良治理事長)は、アミノ酸配列が通常のヒストンと異なる「異型ヒストン[1]」をiPS細胞(人工多能性幹細胞)[2]の作製に用いると、核移植[3]に似たメカニズムを介して、iPS細胞の作製効率が約20倍上昇することを明らかにしました。これは、理研石井分子遺伝学研究室の品川敏恵専任研究員と石井俊輔上席研究員、および理研バイオリソースセンター、理研放射光科学総合研究センター、東京大学、九州大学、筑波大学による共同研究グループの成果です。
京都大学の山中伸弥教授らにより、ES細胞(胚性幹細胞)に多く発現する4つの転写因子(山中因子)を体細胞に発現させると、体細胞が初期化(リプログラミング)され、iPS細胞が作製できることが示されました。しかし、iPS細胞は、ES細胞に比べ多くのタイプの細胞に分化する能力(多分化能)に劣ることが課題となっています。一方、核移植によるクローンの作製は、山中因子とは異なるリプログラミング因子が卵子に存在することを示唆しています。しかし、卵子のリプログラミング因子の実体には不明な点が多くあります。
共同研究グループは、ヒストンが遺伝子発現に重要な役割を果たすことから卵子のリプログラミング因子の候補として卵子内に多量に存在する「TH2A」と「TH2B」の2つの異型ヒストンに注目しました。これらの因子と山中因子を用いてiPS細胞を作製した結果、iPS細胞の作製が山中因子だけの場合に比べて早く進み、かつ効率が約20倍上昇しました。TH2AとTH2Bを用いたiPS細胞作製について解析したところ、核移植に似たメカニズムが働いていることが示されました。
今回の成果から、TH2AとTH2Bは、核移植とiPS細胞作製を橋渡しするものと考えられます。核移植では全能性細胞[4]が形成されるため、TH2AとTH2Bを用いることで、より完全な多分化能を持つiPS細胞作製につながると期待できます。
本研究成果は、科学技術振興機構の戦略的創造研究推進事業 チーム型研究(CREST)「胚細胞ヒストンによるリプログラミング機構」(研究代表者:石井俊輔)の助成を受けており、米国の科学雑誌『Cell Stem Cell』2014年2月6日号に掲載されます。
背景
京都大学の山中伸弥教授らにより、ES細胞(胚性幹細胞)に多く発現する山中因子と呼ばれる4つの転写因子(Oct3/4、Sox2、Klf4、c-Myc)を体細胞に発現させると、体細胞が初期化(リプログラミング)され、iPS細胞が作製できることが示されました。しかしiPS細胞は、ES細胞に比べると多くのタイプの細胞に分化する能力(多分化能)に劣り、ES細胞のような完全な多分化能を持つiPS細胞作製が課題となっています。
体細胞のリプログラミングを最初に実証したのが、核移植によるクローンの作製です。この方法では、体細胞の核を取り出し、核を取り除いた未受精卵内に移植することによって、核内の遺伝子発現パターンが未分化な細胞のパターンにリプログラムされます。核移植ではクローン個体ができることから、完全な多分化能を持つ細胞が作製されます。核移植は、山中因子とは異なるリプログラミング因子が卵子に存在することを示していますが、そのリプログラミング因子の実体については不明な点が多くあります。これまで共同研究グループは、卵子に多く存在する、どの因子がリプログラミングに関与するかを研究してきました、今回さらに研究を進め、卵子に多量に存在する異型ヒストンによるリプログラミングおよびiPS細胞作製の効率化を解析しました。
研究手法と成果
1)卵子に多量に存在する異型ヒストンがiPS細胞作製を促進
共同研究グループは、ヒストンというタンパク質が遺伝子発現に重要な役割を果たすことから卵子のリプログラミング因子の候補として2つの異型ヒストン「TH2A」と「TH2B」に注目しました。ヒストンはDNAを巻き付けてヌクレオソーム[1]という構造を形成し、遺伝子の発現を制御しています(図1)。TH2AとTH2Bは、通常のヒストンであるH2A、H2Bとアミノ酸配列が10%程度異なり、卵子に多く存在します。
共同研究グループは、TH2AとTH2Bを山中因子と一緒に体細胞で発現させてみました。その結果、iPS細胞の作製が山中因子だけの場合に比べ、より早く進み、かつ効率が約20倍上昇しました(図2)。また、TH2AとTH2Bを用いると、山中因子のうちOct3/4とKlf4だけで、iPS細胞を作製できることを見出しました(図3)。山中因子だけの場合に比べて高効率でiPS細胞が作製できる理由として、TH2AとTH2Bを含むヌクレオソームは、通常のヌクレオソームに比べ緩い構造を取り、転写が誘導され易いからだと推定できます(図4)。
2)異型ヒストンを用いたiPS細胞作製は、核移植に似たメカニズムを介する
核移植によるクローン作製は大変効率が低いのですが、「X染色体不活性化に関与するXist RNA欠損細胞の核を用いると、効率が良くなること」が、理研バイオリソースセンター遺伝工学基盤技術室の小倉淳郎室長らのグループにより2010年に報告されています注)。TH2AとTH2Bを用いたiPS細胞の作製の場合にも、Xist RNA欠損細胞を用いると、iPS細胞作製効率が上がることが分かりました。これは、異型ヒストンを用いたiPS細胞作製は、核移植に似たメカニズムで起こっていることを示しています。これらのことからTH2AとTH2Bは、核移植とiPS細胞作製を橋渡しするものと考えられます(図5)。
3)異型ヒストンは受精後の父方遺伝子の活性化に関与
共同研究グループは、TH2AとTH2Bを欠損させた変異マウスを作製し、発生過程の解析を行いました。その結果、TH2AとTH2Bは受精卵に伝わり、受精後の父方遺伝子の活性化に関与し、初期発生に重要な役割を果たすことが示されました(図6)。この結果は、核移植によるクローン作製が発生過程と類似のプロセスを経るという考えと一致します。
注)理研プレスリリース「マウス体細胞クローンの産子出生効率が10倍近くも改善」(2010年9月17日)
今後の期待
核移植によるクローニングでは全能性細胞が形成されるので、卵子特異的なリプログラミング因子の利用は、より完全な多分化能を持つiPS細胞作製につながると期待できます。
原論文情報
- Shinagawa T, Takagi T, Tsukamoto D, Tomaru C, Huynh LM, Sivaraman P, Kumarevel T, Inoue K, Nakato R, Katou Y, Sado T, Takahashi S, Ogura A, Shirahige K, Ishii S.
"Histone Variants Enriched in Oocytes Enhance Reprogramming to Induced Pluripotent Stem Cells" Cell Stem Cell 14, 2014
発表者
理化学研究所
上席研究員研究室 石井分子遺伝学研究室
上席研究員 石井 俊輔(いしい しゅんすけ)
報道担当
独立行政法人理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
独立行政法人科学技術振興機構 広報課
Tel: 03-5214-8404 / Fax: 03-5214-8432
補足説明
- 1.異型ヒストン、ヌクレオソーム
ヒストンはDNAを巻き付けて、細胞核内にコンパクトに納める役割を果たすタンパク質。ヒストンにはH1、H2A、H2B、H3、H4の5種類があり、このうちH2A、H2B、H3、H4の4種類(コアヒストンと呼ばれている)が2つずつ集まってヒストン八量体を形成し、この八量体の周りにDNAが巻き付きヌクレオソームという構造になる。ヌクレオソームは、全ての真核生物における共通構造(クロマチン)の構成単位である( 図1参照)。異型ヒストン(ヒストンバリアントとも呼ばれる)は、通常のヒストンとはアミノ酸配列が少し異なる。 - 2.iPS細胞(人工多能性幹細胞)
体細胞に数種類の遺伝子を導入して作製された細胞で、ES細胞(胚性幹細胞)のように多くの細胞に分化できる多分化能と、自己複製能を有する。京都大学の山中伸弥教授らのグループにより最初に作製された。 - 3.核移植
動物の体細胞核を未受精卵に移植することによりクローンを作成する方法。核移植による最初のクローンは、1962年にケンブリッジ大学(英国)のジョン・ガードン博士によりアフリカツメガエルから作られた。1997年には、ロスリン研究所(スコットランド)のイアン・ウィルムット博士らによってクローン羊ドリーが作られ、1998年には、ハワイ大学の柳町隆造教授らによって、マウスからクローンが作製された。 - 4.全能性細胞
あらゆる細胞に分化することができる、つまり完全な1個体を形成できる能力を持つ細胞。体を形成する3つの胚葉(内胚葉、中胚葉、外胚葉)と共に、胎盤のような胚体外組織に分化する能力を持つ。動物では受精卵とその後に数回分裂した状態の細胞が全能性を有する。一方ES細胞は、3つの胚葉(内胚葉、中胚葉、外胚葉)に分化する能力を持つが、胎盤のような胚体外組織には分化できないため、多能性細胞と呼ばれる。
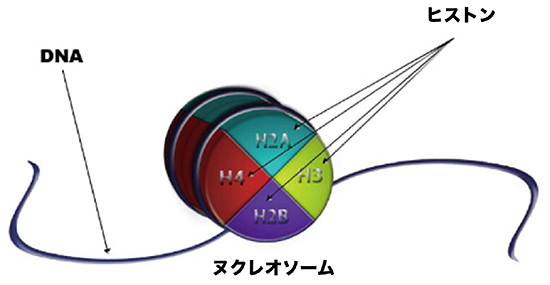
図1 ヒストン、ヌクレオソーム、DNAの関係
H2A、H2B、H3、H4の4種類のヒストンが2つずつ集まってヒストン八量体を形成し、この八量体の周りにDNAが巻き付き、ヌクレオソームという構造になる。
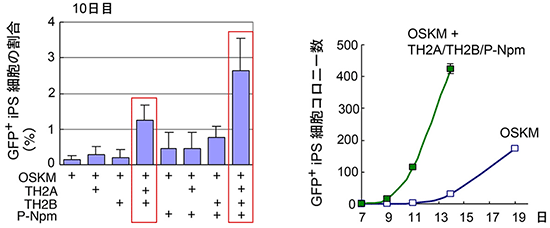
図2 異型ヒストンによるiPS細胞作製の促進
- 左: 2つの異型ヒストンを山中4因子(OSKM)と一緒に発現させると、iPS細胞作製が約10倍促進された。さらにヒストンをヌクレオソームに運ぶ役割を持つヒストンシャペロン、ヌクレオプラスミン(P-Npm)、を一緒に加えると、iPS細胞作製が約20倍促進された。
- 右: 2つの異型ヒストン、ヌクレオプラスミンを加えると、山中4因子(OSKM)だけの場合に比べ、より短時間でiPS細胞が形成された。
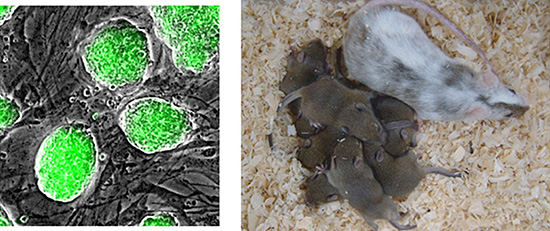
図3 異型ヒストンを用いて作製したiPS細胞とこのiPS細胞で作製したマウス
- 左: TH2AとTH2B、そして山中因子のうちOct3/4とKlf4だけを用いて作製したiPS細胞。
- 右: 右上は、このiPS細胞を用いて作製したキメラマウス。左下は、キメラマウスから生まれたマウス(左下)。このiPS細胞が全ての組織に分化する能力を持つことを示している。
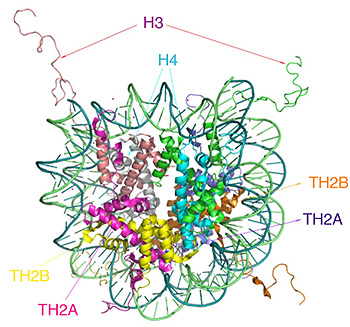
図4 TH2A/TH2Bを含むヌクレオソームの構造モデル
TH2A/TH2Bを含むヌクレオソームの構造モデルを作製し、通常のヒストンH2A/H2Bを含むヌクレオソームの構造と比較すると、前者は不安定な構造を取ることが示唆された。これにより、TH2A/TH2Bを含むヌクレオソームは緩い構造を取り、転写を誘導し易いと推定される。
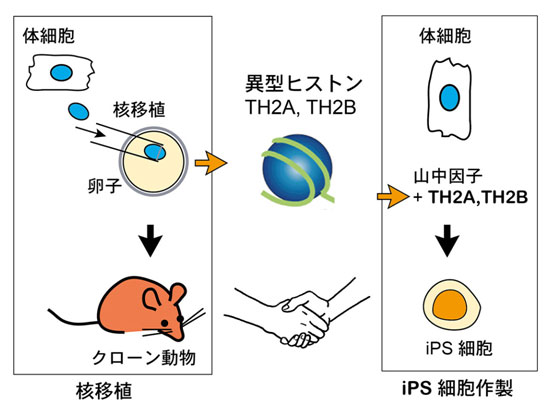
図5 異型ヒストンTH2AとTH2Bによる核移植とiPS細胞作製の橋渡し
卵子に多く存在する異型ヒストンTH2AとTH2BがiPS細胞作製を促進することが示された。これらの異型ヒストンは核移植とiPS細胞作製の橋渡しをするものと考えられる。
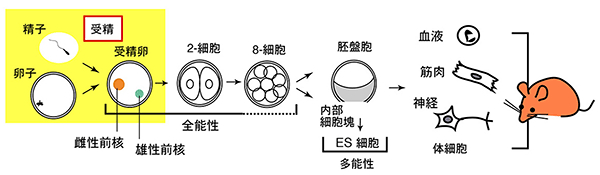
図6 受精後の父方遺伝子の活性化
精子中では、DNAはヒストンの代わりにプロタミンに巻き付き、よりコンパクトに折り畳まれている。精子と卵子が受精してできる受精卵では、精子由来の父方遺伝子は雄性前核に存在し、この固い構造が解きほぐされるが、そのメカニズムはまだ不明な点が多い。今回の実験により、異型ヒストンTH2AとTH2Bが受精卵に伝わり、受精後の父方遺伝子の活性化に関与し、初期発生に重要な役割を果たすことが示された。
