2014年9月19日
独立行政法人理化学研究所
独立行政法人日本原子力研究開発機構
106番元素シーボーギウム(Sg)のカルボニル錯体の合成に成功
-Sgが周期表第6族元素に特徴的な化学的性質を持つことを実証-
ポイント
- 超重元素の有機金属錯体を初合成
- Sgより重い超重元素の有機金属錯体の化学合成や溶液化学研究への展開に期待
- 原子力に重要な超ウラン元素の化学的性質の本質的理解に向けた大きな一歩
要旨
理化学研究所(理研、野依良治理事長)と日本原子力研究開発機構(原子力機構、松浦祥次郎理事長)は、106番元素「シーボーギウム(Sg)」の有機金属錯体(カルボニル錯体[1])の化学合成に成功しました。また、その揮発性に関する化学データから、Sgが周期表の第6族元素に特徴的な化学的性質を持つことを実証しました。これは、ドイツのヘルムホルツ研究所マインツのイーヴン・ジュリア博士、重イオン研究所のヤクシェフ・アレクサンダー サブグループリーダー、マインツ大学のデュルマン・クリストフ教授、理研仁科加速器研究センター(延與秀人センター長)RI応用チームの羽場宏光チームリーダー、原子力機構先端基礎研究センター(前川禎通センター長)超重元素研究グループの浅井雅人研究主幹、佐藤哲也研究員らの国際共同研究グループ[2]の成果です。
原子番号103を超える非常に重い元素は超重元素と呼ばれ、重イオン加速器を利用した核融合反応で人工的に合成されます。Sgは1974年に発見されて以来、周期表上で第6族元素のタングステン(W)の下に並べられてきました。しかし、Sgの化学的性質については、化学実験に利用できるSgの同位体265Sgの生成率が1時間に1個程度と極めて低く寿命が10秒程度と短いこと、また、従来の実験手法では265Sg合成時にできる大量の副反応生成物が265Sgの同定を妨害することなどから、ほとんど明らかにされていませんでした。
国際共同研究グループは、理研RIビームファクトリー(RIBF)の重イオン線形加速器「RILAC」[3]で得られる重イオンビームを用いて265Sgを合成し、気体充填型反跳分離器「GARIS」[4]を用いて質量分離した後、Sgのカルボニル錯体の化学合成とガスクロマトグラフ法による化学分析を試みました。その結果、Sgが第6族元素のモリブデン(Mo)やWと同様に揮発性の高いカルボニル錯体を形成し、二酸化ケイ素表面に対する吸着エンタルピー[5]もMoやWのヘキサカルボニル錯体と同程度であることを明らかにしました。さらに、相対論的分子軌道計算[6]との比較から、その錯体がヘキサカルボニル錯体「Sg(CO)6」であることを明らかにし、Sgが第6族元素に特徴的な化学的性質を持つことを高い信頼度で実証しました。
本研究成果は、米国の科学雑誌『Science』(9月19日号)に掲載されます。
背景
原子番号103を超える非常に重い元素は超重元素と呼ばれ、全て重イオン加速器を利用した核融合反応によって人工的に合成されます(図1)。超重元素の領域では、原子核が持つ大きな核電荷によって電子軌道が大きく変化し(相対論効果[7])、化学的性質に影響を与えることが理論的に予測されています。新しく発見された元素がこれまで知られている周期性に従った性質を示すのか、あるいは、強い相対論効果の影響で思いがけない性質が出現するのかなどについて、実験的に検証することは興味深い研究テーマです。しかし、超重元素の生成率は極めて低く、生成されても寿命は1分間以下と短いため、一度の化学実験にわずか1個の原子しか取り扱うことができません。そのため、超重元素では原子核の存在は確認されているものの、化学的性質はほとんど分かっていません。超重元素の化学は、究極の微量元素分析といわれています。
化学実験に利用できる長寿命の超重元素の同位体は、加速器で高エネルギーに加速した酸素(18O)やネオン(22Ne)などの重イオンビームを、標的のキュリウム(248Cm)などのアクチノイド元素に衝突させることで起きる核融合反応によって合成されます。これまでの超重元素の化学実験では、核融合反応により標的から反跳分離[8]された超重元素をガスジェット法[9]によって、直接、気体または液体クロマトグラフ装置に運んで分析を行っていました。また、不安定な原子核のアルファ壊変[10]や自発核分裂壊変[11]を検出することで、超重元素を同定していました。
しかし、これまでの手法では、超重元素とともに大量の副反応生成物が化学分析装置に混入するため、放射線計測による超重元素の同定が妨害され、研究対象にできる元素が限られ、化学実験系も自由に構築できませんでした。図2aに従来のガスジェット法を用いて、106番元素シーボーギウム(Sg)の同位体265Sgを合成したときのアルファ粒子[10]のエネルギースペクトルを示します。図に示されているように、副反応生成物であるポロニウム(Po)同位体からの大量のアルファ粒子により、265Sgの同定が妨害されます。このようにSgよりも重い超重元素の化学研究では実験手法に問題点が多く、革新的な解決策が切望されていました。
理研と原子力機構を中心とする日本の核化学研究グループは、次世代の超重元素化学研究を進展させるため、理研の重イオン加速器施設「RIビームファクトリー(RIBF)」において、重イオン線形加速器「RILAC」と気体充填型反跳分離器「GARIS」を利用した新しい超重元素化学分析システムの開発を進めてきました(図3)。
GARISは、ビームの原子核や、ビームによってはじき出された標的の原子核、ビームと標的の原子核の一部が融合した不要な生成物などの副反応生成物を取り除き、目的の原子核だけを効率よく確実に分離できる装置です。同研究グループは従来のガスジェット法の欠点を解決するため「GARISガスジェット法」を開発しました(図3)。113番元素などの新元素の探索実験に用いられてきたGARISを化学実験前に利用することにより、超重元素を極めて低い放射線バックグラウンドの下で化学分析することができるようになります。また、これまで不可能であった化学反応が適用可能となります。同研究グループは2012年、Sgの化学研究に必須である同位体265Sgを生成し、世界に先駆けて化学実験室に取り出し、合成核反応データや壊変データを取得することに成功しています。GARISガスジェット法を用いて265Sgを化学実験室に運び計測したアルファ粒子のエネルギースペクトルが図2bです。主な副反応生成物であるPoの大部分が除去され、265Sgと265Sgが壊変する過程でつくられる261Rf(104番元素ラザホージウム)と257No(102番元素ノーベリウム)のピークが明確に観測されています。
Sgは1974年に発見されて以来、元素の周期表上で第7周期の第6族元素として並べられてきました(図1)。しかし上で述べた実験の困難さのために、Sgの気相化学実験としては、単純な無機化合物であるオキシ塩化物とオキシ水酸化物を対象とした2例が報告されているだけで、詳細な化学的性質は分かっていませんでした。同じ6族元素のクロム(Cr)、モリブデン(Mo)やタングステン(W)は、いずれも揮発性の高いヘキサカルボニル錯体を形成することが知られています。Sgが周期表の周期性に従って、MoやWと同じヘキサカルボニル錯体Sg(CO)6を形成するかどうかを確認すれば、Sgが6族元素であることが、より信頼性のおけるものとなります。相対論的分子軌道計算では、SgはWと同様に揮発性の高いヘキサカルボニル錯体Sg(CO)6(図4)を形成することが予測されています。
研究手法と成果
国際共同研究グループは、GARISガスジェット法の利点を最大限に生かして、Sgのカルボニル錯体の化学合成とその気相化学実験を行いました。実験の概念図を図5に示します。実験に用いる265Sgは、RILACで加速した22Ne6+イオンビームを248Cm標的に照射して合成しました。248Cm標的から反跳分離された265Sgイオンを、GARISの4つの電磁石によってビームや副反応生成物から質量分離し、続いてガスジェットチャンバー内でヘリウム(He)と一酸化炭素(CO)の混合ガス中に捕獲しました。ここで、Sgのカルボニル錯体を化学合成し、GARISガスジェット法によって数秒のうちにテフロン管を通して化学実験室に引き出しました。カルボニル錯体の化学分析は、32対のシリコン半導体検出器と液体窒素冷却装置からなる低温ガスクロマトグラフ装置「COMPACT[12]」を用いて行いました。また、MoとWの同位体(87,88Mo、164W)についても、マグネシウムイオン(24Mg7+)ビームをそれぞれ亜鉛(natZn、nat:天然同位体組成)とサマリウム(144Sm)の標的に照射して合成し、Sgと同様にカルボニル錯体の化学合成と化学分析を行いました。
17日間にわたる加速器実験で、265Sgの壊変過程で放出されるアルファ粒子または自発核分裂片を計18個観測することに成功しました。図6に265Sgのカルボニル錯体のシリコン半導体検出器に対する吸着分布図を、87,88Moと164Wのカルボニル錯体の分布図と比較して示します。265Sg、87,88Moと164Wのカルボニル錯体は、同じ表面温度の検出器に吸着することが分かります。これにより、SgがMoやWと同様な揮発性の高いカルボニル錯体を形成することが明らかになりました。モンテカルロシミュレーション[13]により、カルボニル錯体の検出器表面の二酸化ケイ素(SiO2)に対する吸着エンタルピーを解析したところ、Sgのカルボニル錯体の吸着エンタルピーが、MoとWのヘキサカルボニル錯体の吸着エンタルピーと等しいことが分かりました。さらに、今回得られた吸着エンタルピーは、相対論的分子軌道計算による理論計算値とよく一致しており、Sgがヘキサカルボニル錯体Sg(CO)6を形成していると結論づけました。このことから、Sgが第6族元素に特徴的な化学的性質を持つことを高い信頼度で実証しました。
超重元素の気相化学実験は、これまでビームがガスジェットチャンバー内を貫く従来ガスジェット法の制限から、単純な無機化合物あるいは単体を対象としたものに限られていましたが、今回GARISガスジェット法を用いて、超重元素領域では初めての有機金属化合物Sg(CO)6の化学合成に成功しました。これまで調べられてきた無機化合物中のSgは高い酸化状態(6+)ですが、Sg(CO)6中の酸化状態は0で、Sgの電子状態や化学結合に関する新しい情報を得ることができました。
今後の期待
国際共同研究グループは今後、Sg金属とCO分子の結合の強さを調べるため、Sg(CO)6錯体の熱分解実験を行い、相対論的分子軌道計算と比較しながら相対論効果が化学結合に与える影響などをさらに検証していく予定です。今回のSg(CO)6合成の成功により、さらに重い107番元素ボーリウム(Bh)や108番元素ハッシウム(Hs)のカルボニル錯体の化学研究も視野に入ってきました。また、GARISによる質量分離とSg(CO)6の気相化学実験を組み合わせ、超低バックグラウンドでの新しいSg同位体の探索や詳細な原子核分光研究の展開も期待できます。
GARISガスジェット法により、従来の実験法では困難だったSg以上の新しい元素の化学実験、超重元素の有機金属錯体の化学合成や液体シンチレーション検出器を用いた超重元素の溶液化学研究などへの展開も期待できます。また、このような超重元素の化学的性質の研究は、相対論的分子軌道計算の精度を向上させ、原子力に重要な超ウラン元素の化学的性質のより深い理解に貢献することも期待できます。
原論文情報
- J. Even, A. Yakushev, Ch.E. Düllmann, H. Haba, M. Asai, T.K. Sato, H. Brand, A. Di Nitto, R. Eichler, F.L. Fan, W. Hartmann, M. Huang, E. Jäger, D. Kaji, J. Kanaya, Y. Kaneya, J. Khuyagbaatar, B. Kindler, J.V. Kratz, J. Krier, Y. Kudou, N. Kurz, B. Lommel, S. Miyashita, K. Morimoto, K. Morita, M. Murakami, Y. Nagame, H. Nitsche, K. Ooe, Z. Qin, M. Schädel, J. Steiner, T. Sumita, M. Takeyama, K. Tanaka, A. Toyoshima, K. Tsukada, A. Türler, I. Usoltsev, Y. Wakabayashi, Y. Wang, N. Wiehl, S. Yamaki, "Synthesis and detection of a Seaborgium carbonyl complex". Science, 2014, doi: 10.1126/science.1255720
発表者
理化学研究所
仁科加速器研究センター 応用研究開発室 RI応用チーム
チームリーダー 羽場 宏光(はば ひろみつ)
独立行政法人日本原子力研究開発機構
原子力科学研究部門 先端基礎研究センター 超重元素研究グループ
サブリーダー 塚田 和明(つかだ かずあき)
お問い合わせ先
独立行政法人理化学研究所
仁科加速器研究推進室
Tel: 048-467-9451 / Fax: 048-461-5301
独立行政法人日本原子力研究開発機構
原子力科学研究部門 先端基礎研究センター 研究推進室
Tel: 029-282-6980 / Fax: 029-282-5927
報道担当
独立行政法人理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
独立行政法人日本原子力研究開発機構
広報部 報道課長 中野 裕範(なかの ひろのり)
Tel: 03-3592-2346 / Fax: 03-5157-1950
補足説明
- 1.カルボニル錯体
一酸化炭素(CO)が配位した遷移金属錯体。周期表の第6族元素であるクロム(Cr)やモリブデン(Mo)、タングステン(W)は、COが6分子配位したヘキサカルボニル錯体を形成する。 - 2.国際共同研究グループ
ヘルムホルツ研究所マインツ(ドイツ)、重イオン研究所(ドイツ)、マインツ大学(ドイツ)、理化学研究所、日本原子力研究開発機構、ベルン大学(スイス)、ポールシェラー研究所(スイス)、近代物理研究所(中国)、広島大学、九州大学、新潟大学、カリフォルニア大学バークレー校(米国)、ローレンスバークレー国立研究所(米国)、埼玉大学。 - 3.重イオン線形加速器「RILAC」
RILACは RIKEN Liner ACceleratorの略。高周波電場を用いて、ウランまでのあらゆる元素の重イオンを直線的に加速する加速器。線形加速器では、多数のチューブ型電極が空洞の中に直線上に並べられている。電極の長さと高周波の周波数は、電極間の電場の向きがイオンの到達時間に同期して変わるように設計され、電極間を通過するたびにイオンが加速される。RILACは、重イオンを加速するために、低い周波数(18~45MHz)で運転できるようになっており、また多種のイオンに対応するため周波数を変えることができる(可変周波数構造)。通常の線形加速器はパルス運転であるが、RILACは連続運転ができるため、平均ビーム強度が非常に高い。 - 4.気体充填型反跳分離器「GARIS」
GARISは GAs-filled Recoil Ion Separatorの略。重イオン核融合反応で合成した目的の原子核を、入射ビームや副反応生成物から、高効率・高分離能で分離、収集する装置。ヘリウムガスの充填により、目的とする原子核が標的からどのようなイオン価数で飛び出してきても、効率良く収集することができる。 - 5.吸着エンタルピー
気体状態の分子や原子がある物質表面に吸着する際に生じるエネルギー変化。通常、1モル(mol)当たりのエネルギー変化である[kJ/mol]を単位として表す。ガスクロマトグラフ実験で取得される物理量で、化合物や原子の揮発性の度合いを示す。 - 6.相対論的分子軌道計算
相対論的な電子運動の記述を取り入れた分子軌道計算。分子における一電子波動関数(分子軌道)を計算し、分子の最安定構造やエネルギーを求める。 - 7.相対論効果
超重元素のような重い原子では、中心にある原子核の正電荷が大きくなり、負電荷をもつ電子との相互作用が非常に大きくなる。すると原子核の近くにあるs電子やp電子(内殻電子)の速度は光速に近づき、相対論効果によって電子の質量が増大しその結果軌道半径が収縮する。一方、d電子やf電子(外殻電子)の軌道半径は、内殻軌道の収縮により原子核の正電荷が遮蔽され、反対に大きくなる。軽い元素でも相対論効果は見られるが、原子番号が大きい元素ほどこの効果は顕著に現れる。このように化学結合に関与する原子価電子の軌道が大きく変化し、超重元素は他の同族の元素とは異なる化学的性質を示すことがある。 - 8.反跳分離
原子核反応の結果生成した原子核は、運動エネルギー(反跳エネルギー)を持ち標的物質から飛び出す。この効果を利用して標的物質から同位体を分離することを反跳分離という。 - 9.ガスジェット法
原子核反応の結果標的から反跳分離された原子核をヘリウムなどの気体中で捕獲し、ジェット気流にのせて迅速かつ連続的に標的チャンバーの外に取り出す手法。しばしば反跳原子核を塩化カリウムなどのエアロゾルに吸着させ、これを気流にのせて効率良く搬送する。 - 10.アルファ壊変(α壊変)、アルファ粒子
不安定な原子核の放射壊変の1つ。アルファ粒子(ヘリウム4の原子核で原子番号2、質量数4)を放出してより安定な原子核に壊変する。この壊変の結果、原子番号が2、質量数が4小さい原子核に変化する。核種に固有なアルファ壊変の寿命とアルファ粒子のエネルギーを測定することにより、265Sgと265Sgがアルファ壊変する過程でつくられる261Rfと257Noを明確に同定できる。 - 11.自発核分裂壊変
不安定な原子核の放射壊変の1つ。とくに原子番号の大きな原子核にみられ、自発的に2つ以上の原子核に分裂する壊変。 - 12.COMPACT
COMPACTは Cryo- Online Multidetector for Physics And Chemistry of the Transactinidesの略。超重元素の物理・化学研究のための低温ガスクロマトグラフ検出器のこと。超重元素の放射壊変の検出と気相化学分離を行うため、32対のシリコン半導体検出器でガスクロマトグラフの流路がつくられている。検出器には、室温から液体窒素温度までの温度勾配をかけ、超重元素(またはその化合物)の揮発性を調べることができる。重イオン研究所(ドイツ)を中心とする研究グループによって開発された。 - 13.モンテカルロシミュレーション
乱数をモデルの変数に入れて模擬実験を何度も繰り返し、近似解を求める計算手法。超重元素のガスクロマトグラフ実験の解析において、カラム内を移動する気体分子や原子の様子をモンテカルロシミュレーションすることにより、カラム表面に対する吸着エンタルピーを得ることができる。
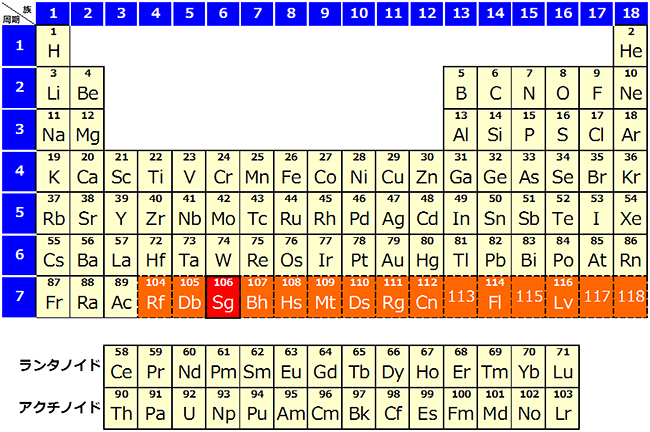
図1 元素の周期表(2014年9月現在)
オレンジ色で示されている104番以降の元素は、周期表上にそれぞれ並べられているが、化学実験の困難さのため信頼性の高い化学データはほとんど得られていない。今回、国際共同研究グループは、106番元素Sgの化学実験を行い、Sgが第6族元素に特徴的な化学的性質を持つことを高い信頼度で実証した。
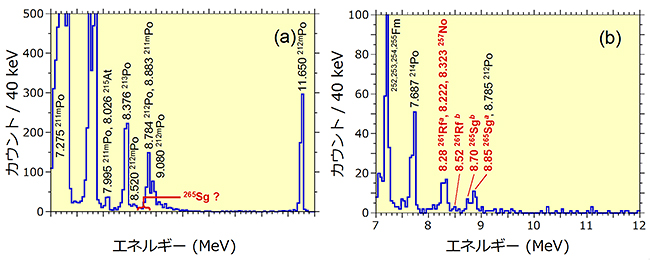
図2 265Sg合成時におけるアルファ粒子のエネルギースペクトル
- (a) 従来のガスジェット法を用いて取得したアルファ粒子のエネルギースペクトル。副反応生成物からの大量のアルファ粒子のため、265Sgのアルファ粒子を同定できない。
- (b) GARISガスジェット法を用いて取得したアルファ粒子のエネルギースペクトル。副反応生成物であるポロニウム(Po)同位体がGARISによって分離除去され、265Sgとその壊変生成物261Rfと257Noのピークが明確に観測されている。214Po(7.687MeV)と212Po(8.785MeV)のピークは、それぞれ大気中に含まれる天然放射性核種222Rn、220Rnの娘核で、核反応生成物ではない。
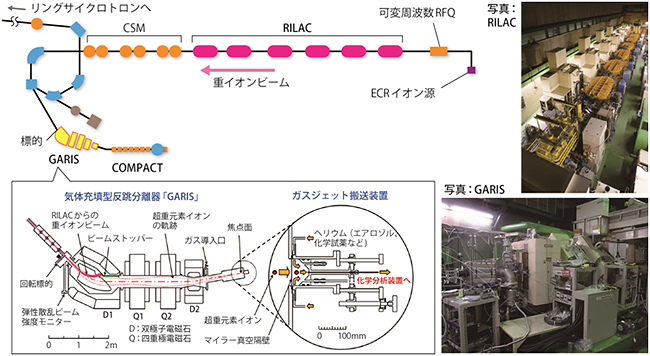
図3 超重元素化学分析システムとGARISガスジェット法の概念図
ECRイオン源から引き出した重イオンビームを、可変周波数RFQとRILAC、CSMによって光速の10%の速度まで加速し、標的に照射すると核融合反応が起こる。気体充填型反跳分離器「GARIS」で核融合反応により生成される多量な副反応生成物を除去し、目的の原子核だけを焦点面に導く。その後、GARISに結合したガスジェット搬送装置内で化学試薬と反応させ、目的の揮発性化合物を化学合成した後、低温ガスクロマトグラフ検出器「COMPACT」に運んで、化学的性質を調べる(図5参照)。
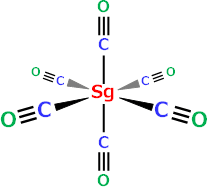
図4 106番元素シーボーギウム(Sg)のヘキサカルボニル錯体Sg(CO)6
相対論的分子軌道計算によって、Sgは周期表第6族元素のモリブデン(Mo)やタングステン(W)と同様に、一酸化炭素分子(CO)が6分子配位したヘキサカルボニル錯体を形成することが予測されている。
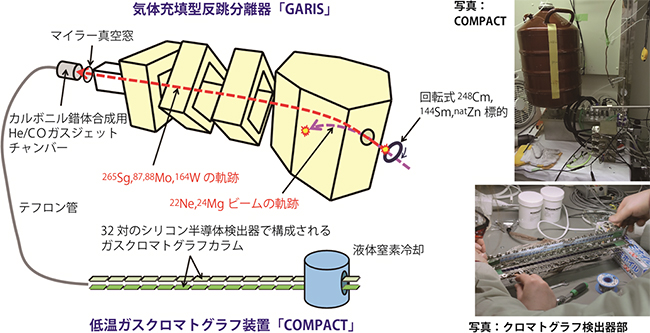
図5 実験の概念図
標的から反跳分離された265Sgイオンを、GARISの4つの電磁石によってビームや副反応生成物から質量分離し、続いてガスジェットチャンバー内でヘリウム(He)と一酸化炭素(CO)の混合ガス中に捕獲する。ここで、Sgのカルボニル錯体を化学合成し、GARISガスジェット法によって数秒のうちにテフロン管を通して化学実験室に運ぶ。カルボニル錯体の気相化学分析を低温ガスクロマトグラフ装置「COMPACT」を用いて行う。
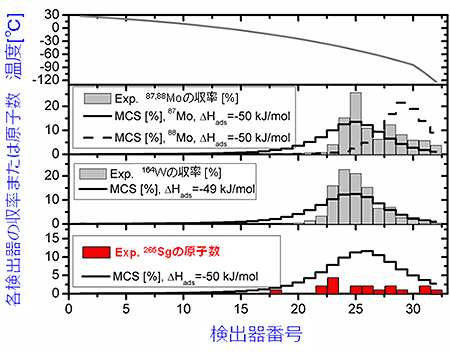
図6 シリコン半導体検出器の温度分布図と87,88Mo、164Wおよび265Sgのカルボニル錯体の吸着分布図
265Sgのカルボニル錯体の検出器に対する吸着分布図を、87,88Moと164Wのカルボニル錯体の分布図と比較して示す。265Sgのデータは、一酸化炭素ガスの流量と濃度が異なる複数の実験の結果を積算したもので、幅広い吸着分布となっている。265Sg、87,88Moと164Wのカルボニル錯体は、同じ表面温度の検出器に吸着することが分かる。また、モンテカルロシミュレーション(MCS)により、カルボニル錯体の検出器表面の二酸化ケイ素(SiO2)に対する吸着エンタルピーを解析したところ、Sgのカルボニル錯体の吸着エンタルピーが、MoとWのヘキサカルボニル錯体の吸着エンタルピーと等しいことが分かった。
