理化学研究所(理研)生命機能科学研究センター集積バイオデバイス研究チームの田中陽チームリーダー、産業技術総合研究所(産総研)バイオメディカル研究部門次世代メディカルデバイス研究グループの永井秀典研究グループ長らの共同研究グループは、タンパク質のアルブミン[1]を原料として、シリコーンゴム[2]の鋳型で型取りすることにより、細胞培養用の微小デバイスを簡単に作製することに成功しました。
本研究成果は、微小デバイス開発のための工学的理解にとどまらず、微小デバイスを用いた細胞培養により、微小環境が細胞に与える影響や、細胞と細胞接着基材表面のタンパク質との相互作用の理解に貢献すると期待できます。
今回、共同研究グループは、「細胞パターニング[3]」用のデバイスを作製するにあたり、真空吸引を利用してさまざまな溶液の鋳型への流れ込み方について調べた結果、鋳型に流れ込む溶液の量は溶液の粘性には依存せず、多様な溶液を使用できることが分かりました。さらに、産総研が開発した「架橋アルブミン」水溶液を用いたところ、1日以内に細胞パターニング用の微小デバイスが作製でき、そのデバイスは7日間の細胞培養に耐えられることが分かりました。
本研究は、科学雑誌『PLOS ONE』(5月20日付:日本時間5月21日)に掲載されます。

架橋アルブミンによる細胞パターニング
背景
細胞生物学において細胞集団の空間的な配置は、細胞集団の形態形成や組織機能の発現に関わる重要な要因として知られています。このため、細胞培養皿の表面など、細胞が接着する基材表面において、化学的な表面処理などにより、細胞が接着する部分と接着しない部分に区分けし、細胞の接着エリアを制御する「細胞パターニング」という手法がよく用いられます。
田中陽チームリーダーらは、生体高分子の一種で、海藻の寒天から精製されるアガロース[4]などの水溶液を用いた細胞パターニング手法をこれまでにも開発してきました注1-2)。これらの手法は、硬貨や自動車部品を作る際に用いられる「鋳造」という方法を応用し、どこでも簡単に作れるものです。シリコーンゴムの表面に深さ1mm以下の細かな溝を設けた「鋳型」を作り、そこにアガロース水溶液を流し込んだ後、鋳型を取り外すと、アガロースが鋳型の形に成型されます。これを細胞培養に使うと、アガロースで覆われた部分には細胞が接着しないため、アガロースで覆われた所とそうでない所が区分けされ、アガロースで覆われていない所だけに細胞を接着させることができます。
共同研究グループは今回、材料がシリコーンゴムの鋳型にどのように流れていくのかを詳しく調べ、さらに細胞パターニングのための新しい材料を検討しました。
- 注1)2017年4月6日プレスリリース「どこでも微小構造体」で幹細胞の分化パターンを解析」
- 注2)2017年12月21日プレスリリース「細胞個性をハイスループット解析」
研究手法と成果
共同研究グループは、フォトリソグラフィーと呼ばれる半導体製造に使われる手法を応用し、シリコーンゴムに細長い微小な溝を彫りました。溝が下になるようにして、シリコーンゴムを容器上に置き、真空中に1時間ほど置くと、シリコーンゴムに溶け込んでいる気体分子を取り除くことができます。そして、再び大気圧に戻すと、気体分子がシリコーンゴムに溶け込みますが、これによりシリコーンゴムで囲まれた空間が真空になることが知られています。この真空を利用して、粘性が異なる溶液を、さまざまなサイズのシリコーンゴムの溝に吸引させました(図1A)。このとき溶液が溝に流れ込む様子を観察し、単位時間あたりに流れ込む溶液の量を算出しました(図1B-C)。
解析の結果意外にも、粘性が高いドロドロした液体であっても、水のようにサラサラした液体と同じように溝の中に吸引できる一方で、溝の高さや幅などのサイズが流量を大きく左右することが分かりました(図1D-E)。これは、粘性に関係なく、多様な溶液が使用可能であること、流量はシリコーンゴムによる気体の吸引量が支配的であり、シリコーンゴムに囲まれた領域のサイズが大きいほど吸引量が平均的に増えることを示しています。さらに、シリコーンゴムの気体吸引を考慮したモデルを構築し、数値シミュレーションによって、実際の液体の流量を再現することに成功しました(図1C)。
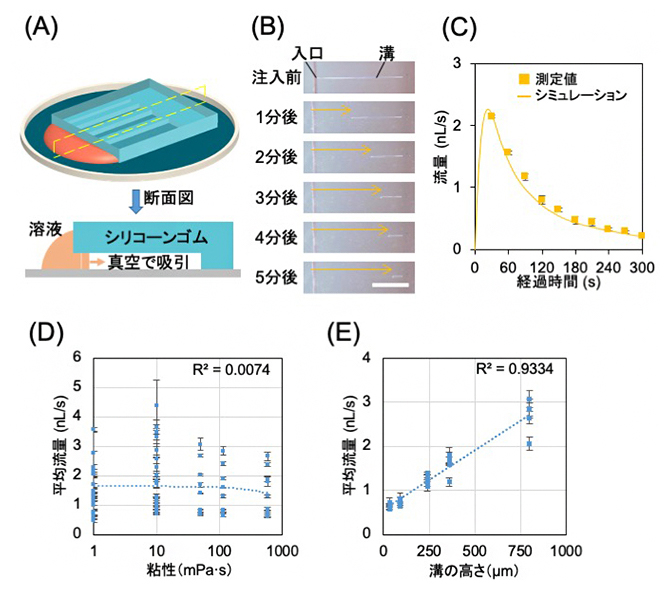
図1 シリコーンゴム鋳型に流れ込む溶液の解析
- (A)溶液導入の原理。真空吸引することで、溶液をシリコーンゴムで作った溝に導入する。
- (B)真空吸引によって、溶液が溝に流れ込む様子の経時変化。白いスケールバーは5mm。
- (C)実験で得られた流量とシミュレーションによって示された流量の経時変化。シミュレーション結果は、実際の流量を再現した。
- (D)溶液の粘性と流量の関係。粘性と平均流量は相関しなかった。
- (E)溝の高さと流量の関係。溝の高さが高いほど、鋳型に流れ込む量が高いことが分かった。
次に、どのような材料が細胞パターニングに適しているかを検討しました。注目したのは、産総研で開発された「架橋アルブミン」というタンパク質をベースにした材料です。血液中に多く含まれるタンパク質であるアルブミンは、一般的に水に溶けやすく、細胞培養の際に用いられる培養液に溶けてしまうため、細胞培養用デバイスの材料には不向きです。これに対して、化学処理によって複数のアルブミン分子を架橋させた架橋アルブミン水溶液は、いったん乾燥させると水に溶けない固形の材料に加工することができます。そこで、シリコーンゴムの鋳型に架橋アルブミン水溶液を流し込み乾燥させれば、培養液中でも安定して使用できる細胞培養用デバイスが作製できると考えました。
実験の結果、架橋アルブミン水溶液をシリコーンゴムの鋳型に流し込み、真空吸引後大気圧に戻し、溶液が乾燥した後鋳型を取り外すことで、1日以内に細胞培養用デバイスを作製できることが分かりました(図2A-C)。これまで、溶液の乾燥に3日以上かかっていたアガロース水溶液を用いた方法よりも、迅速にデバイスの準備ができます。
実際に、作製した架橋アルブミン製細胞培養用デバイスを用いて、細胞パターニングを行ったところ、架橋アルブミンもアガロースと同様に、細胞がその上には接着しませんでした。架橋アルブミンの直線パターンを細胞培養皿に作り、マウス骨格筋由来の筋芽細胞株であるC2C12細胞を培養液中で培養しました。比較対象とした、架橋していない通常のアルブミンで作った細胞培養用デバイスでは、細胞が全体に広がり細胞パターニングができないのに対して、架橋アルブミンでは、直線パターンが7日間にわたって維持されることが確認できました(図2D、E)。
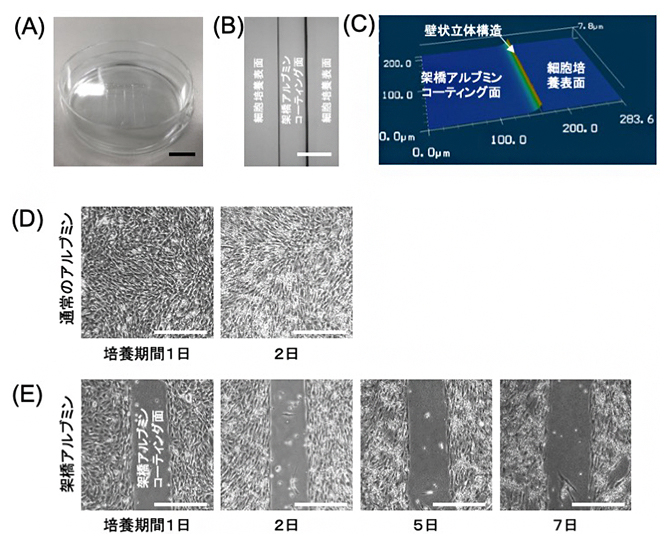
図2 架橋アルブミン製細胞培養用デバイスの作製と細胞パターニング
黒いスケールバーは1cm、白いスケールバーは0.4mm。
- (A)培養皿上に置いた架橋アルブミン製の微小デバイス。
- (B)鋳型から外した後の培養皿上の架橋アルブミン構造体の拡大画像。2本の直線の間に架橋アルブミンがコーティングされている。
- (C)溝の高さ200μmの鋳型を使って作製した架橋アルブミン構造を共焦点レーザー顕微鏡によって3次元観察した結果。架橋アルブミンコーティング面の端に、鋳型に沿って生じた高さ約7μmの立体構造が見える。1μmは1,000分の1mm。
- (D)通常のアルブミンを用いた場合の細胞パターニングの結果。細胞が全体に広がってパターニングができなかった。
- (E)架橋アルブミンを用いた場合の細胞パターニング結果。架橋アルブミンコーティング面には細胞が接着せず、それが7日間保持された。
今後の期待
これまでアガロースを使った細胞培養用デバイスは、長期間の細胞培養でも安定でしたが、作製に時間がかかるという課題がありました。今回使用した架橋アルブミンを用いれば、より短期間で作製できることから、実験に必要なものを必要なときに準備できるようになり、実験の効率化に貢献すると期待できます。
また、開発した微小デバイスは、シリコーンゴムの鋳型にタンパク質溶液を吸引させて作製した初めての細胞培養デバイスです。今回は手法の実証を目的として「細胞非接着性」のアルブミンを使用しましたが、シリコーンゴム製マイクロ流路の吸引力を利用した本手法は、「細胞接着性」の水溶性タンパク質にも展開可能です。細胞と細胞接着性タンパク質の相互作用(細胞の形状や発生・分化といった細胞機能と細胞接着性タンパク質の関連)を調査したいというニーズは高く、特定の形状を持つ構造の細胞接着性タンパク質を用いた微小デバイスがそのような研究にも応用されると考えられます。
さらに理研では、シリコーンゴムの鋳型を含む微細加工デバイスサービスを提供しており注3)、産総研で開発された架橋アルブミンと組み合わせることで、世界中の研究者が本手法に容易にアクセスできるようになると考えられます。
- 注3)2020年4月1日お知らせ「「微細加工デバイスサービス」を開始」
補足説明
- 1.アルブミン
血清アルブミンのこと。分子量約66,000の安定な可溶性タンパク質で、血液中のタンパク質の約60%を占める。血液の浸透圧調整の役割を担っている。タンパク質の標準物質として広く研究に用いられている。 - 2.シリコーンゴム
シリコーンを主成分とする樹脂。液体状態の原料(モノマー)に触媒を加えると、重合反応により硬化し、ゴム状になる。本研究ではポリジメチルシロキサン(PDMS)というシリコーンゴムを用いている。 - 3.細胞パターニング
培養皿の上など、細胞が接着する基材表面において、化学的な表面処理などにより、細胞が接着する部分と接着しない部分に分画し、細胞の接着エリアを制御する技術。近年発達している一細胞レベルでの解析や大量の細胞解析といった最先端細胞科学の発展には欠かせないものとなっている。例えば、細胞を定位置に置くことで観察のハイスループット化を可能にする。 - 4.アガロース
海藻から作られる寒天を精製したもので、生物学実験では核酸電気泳動や大腸菌培養などに利用され、生物学分野の研究室ではなじみ深い物質である。
共同研究グループ
理化学研究所 生命機能科学研究センター
集積バイオデバイス研究チーム
チームリーダー 田中 陽(たなか よう)
研修生 シン キゴウ(Shen Yigang)
上級研究員 田中 信行(たなか のぶゆき)
一細胞質量分析研究チーム
研究員 川井 隆之(かわい たかゆき)
産業技術総合研究所 バイオメディカル研究部門
次世代メディカルデバイス研究グループ
研究グループ長 永井 秀典(ながい ひでのり)
主任研究員 山添 泰宗(やまぞえ ひろのり)
研究グループ付 古谷 俊介(ふるたに しゅんすけ)
研究支援
本研究は、理化学研究所-産業技術総合研究所共同研究「チャレンジ研究」、日本学術振興会(JSPS)科学研究費補助金新学術領域研究(研究領域提案型)「オジギソウ搭載型植物機能利用スマートマシーン創発(研究代表者:田中陽)」、笹川科学研究助成(20192031)および文部科学省国費外国人留学生制度による支援を受けて行われました。
原論文情報
- Yigang Shen, Nobuyuki Tanaka, Hironori Yamazoe, Shunsuke Furutani, Hidenori Nagai, Takayuki Kawai, and Yo Tanaka, "Flow analysis on microcasting with degassed polydimethylsiloxane micro-channels for cell patterning with cross-linked albumin", PLOS ONE, 10.1371/journal.pone.0232518
発表者
理化学研究所
生命機能科学研究センター 集積バイオデバイス研究チーム
チームリーダー 田中 陽(たなか よう)
産業技術総合研究所 バイオメディカル研究部門
次世代メディカルデバイス研究グループ
研究グループ長 永井 秀典(ながい ひでのり)
報道担当
理化学研究所 広報室 報道担当
お問い合わせフォーム
産業技術総合研究所 企画本部 報道室
Tel: 029-862-6216
Email: press-ml [at] aist.go.jp
※[at]は@に置き換えてください。
