2023年10月30日
理化学研究所
国立医薬品食品衛生研究所
新潟大学
抗てんかん薬による薬疹の種類別リスク因子を発見
-遺伝子検査で異なるタイプの薬疹の発症を予防-
理化学研究所(理研)生命医科学研究センター ファーマコゲノミクス研究チームの莚田 泰誠 チームリーダー、福永 航也 研究員(国立医薬品食品衛生研究所 医薬安全科学部 協力研究員)、国立医薬品食品衛生研究所 医薬安全科学部の斎藤 嘉朗 部長(研究当時、現 同研究所 副所長)、新潟大学大学院 医歯学総合研究科の阿部 理一郎 教授らの共同研究グループは、抗てんかん薬カルバマゼピンによって生じる重症薬疹[1]のうちスティーブンス・ジョンソン症候群(SJS)[2]や中毒性表皮壊死融解症(TEN)[3]には特定のHLAアレル[4]である「HLA-B*15:11」、それ以外の薬疹には「HLA-A*31:01」が強く関連することを発見しました。
本研究で同定された二つのHLAアレルは、カルバマゼピンによる薬疹の発症リスクを予測するバイオマーカー[5]として活用されることが期待されます。
カルバマゼピンは、世界中でてんかんの治療薬として使われていますが、副作用である薬疹の発症率が高いことが問題となっています。重症薬疹であるSJS、TENや薬剤性過敏症症候群(DIHS)[6]に加えて、軽症薬疹である播種状紅斑丘疹型薬疹(MPE)や多形紅斑(EM)など多様なタイプの薬疹が存在し、症状や治療方法もさまざまです。
今回、共同研究グループは、SJSまたはTEN発症患者におけるHLA-B*15:11の保有率は29%であり、日本人集団における保有率2%と比較して統計的に有意に高頻度であることを突き止めました。HLA-A*31:01はSJSおよびTEN以外の薬疹と強く関係していることも明らかにしました。この二つのバイオマーカーを用いることでカルバマゼピンによる薬疹患者の約3分の2を説明することができました。
本研究は、科学雑誌『Journal of Investigative Dermatology』オンライン版(10月30日付:日本時間10月30日)に掲載されました。
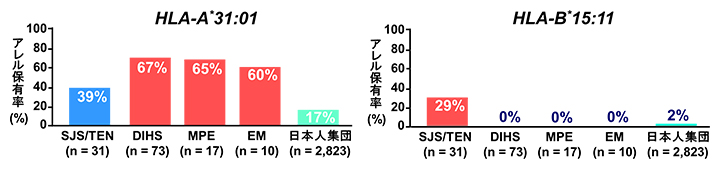
カルバマゼピンによる薬疹発症患者におけるHLA-A*31:01とHLA-B*15:11の保有率
背景
カルバマゼピンは、てんかん、躁病、躁うつ病の躁状態、統合失調症の興奮状態、三叉神経痛の治療に広く使われています。しかし、薬疹発症率が3.7~13%と非常に高く注1)、治療の上で大きな問題となっています。重症薬疹であるスティーブンス・ジョンソン症候群(SJS)、中毒性表皮壊死融解症(TEN)、薬剤性過敏症症候群(DIHS)、軽症薬疹である播種状紅斑丘疹型薬疹(MPE)や多形紅斑(EM)など多様なタイプの薬疹が存在し、その症状もさまざまです。いずれの薬疹も重篤化、後遺症または死亡につながる可能性があります。
これまで、共同研究グループは、カルバマゼピンを投薬する前に薬疹が起こりやすい患者を予測するためのバイオマーカーを研究してきました。2011年、理研統合生命医科学研究センター(研究当時、現生命医科学研究センター)は、カルバマゼピンによる薬疹発症例を用いたゲノムワイド関連解析(GWAS)[7]を行い、HLA-A遺伝子のHLA-A*31:01型を持つ日本人の患者は、同型を持たない患者に比べてカルバマゼピンによる薬疹が9.5倍起こりやすいことを報告しました注2)。そして2018年、前向き臨床研究「Genotype-Based Carbamazepine Therapy(GENCAT)study[8]」によってHLA-A*31:01を用いた薬理遺伝学検査が臨床現場において有用であることを実証しました注3)。しかし、この検査だけでは全ての患者の薬疹発症を予測することができず、また、異なる薬疹のタイプに関連する遺伝要因の違いも不明であったため、カルバマゼピンによる薬疹のタイプ別の詳細なゲノム解析の実施が待たれていました。
- 注1)Kramlinger KG, Phillips KA, Post RM. Rash complicating carbamazepine treatment. J Clin Psychopharmacol 1994;14(6):408-413; Arif H, Buchsbaum R, Weintraub D, et al. Comparison and predictors of rash associated with 15 antiepileptic drugs. Neurology 2007;68(2):1701-1709; McCormack M, Alfirevic A, Bourgeois S, et al. HLA-A*31:01 and carbamazepine-induced hypersensitivity reactions in Europeans. N Engl J Med 2011;364(12):1134-1143; Shirzadi M, Alvestad S, Hovdal H, et al. Comparison of carbamazepine rash in multiple sclerosis and epilepsy. Acta Neurol Scand 2012;125(1):60-63.
- 注2)Ozeki T, Mushiroda T, Yowang A, et al. Genome-wide association study identifies HLA-A*3101 allele as a genetic risk factor for carbamazepine-induced cutaneous adverse drug reactions in Japanese population. Hum Mol Genet 2011;20(5):1034-1041.
- 注3)2018年4月3日プレスリリース「てんかん治療薬遺伝子型検査の臨床的有用性を実証」
研究手法と成果
共同研究グループは、カルバマゼピンの服用後SJSまたはTENを生じた患者31人、DIHSを生じた73人、MPEを生じた17人、EMを生じた10人の計131人および日本人一般集団2,823人のゲノムDNAを用いて、GWASとHLA遺伝子の解析を行いました。国立医薬品食品衛生研究所および厚生労働省難治性疾患等政策研究事業(難治性疾患政策研究事業)重症多形滲出性紅斑に関する調査研究班によって収集されたコホート[9]をそれぞれコホート1、コホート2としました。各ゲノムDNAの一塩基多型(SNP)[10]のジェノタイピング[11]を行った後、サンプルごと、SNPごとの質を評価し、基準を満たしたサンプル、SNPを選別しました。その後、高精度の参照配列[12]を用いてインピュテーション法[13]を行い、解析対象のSNP情報を増やし、さらにSNP情報に基づいてHLAアレル情報を取得しました。各コホートでGWASを行った後、メタ解析でコホートデータを統合した結果、ゲノムワイド有意水準[14]を満たすHLA領域を同定しました(図1)。HLAアレル情報を用いて詳細な解析を行ったところ、カルバマゼピンによる薬疹とHLA-A*31:01が最も強く関連していることが分かりました。
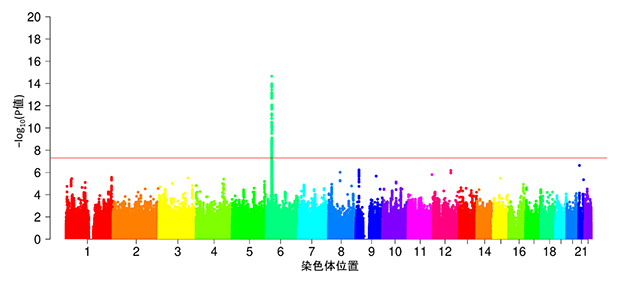
図1 カルバマゼピンによる薬疹発症患者におけるメタ解析の結果
2つのコホートの各SNPとカルバマゼピンによる薬疹のGWAS結果を統合したメタ解析の結果。横軸にヒトゲノム染色体上の位置、縦軸に各SNPとカルバマゼピンによる薬疹のメタ解析後のP値の負の対数値を示した。図の上に位置するほど関連が確からしいことを示す。赤い実線のゲノムワイド有意水準を超えるP値を示した6番染色体のHLA領域について詳細な解析を行った。
次に、薬疹の種類別にHLA解析を行ったところ、HLA-A*31:01はカルバマゼピンによるDIHS(P値=8.64×10-20、オッズ比[15]=10.1)、MPE(P値=1.51×10-5、オッズ比=9.1)、EM(P値=0.0019、オッズ比=7.4)と関連していましたが、SJSおよびTEN(P値=0.0022、オッズ比=3.1)では他の種類の薬疹ほど強い関連を示しませんでした(図2)。一方、HLA-B*15:11はDIHS、MPE、EMとの関連は有意ではありませんでしたが、SJSおよびTEN(P値=3.02×10-12、オッズ比=18.2)との関連は有意でした。なお、カルバマゼピンによる薬疹を起こした患者のうちHLA-A*31:01またはHLA-B*15:11のいずれかを持っている人は全体の66%でした。
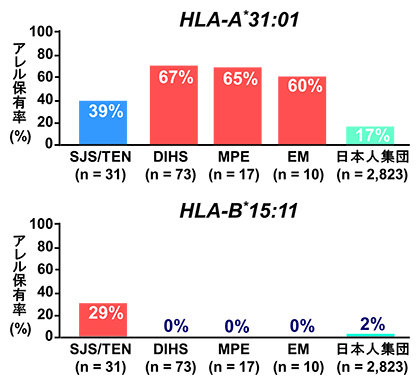
図2 カルバマゼピンによる薬疹発症患者におけるHLA-A*31:01とHLA-B*15:11の保有率
カルバマゼピンによる異なる種類の薬疹とHLA-A*31:01、HLA-B*15:11との関連を調べた結果。縦軸は各HLAアレルを保有している人の割合。
今後の期待
今回の研究結果から、HLA-B*15:11を保有する人は、保有しない人に比べてカルバマゼピンによるSJSまたはTENを発症するリスクが高く、HLA-A*31:01を保有する人はそれ以外の薬疹を発症するリスクが高いことが示されました。本研究で同定したHLA-B*15:11とHLA-A*31:01を組み合わせた遺伝子検査により、カルバマゼピンの治療開始前でも薬疹の発症リスクを予測することができ、てんかん治療薬の種類を替えることで副作用を回避したり、治療方法が異なる薬疹のタイプ別に早い段階で対処したりすることが期待されます。
補足説明
- 1.薬疹
薬によって起こる皮膚や眼、口などの粘膜に現れる発疹。 - 2.スティーブンス・ジョンソン症候群(SJS)
高熱(38℃以上)を伴って、発疹・発赤、火傷のような水ぶくれなどの激しい症状が、比較的短期間に全身の皮膚、口、目の粘膜に現れる病態。その多くは医薬品が原因と考えられており、原因となる医薬品は抗菌薬、解熱消炎鎮痛薬、抗けいれん薬などの広範囲にわたる。SJSはStevens-Johnson syndromeの略。 - 3.中毒性表皮壊死融解症(TEN)
全身の体表面積の10%を超える火傷のような水ぶくれ、皮膚の剥がれ、ただれなどが認められ、高熱(38℃以上)、目が赤くなるなどの症状を伴う重症の皮膚障害。中毒性表皮壊死融解症の症例の多くが、スティーブンス・ジョンソン症候群の進展型と考えられている。TENはtoxic epidermal necrolysisの略。 - 4.HLAアレル
ヒト白血球型抗原(HLA)を決定する遺伝子の型。HLA遺伝子には多くの種類が存在し、さらにそれぞれの遺伝子が数十種類の異なるタイプを持つ。HLAは免疫に関係が深く、多くの疾患の発症や副作用の発現のリスク因子であることが報告されている。HLA-A*31:01やHLA-B*15:11はHLAアレルの一つ。アレルとは対立遺伝子のことで、同一の遺伝子座にありながらDNA塩基配列に差がある変異体を指す。HLAはhuman leukocyte antigenの略。 - 5.バイオマーカー
疾患の発症や進行の予測に役立つ生体由来の物質のこと。特定の遺伝子配列や血液中のタンパク質や代謝産物などが対象になる。 - 6.薬剤性過敏症症候群(DIHS)
高熱(38℃以上)を伴って、全身に赤い斑点が見られ、さらに全身のリンパ節(首、わきの下、股の付け根など)が腫れたり、肝機能障害などの血液検査値の異常が見られたりする重症の皮膚障害。通常の薬疹とは異なり、原因となる医薬品の服用後すぐには発症せずに2週間以上経ってから発症することが多い。DIHSはdrug-induced hypersensitivity syndromeの略。 - 7.ゲノムワイド関連解析(GWAS)
疾患感受性遺伝子を見つける代表的な方法。ヒトゲノムを網羅した数百万~1,000万カ所の一塩基多型を対象に、対象サンプル群における疾患との因果関係を評価できる。2002年に世界で初めて理研で実施された手法であり、以後世界中で精力的に実施されている。GWASはgenome-wide association studyの略。 - 8.Genotype-Based Carbamazepine Therapy(GENCAT)study
2012年に全国の18医療機関、36病院と理研が共同研究グループを立ち上げ、抗てんかん薬カルバマゼピン治療におけるHLA-A*31:01遺伝子検査の臨床的有用性を実証した前向き臨床介入研究。 - 9.コホート
医学研究における対象者の集団。 - 10.一塩基多型(SNP)
ヒトの染色体にある全DNA情報(ヒトゲノム)は、約30億文字の並び(塩基配列)で構成されている。この文字の並びは遺伝情報となっており、その99.7%は全人類で共通であるが、0.3%程度に個人差(遺伝子多型)があることが分かっている。多くの遺伝子多型ではその影響は見られないが、一部は病気へのかかりやすさなどに関係していると考えられている。SNP(スニップ)とは、塩基配列の文字の並びが一つだけ異なっているものであり、30億塩基の中に約1,000万カ所ある。SNPはsingle nucleotide polymorphismの略。 - 11.ジェノタイピング
プローブと呼ばれる塩基を検出するためのDNA断片が、チップ上に高密度に敷き詰められたSNPアレイを用いて、SNPの塩基情報を解析する手法。 - 12.参照配列
全ゲノム領域のSNP情報やHLA情報が明らかになっている既知のデータ群。本研究では、1000ゲノムプロジェクト(The 1000 Genomes Browsers)で公開されている全ゲノムシークエンスデータおよびNBDCヒトデータベースで公開されているSNP情報とHLA情報の統合参照配列(hum0028.v2)を用いた。 - 13.インピュテーション法
SNPアレイでは測定できないSNPやHLAアレルを推定し、補完する遺伝統計学的手法。 - 14.ゲノムワイド有意水準
P値は、ある試験において、二つの群間の差が偶然生じる可能性を示す指標であり、小さいほど2群間の差が生じている可能性が高い。通常の統計解析では、P値が0.05未満である場合、統計的に意味があると判断する。これは、ある結果を偶然生じることが100回に5回未満であることを意味するが、GWASでは数百万回以上の検定を行うため、全く関係がなくても偶然に関係があると誤って判断されてしまう可能性がある。そこで、通常の判定基準である0.05をさらに100万で割った5×10-8未満という厳しい判定基準を採用して、誤った判断をしないように独自に有意水準を設定している。 - 15.オッズ比
発症リスクの大きさの指標。健常者の集団のリスク要因を持つ人の割合(オッズ)に対する、発症患者でリスク要因を持つ人の割合の比で表す。
共同研究グループ
理化学研究所 生命医科学研究センター ファーマコゲノミクス研究チーム
チームリーダー 莚田 泰誠(ムシロダ・タイセイ)
研究員(研究当時)大関 健志(オオゼキ・タケシ)
研究員 福永 航也(フクナガ・コウヤ)
(国立医薬品食品衛生研究所 医薬安全科学部 協力研究員)
国立医薬品食品衛生研究所 医薬安全科学部
部長(研究当時)斎藤 嘉朗(サイトウ・ヨシロウ)
(現 国立医薬品食品衛生研究所 副所長)
室長 中村 亮介(ナカムラ・リョウスケ)
主任研究官 田中 庸一(タナカ・ヨウイチ)
研究員 塚越 絵里(ツカゴシ・エリ)
藤田医科大学 医学部 アレルギー疾患対策医療学講座
教授 松永 佳世子(マツナガ・カヨコ)
千葉大学 大学院医学研究院
感染生体防御学
特任教授 関根 章博(セキネ・アキヒロ)
公衆衛生学
技術専門職員 真下 陽一(マシモ・ヨウイチ)
厚生労働省難治性疾患等政策研究事業(難治性疾患政策研究事業)重症多形滲出性紅斑に関する調査研究班
杏林大学 医学部 皮膚科学教室
教授 水川 良子(ミズカワ・ヨシコ)
講師 倉田 麻衣子(クラタ・マイコ)
横浜市立大学 大学院医学研究科 環境免疫病態皮膚科学
教授 山口 由衣(ヤマグチ・ユキエ)
講師 渡邉 裕子(ワタナベ・ユウコ)
島根大学 医学部 皮膚科学講座
教授(研究当時)森田 栄伸(モリタ・エイシン)
講師 新原 寛之(ニイハラ・ヒロユキ)
昭和大学 横浜市北部病院 皮膚科
教授 渡辺 秀晃(ワタナベ・ヒデアキ)
国立病院機構 四国がんセンター
副院長 藤山 幹子(トウヤマ・ミキコ)
京都大学 医学研究科 皮膚科学教室
教授 椛島 健治(カバシマ・ケンジ)
特定准教授 野村 尚史(ノムラ・タカシ)
特定准教授 中島 沙恵子(ナカジマ・サエコ)
奈良県立医科大学 皮膚科学教室
教授 浅田 秀夫(アサダ・ヒデオ)
准教授(研究当時)小豆澤 宏明(アズキザワ・ヒロアキ)
新潟大学大学院 医歯学総合研究科 皮膚科学分野
教授 阿部 理一郎(アベ・リイチロウ)
講師 濱 菜摘(ハマ・ナツミ)
助教 長谷川 瑛人(ハセガワ・アキト)
研究支援
本研究の一部は、厚生労働科学研究費補助金 難治性疾患政策等研究事業(難治性疾患政策研究事業)「重症多形滲出性紅斑に関する調査研究(研究代表者:阿部理一郎)」による支援を受けて行われました。
原論文情報
- Koya Fukunaga, Eri Tsukagoshi, Maiko Kurata, Yoshiko Mizukawa, Hiroyuki Nihara, Eishin Morita, Yuko Watanabe, Yukie Yamaguchi, Hideaki Watanabe, Saeko Nakajima, Takashi Nomura, Kenji Kabashima, Mikiko Tohyama, Hiroaki Azukizawa, Hideo Asada, Akito Hasegawa, Natsumi Hama, Takeshi Ozeki, Yoichi Mashimo, Akihiro Sekine, Kayoko Matsunaga, Yoichi Tanaka, Ryosuke Nakamura, Riichiro Abe, Taisei Mushiroda, Yoshiro Saito, "Differential effects of HLA-B*15:11 and HLA-A*31:01 on carbamazepine-induced cutaneous adverse reactions", Journal of Investigative Dermatology, 10.1016/j.jid.2023.09.282
発表者
理化学研究所
生命医科学研究センター ファーマコゲノミクス研究チーム
チームリーダー 莚田 泰誠(ムシロダ・タイセイ)
研究員 福永 航也(フクナガ・コウヤ)
(国立医薬品食品衛生研究所 医薬安全科学部 協力研究員)
 莚田 泰誠
莚田 泰誠
 福永 航也
福永 航也
国立医薬品食品衛生研究所 医薬安全科学部
部長(研究当時)斎藤 嘉朗(サイトウ・ヨシロウ)
(現 国立医薬品食品衛生研究所 副所長)
新潟大学大学院 医歯学総合研究科
教授 阿部 理一郎(アベ・リイチロウ)
報道担当
理化学研究所 広報室 報道担当
お問い合わせフォーム
国立医薬品食品衛生研究所 業務課業務係
Tel: 044-270-6600内線11560 / Fax: 044-270-6622
Email: gyoumukakari [at] nihs.go.jp
新潟大学 広報事務室
Tel: 025-262-7000
Email: pr-office [at] adm.niigata-u.ac.jp
※上記の[at]は@に置き換えてください。
