理化学研究所(理研)環境資源科学研究センター 天然物生合成研究ユニットの高橋 俊二 ユニットリーダー、藤山 敬介 訪問研究員(研究当時、現 植物化学遺伝学研究チーム 基礎科学特別研究員)、髙木 海 テクニカルスタッフⅠ、ニュー・ノック・クウィン・ヴォ 特別研究員(研究当時、現 植物ゲノム発現研究チーム 研究員)、森田 直子 テクニカルスタッフⅠ、分子構造解析ユニットの野川 俊彦 技師の研究チームは、ユニークなドメイン[1]構成を有する海洋細菌Aquimarina spongiae由来のドリメノール合成酵素(AsDMS)[2]の立体構造を解明しました。また、AsDMSに部位特異的変異を導入[3]することで、ドリメノールとは異なるテルペノイド[4]を生産できる機能改変酵素の創出に成功しました。
テルペノイドは、植物や一部の微生物が生産する多様な天然化合物群で、医薬品や工業原料、香水・精油などに利用され、文明や健康、食文化の発展に不可欠でした。今後、さらなる酵素機能の改変によって酵素反応の増強や多様なテルペノイドの生産が期待されます。
研究チームはAsDMSに対してX線結晶構造解析[5]を実施し、全体構造や基質、酵素[6]の結合様式を原子レベルで明らかにしました。これにより、AsDMSにおける基質の結合や触媒作用に関わるアミノ酸残基(触媒残基)[7]を同定することに成功しました。また、これらアミノ酸残基に部位特異的変異を導入した変異型AsDMSを複数作製し、それらの機能を調べることにより、AsDMSがドリメノールを生産する触媒メカニズムを原子レベルで理解するだけでなく、ドリメノールとは異なるテルペノイドを生産できる機能改変酵素の創出に成功しました。
本研究は、科学雑誌『Chemical Science』オンライン版(7月28日付)に掲載されました。

AsDMSが触媒する連続的な反応と立体構造
背景
自然界にはさまざまな二次代謝産物[8]が存在しています。その中でもテルペノイドは非常に多様な構造を有しており、抗炎症作用を持つ医薬品や抗がん剤の原料、さらには農薬や香料など、あらゆる場面で利用されています。テルペノイドの生合成[8]はテルペン[4]環化酵素(TC)による基質の環化反応から始まることが知られており、その遺伝子は動物、植物、微生物、ウイルスなどの多様な生物種から発見されています。一般的に、典型的なTCの立体構造は生物種によらずほぼ同様で、α、β、γの3種のドメインの組み合わせによって構成されています。近年、このドメイン構成に従わないTCがいくつも発見されており、それらの基質認識機構や触媒メカニズムへの注目が高まっています。
ハロ酸デハロゲナーゼ様ホスファターゼ(HAD)[9]とTCのβドメイン(TCβ)から構成される酵素群(HAD-TCβ)もその一つで、過去に、高橋ユニットリーダーらはastellolide生合成クラスターからAstCと名付けられたHAD-TCβを世界に先駆けて報告した他注1)、細菌由来初のHAD-TCβとして海洋細菌Aquimarina spongiae由来のドリメノール合成酵素(AsDMS)を報告してきました注2)。
以前の研究から、AsDMSは二段階の反応を触媒(一段階目に基質の環化、二段階目に環化基質の脱リン酸化)すると考えられており、AsDMSの反応効率は、同様の反応を触媒する植物由来のTCよりも優れていることが分かっていました。しかしながら、HAD-TCβの立体構造は依然として明らかにされておらず、その特徴的なドメイン構成と機能の相関については解明されていませんでした。そこで研究チームは、AsDMSを研究対象としてX線結晶解析を行い、原子レベルでAsDMSの機能の理解を目指しました。
- 注1)2016年9月26日プレスリリース「新規セスキテルペン生合成遺伝子の発見」
- 注2)2022年5月18日プレスリリース「海洋細菌由来の新しいテルペン合成酵素の発見」
研究手法と成果
まず、研究チームはX線結晶構造解析に有利となる変異(活性部位であるD333からD333Nへの変異)をAsDMSに導入し、X線結晶構造解析を行いました。明らかにされた全体像を見ると、AsDMSは二つの同じ分子が結合した二量体を形成しており、TCβドメインとHADドメインがそれぞれの基質を特異的に取り込むことができる独立した触媒ポケットを有していました(図1)。TCβドメインに注目すると、他の酵素のTCβドメインと非常に似ていた一方で、HADドメインについてはロスマンフォールド[10]領域の一部が、一般的な折りたたみ方と異なっていることが判明しました。HAD-TCβに見られる二つの機能を有した酵素は、分子進化の過程でそれぞれ独立した酵素が融合することで生まれたと考えられます。その分子進化の過程で構造最適化を受けたことで、AsDMSのHADドメインのロスマンフォールドが変化した可能性が示唆されました。

図1 AsDMSの全体構造およびFPPとDPの結合様式
(上)X線結晶構造解析によって明らかにされたAsDMSの全体構造。(下)FPP(ファルネシル二リン酸)結合型AsDMSの結晶構造によって明らかになったTCβドメイン内部におけるFPPの結合様式(左)と、DP(ドリメニルリン酸)結合型AsDMSの結晶構造によって明らかになったHADドメイン内部におけるDPの結合様式(右)。黄色の波線は水素結合、赤い球体モデルは水分子、マゼンタで示した部分は各ドメインにおける触媒残基をそれぞれ示す。
次に基質の結合様式と反応メカニズムを明らかにするため、一段階目の基質(ファルネシル二リン酸:FPP)が結合したAsDMSの結晶構造を決定しました。FPPはTCβドメインの内部にS字状に折り曲げられた状態で結合していることが明らかになり、FPPのC10位は、触媒となるアミノ酸残基の近傍に配置されていました(図1、下段左側)。また、FPPの結合や反応中間体の安定化などの役割を担うアミノ酸残基が明らかになり、それらアミノ酸残基の部位特異的変異体を用いた実験によって、各種アミノ酸残基の重要性が実証されました。
また、研究チームはAsDMSのホモログ[11]の一つであるAncCが別のテルペノイドのアルビカノールを生産することに注目し、HAD-TCβの「テルペノイドのつくり分けメカニズム」の解明を目指しました。AsDMSの立体構造とAIによって予測・生成されたAncCの立体構造を比較したところ、触媒部位の周囲で四つのアミノ酸残基の違いが確認されました。これらのアミノ酸残基を交換したAsDMS(変異型AsDMS)の活性を確認したところ、変異型AsDMSはアルビカノールを主成分として生成しました。この実験から、HAD-TCβがテルペノイドをつくり分けるために必要なアミノ酸残基が明らかにされました。
次に、AsDMSによる中間体の脱リン酸化メカニズムを明らかにするために、研究チームは生化学的な実験を実施しました。AsDMSのHADドメインの機能を不活化もしくは阻害した状態でFPPを酵素反応させたところ、FPPが環化したドリメニル二リン酸(DPP)が検出されたため、これがHADドメインの基質であることが明らかになりました。続けて、リン酸のみを検出できる分析方法を利用したところ、HADドメインは二段階の脱リン酸化を触媒することでドリメノールを生産していることが分かりました。この結果から、AsDMSは三段階の反応を触媒していることが明らかとなりました(図2)。
最後に、研究チームはHADドメインの触媒残基を明らかにするために、中間体のドリメニルリン酸(DP)(図2)が結合したAsDMSの結晶構造を決定しました。DPはHADドメインの中心に結合しており、触媒残基と考えられるアミノ酸残基の位置を捉えました(図1、下段右側)。また、TCβドメインの時と同様に、それらアミノ酸残基の部位特異的変異体を用いた検証実験により、触媒残基の同定や他のアミノ酸残基の役割を決定することに成功しました。
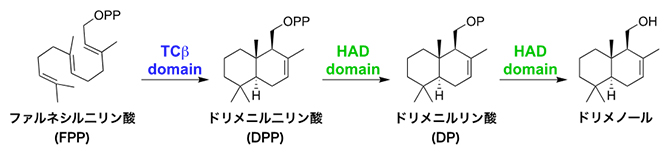
図2 AsDMSによるFPPからドリメノールへの変換反応
本研究によって明らかにされたAsDMSによるFPP(ファルネシル二リン酸)からドリメノールへの変換スキーム。従来の生化学的な実験に加え、さまざまな実験による結果を統合したことで明らかとなった。
以上の実験結果を統合することで、AsDMSが触媒する連続した触媒反応メカニズムを決定し、同時に、AsDMSの改変によるさまざまなテルペノイド生産の可能性が示されました。また、本研究によって連続的な触媒反応を効率化させる酵素機能の存在や、細菌と真菌のHAD-TCβの違いなども浮き彫りになりました。
今後の期待
人類は古くから、植物や菌類などのテルペノイドを含む天然物を鎮静剤や香料、農薬として利用してきました。テルペノイドは医療から嗜好品まで多岐にわたる分野で活用されていますが、その複雑な分子構造故に、化学合成が困難な場合もあります。一方で、酵素やその遺伝子を導入した微生物などを利用したテルペノイド生産は、正確かつ環境負荷の少ない手法として期待されています。得られた成果を基に、今後はAsDMSをはじめとするHAD-TCβの機能の改変・強化による有用テルペノイドの生産が期待されます。
本研究成果は、国際連合が定めた17の目標「持続可能な開発目標(SDGs)[12]」のうち「3.すべての人に健康と福祉を」と「9.産業と技術革新の基盤を作ろう」に大きく貢献するものです。
補足説明
- 1.ドメイン
ここでは、いくつかのアミノ酸残基のみによってフォールド([10]参照)し、特定の立体構造を取る領域を指す。小さいタンパク質は一つのドメインのみによって構成、機能を有する場合があり、大きいタンパク質は複数のドメインによって構成されることが多い。 - 2.ドリメノール合成酵素(AsDMS)
テルペノイド([4]参照)の一種であるドリメノールを作り出す酵素。AsDMSは、海洋細菌であるAquimarina spongiaeの頭文字とドリメノール合成酵素の英語表記(drimenol synthase)から名付けられた。 - 3.部位特異的変異を導入
タンパク質を構成する特定のアミノ酸の改変を目的として、酵素遺伝子に変異を導入する実験手法。 - 4.テルペノイド、テルペン
テルペノイドは、炭素5個のイソプレンを構成単位とする天然有機化合物の総称。炭化水素では単にテルペンと呼ばれ、酸素原子が挿入されるなどの修飾を受けたものを特にテルペノイドと呼ぶ。 - 5.X線結晶構造解析
核酸やタンパク質などの大きな生体分子の立体構造を決定する上で有効な手段の一つとしてよく用いられている手法。試料の結晶化が必須となるが、原子レベルで分子の立体構造を明らかにできる。なお、結晶は分子が3次元的に規則正しく並んだ状態を指しており、塩や砂糖と同様に、条件さえ整えばタンパク質も結晶化する。結晶に対してX線を照射することで回折と呼ばれる現象が起こる。回折によって得られる斑点状の回折の強度には、結晶を構成する分子の構造に由来する情報が反映されているため、回折像を解析することで、結晶を構成する分子の立体構造を求められる。 - 6.基質、酵素
一般的に、酵素とはある物質を別の物質へと変換する能力(触媒能力)を持つタンパク質のことを指す。酵素はその種類ごとに認識する物質が決まっており、それらを基質と呼ぶ。 - 7.アミノ酸残基(触媒残基)
タンパク質は20種類のアミノ酸が特定の順序でつながった巨大な分子であり、その由来となったタンパク質中のアミノ酸のことを特にアミノ酸残基と呼ぶ。タンパク質を構成するアミノ酸残基の種類とその順序はアミノ酸配列と呼ばれる。アミノ酸残基はそれぞれ1文字のアルファベットで示され、例えば、'D43'は43番に配置されたアミノ酸がD(アスパラギン酸)であることを意味する。同じアミノ酸残基であっても、タンパク質の種類やその位置によって役割は全く異なる。酵素中では、一部のアミノ酸残基が基質の変換(触媒)を担う核となっており、それらを触媒残基と呼ぶ。 - 8.二次代謝産物、生合成
生合成は生体内で必要な生体物を生成する過程。生物体を構成、維持する上で重要な物質を一次代謝産物、生育に必ずしも必須ではない物質を二次代謝産物と呼ぶ。微生物において、二次代謝産物の生合成に関わる遺伝子群はゲノム中のある特定の領域に並んで存在している。 - 9.ハロ酸デハロゲナーゼ様ホスファターゼ(HAD)
ハロ酸デハロゲナーゼ様スーパーファミリー(haloacid dehalogenase-like hydrolase superfamily)に属する酵素。酵素の機能の多くは明らかにされていないが、その一つに脱リン酸化活性が知られている。 - 10.ロスマンフォールド
フォールドは日本語で「折りたたみ」を意味する。例えば、タンパク質を構成するアミノ酸配列は単にアミノ酸が連なった「紐(ひも)」であるが、特定の条件(曲げ方)を満たすと「布」になり、さらにそれを「編み込む」ことで、「カゴ」となってモノを運ぶ機能を獲得する。この例のように、フォールドは、単なるアミノ酸配列が特定の構造へと折りたたまれる過程や折りたたまれた後の構造のことを指す。ロスマンフォールドは1970年にロスマン博士によって見つけられた、タンパク質において頻出する典型的なフォールドを指す。 - 11.ホモログ
共通する祖先を持つ遺伝子を指す。アミノ酸配列が類似しており、機能や立体構造においても似ていることが多い。特に、機能において非常に重要な触媒残基の機能や位置などは、ホモログ間で完全に一致することがよく見られる。 - 12.持続可能な開発目標(SDGs)
2015年9月の国連サミットで加盟国の全会一致で採択された「持続可能な開発のための2030アジェンダ」にて記載された、2016年から2030年までの15年間で達成する国際目標。持続可能な世界を実現するための17の目標、169のターゲットから構成され、発展途上国のみならず、先進国自身が取り組むユニバーサル(普遍的)なものであり、日本としても積極的に取り組んでいる(外務省ホームページから一部改変して転載)。SDGsはSustainable Development Goalsの略。
研究支援
本研究は、日本学術振興会(JSPS)科学研究費助成事業基盤研究(A)「天然化合物の多様性拡張を志向した生合成分子基盤の解明(研究代表者:高橋俊二、20H00416)」「天然化合物に生理活性を付与する生合成分子基盤の解明と新規酵素のデノボデザイン(研究代表者:高橋俊二、25H00924)」、同学術変革領域研究(A)「AIを活用した未知の二次代謝生合成酵素の機能解明と分子間相互作用の精密解析(研究代表者:高橋俊二、23H04564)」「二次代謝産物の生合成における複合酵素反応と未知の基質チャネリング機構の解明(研究代表者:高橋俊二、25H01597)」、同特別研究員奨励費「ブラシノステロイドを輸送するトランスポーターの探索(研究代表者:藤山敬介、21J01340)」による助成を受けて行われました。
また、結晶構造解析は、日本医療研究開発機構(AMED)創薬等ライフサイエンス研究支援基盤事業創薬等先端技術支援基盤プラットフォーム(BINDS)の支援を受けて行われました。
原論文情報
- Keisuke Fujiyama, Hiroshi Takagi, Nhu Ngoc Quynh Vo, Naoko Morita, Toshihiko Nogawa, and Shunji Takahashi, "Structural Insights into a Bacterial Terpene Cyclase Fused with Haloacid Dehalogenase-like Phosphatase", Chemical Science, 10.1039/D5SC04719F
発表者
理化学研究所
環境資源科学研究センター 天然物生合成研究ユニット
ユニットリーダー 高橋 俊二(タカハシ・シュンジ)
訪問研究員(研究当時)藤山 敬介(フジヤマ・ケイスケ)
(現 植物化学遺伝学研究チーム 基礎科学特別研究員)
テクニカルスタッフⅠ 髙木 海(タカギ・ヒロシ)
特別研究員(研究当時)ニュー・ノック・クウィン・ヴォ(Nhu Ngoc Quynh Vo)
(現 植物ゲノム発現研究チーム 研究員)
テクニカルスタッフⅠ 森田 直子(モリタ・ナオコ)
分子構造解析ユニット
技師 野川 俊彦(ノガワ・トシヒコ)
 藤山 敬介
藤山 敬介
 高橋 俊二
高橋 俊二
報道担当
理化学研究所 広報部 報道担当
お問い合わせフォーム
