2012年4月27日
独立行政法人 理化学研究所
腸内環境のアンバランスが全身の免疫系を過剰に活性化
-腸内環境の改善が自己免疫疾患の症状軽減や予防に役立つ可能性示す-
ポイント
- 免疫抑制受容体「PD-1」がIgA抗体の質を維持し、腸内環境のバランスを制御
- PD-1を欠損すると、腸内の善玉菌はほとんど消失し、悪玉菌は400倍に増加
- IgA抗体の腸内細菌への結合力低下が、腸内環境のアンバランスを導く
要旨
理化学研究所(野依良治理事長)は、免疫系を抑える機能をもつ免疫抑制受容体「PD-1(programmed cell death-1)」 が、腸管免疫に重要な影響を及ぼす腸内細菌の構成を制御していることを発見しました。これは理研免疫・アレルギー科学総合研究センター(谷口克センター長)粘膜免疫研究チームのシドニア ファガラサン(SIDONIA FAGARASAN)チームリーダーらによる研究成果です。
ヒトの腸管内には500~1,000種類、総数100兆個にも及ぶ腸内細菌が共存し、腸管免疫系を適切に活性化して、私たちの健康を維持しています。この適切な活性化には腸内細菌の構成が重要で、ここで産生される大量の免疫グロブリンA(IgA抗体※1)というタンパク質が主な役割を担っています。
免疫抑制受容体PD-1は、抗体産生を調節するヘルパーT細胞※2に発現しており、免疫系を抑える機能をもつとされています。実際にマウスのPD-1を欠損すると、免疫反応が暴走してさまざまな自己免疫疾患を発症します。しかし、このPD-1欠損マウスの腸内細菌を除くと、自己免疫疾患を発症しないことも知られており、腸内細菌が自己免疫疾患に及ぼす影響の詳細は不明のままでした。
研究チームは、PD-1欠損マウスを用いて、腸管で産生されるIgA抗体や腸内細菌の構成を調べました。その結果、PD-1欠損マウスでは、B細胞に司令を出すヘルパーT細胞が3倍に増加して、適切な抗体を産生するB細胞※2の選択ができなくなり、腸内細菌との結合力が弱いIgA抗体ができることが分かりました。これにより腸内細菌の構成が変化し、善玉菌※3として知られるビフィズス菌が検出できないほど減少し、通常は少ないはずの悪玉菌※3であるエンテロバクター属菌が400倍も増加することを発見しました。さらに、PD-1欠損マウスでは、炎症性のサイトカイン※4を産生するヘルパーT細胞の数が4倍に増加したとともに、通常は腸管だけにあるはずの腸内細菌に対する抗体を、血液中から検出しました。これらの結果から、腸内環境のアンバランスな状態が、全身の免疫系を過剰に活性化することを明らかにし、自己免疫疾患などの病態を悪化させている可能性を見いだしました。
今後、腸内環境が全身の免疫系へ及ぼす影響が明らかになると、自己免疫疾患の症状を和らげたり予防したりする新たな治療法の開発につながると期待できます。
本研究成果は、米国の科学雑誌『Science』(4月27日号)に掲載されます。
背景
ヒトの腸管内には500~1,000種類、総数100兆個にも及ぶ細菌が共存しているうえ、食物や病原菌など、さまざまな異物が日々取り込まれています。免疫系は、病気を引き起こす細菌やウイルスなどの感染を防ぐ一方、腸管に生息する腸内細菌や食物といった無害な異物に対しては破壊的に反応せず、私たちの健康を維持しています。この免疫応答が少なすぎると免疫不全症を引き起こし、逆に多すぎると自己免疫疾患やアレルギー疾患などを発症します。腸管で正しい免疫応答を引き起こすには、腸内細菌の構成が重要であることが分かっていました。
この構成の制御に重要な役割を担っているのが、腸管内腔へ大量に分泌されるIgA抗体というタンパク質です。IgA抗体は、腸管のパイエル板※5にある胚中心※6と呼ばれる特殊な環境下で、ヘルパーT細胞の司令を受けたB細胞により産生されます。
このようにIgA抗体産生に重要な役割を果たしているヘルパーT細胞は、免疫抑制受容体PD-1というタンパク質を細胞表面に高発現しています。PD-1を発現しているヘルパーT細胞は増殖が適度に抑えられるため、免疫応答が異常に活性化されないと考えられています。実際にPD-1を欠損したマウスは、さまざまな自己免疫疾患を発症します。一方、PD-1欠損マウスの腸内細菌を除くと、自己免疫疾患を発症しないことが知られていました。このことは、腸内細菌が自己免疫疾患に何らかの影響を及ぼしていることを示唆していますが、そのメカニズムの詳細は分かっていませんでした。
これまで研究チームは、IgA抗体が善玉菌と悪玉菌の構成を制御するという知見を報告してきました。そこで、PD-1欠損マウスのIgA抗体の質と腸内細菌の構成を測定し、それらが自己免疫疾患にどのような影響を及ぼしているのかを調べました。
研究手法と成果
まず、正常マウスとPD-1欠損マウスの腸管内にどのような細菌がどのくらい存在しているのかを比較しました。その結果、腸内細菌の総数は同じでしたが、その構成が変わっていることを見いだしました。具体的には、PD-1欠損マウスでは善玉菌で知られるビフィズス菌が検出できないほど減少した一方、腸管内で本来増えることができない悪玉菌(エンテロバクター属菌)は400倍も増加していることが分かりました。このように構成が変わった理由を突き止めるため、IgA抗体の質と量を調べました。その結果、IgA抗体を産生するB細胞は、正常マウスとPD-1欠損マウスでほぼ同数で(図1右)、腸管内に分泌されているIgA抗体の量も同じでした。しかし、PD-1欠損マウスのIgA抗体は腸内細菌に結合する力が弱いことが分かりました。
次に、IgA抗体の結合力が低下した理由を調べるため、パイエル板にあるB細胞やT細胞を調べました。その結果、PD-1欠損マウスでは、パイエル板の胚中心が大きくなり(図1左)、その中のヘルパーT細胞の数が3倍も増加していることが分かりました(図1中)。これらのことから、増加したヘルパーT細胞がB細胞に過剰に働きかけ、本来ならば除かれるべき“出来の悪い”B細胞が生き残った結果、結合力が弱いIgA抗体が腸管内腔に分泌されていることが分かりました。
続いて、腸内細菌の構成の変化と全身の免疫系との関係を調べました。PD-1欠損マウスでは、正常マウスに比べ炎症性のサイトカインを産生するヘルパーT細胞が4倍に増加していること、正常の状態では現れない胚中心が腸管以外のリンパ節に存在し、T細胞やB細胞の数もそれぞれ2.5倍と2倍に増えていることが分かりました。また、通常は腸管でしか見られないはずの腸内細菌に対する抗体を血液中からも検出したことから、PD-1欠損マウスでは全身の免疫系が過剰に活性化していることが明らかになりました。PD-1欠損マウスに抗生物質を投与して、構成変化後の腸内細菌を除くと過剰な活性化が治まったことから、腸内細菌の構成が不適切になると、全身の免疫系の過剰な活性化につながることが分かりました。
今後の期待
今回、PD-1がIgA抗体の質を制御して腸内環境のバランスを保っていることが判明しました。また、IgA抗体の結合力低下が引き起こす腸内環境のアンバランスな状態が、全身の免疫系の過剰な活性化につながることを明らかにし、自己免疫疾患などの病態を悪化させている可能性を示しました(図2)。今後、腸内環境が全身の免疫系へ及ぼす影響を明らかにし、腸内環境の改善で自己免疫疾患の症状を和らげたり、予防したりする新たな治療法の開発につなげていくことを目指します。
発表者
理化学研究所
免疫・アレルギー科学総合研究センター
粘膜免疫研究チーム チームリーダー
Sidonia Fagarasan(シドニア ファガラサン)
お問い合わせ先
横浜研究推進部 企画課
Tel: 045-503-9117 / Fax: 045-503-9113
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.IgA抗体
哺乳類の抗体(免疫グロブリン)には、構造的特徴から大きく分けてIgM、IgD、IgG、IgE、IgAの5種類の型が存在し、それぞれ異なった機能を持つ。IgAは主に腸管などの粘膜組織に存在するB細胞が産生し、粘膜上皮細胞を通過して腸管内へ分泌されて異物が体内に侵入するのを防ぐ。腸内細菌の制御でも重要な役割を持つ。 - 2.T細胞、B細胞
免疫系を構成する主な細胞であるリンパ球はB細胞とT細胞に大きく分けられる。B細胞は抗体(免疫グロブリン)と呼ばれるタンパク質を作り、この抗体がウイルスや細菌、毒素といった異物に特異的に結合して排除する。T細胞は、T細胞レセプターと呼ばれるタンパク質を細胞表面に持ち、このレセプターを介して異物を特異的に認識し活性化する。T細胞はその働きから、ウイルス感染細胞やがん細胞などを特異的に殺すキラーT細胞と、B細胞やマクロファージ(食細胞)などほかの免疫細胞に働きかけてその機能を活性化するヘルパーT細胞に大きく分類されている。 - 3.善玉菌、悪玉菌
善玉菌とは、ビフィズス菌に代表される Bifidobacterium属や、乳酸菌と呼ばれる Lactobacillus属の細菌など、乳酸や酪酸といった有機酸を作って、宿主の健康維持に貢献している菌。悪玉菌とは、ウェルシュ菌に代表される Clostridium属や大腸菌など、悪臭のもととなるいわゆる腐敗物質を産生する菌で、宿主の健康に害を与える菌。 - 4.サイトカイン
細胞同士の情報伝達にかかわるさまざまな生理活性を持つ可溶性タンパク質の総称。さまざまな細胞から分泌、標的細胞の増殖・分化・細胞死を誘導する。炎症性サイトカインは、体内への異物の侵入を受け産生されるサイトカインで、生体防御に関与する多種類の細胞に働き、炎症反応を引き起こす。 - 5.パイエル板
リンパ球などの免疫細胞が集合して、小腸内に作られるリンパ組織。B細胞がヘルパーT細胞の司令を受けて、IgA抗体を誘導する主要な場である。 - 6.胚中心
免疫応答の際に2次免疫組織につくられる微小構造。抗体を産生するB細胞の活発な増殖、選択、成熟と消失がみられる部位。胚中心はその構造学的特徴から暗領域、明領域に分けられ、こうしたB細胞の成熟過程は主に胚中心の明領域で行われる。胚中心の明領域にあるヘルパーT細胞がB細胞の成熟過程で重要な役割をもつ。
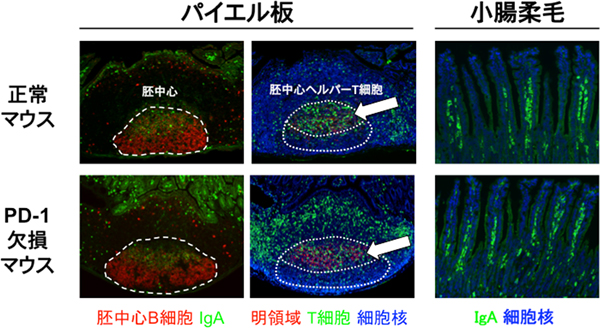
図1 パイエル板と小腸柔毛内のB細胞、T細胞の様子
- 左: 正常のマウスと比較して、PD-1欠損マウスのパイエル板では胚中心(白線)にB細胞(赤色)が多く集まっている。
- 中: 正常のマウスと比較して、PD-1欠損マウスのパイエル板では胚中心(特にB細胞の成熟過程に重要な明領域:矢印の白線内)のT細胞(緑色)を含め、パイエル板全体のヘルパーT細胞の数が多い。
- 右: 正常マウスとPD-1欠損マウスの間で、小腸の柔毛内にあるIgA抗体を産生するB細胞の数(緑色)は差がなく、腸管内に分泌されているIgA抗体の量も差がない。
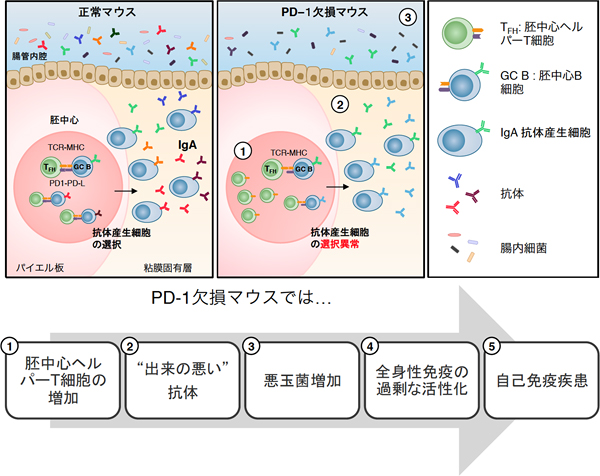
図2 PD-1欠損マウスにおける腸内細菌の様子
PD-1欠損マウスでは、まずパイエル板の胚中心にあるヘルパーT細胞が過剰に増殖する(①)。次に、本来除かれるはずの“出来の悪い”B細胞が生き残り、腸内細菌に結合する力が弱いIgA抗体が腸管内に分泌される(②)。その結果、腸管内の悪玉菌が増殖し腸内細菌のバランスが崩れる(③)。それによって、全身の免疫系が過剰に活性化される(④)。この結果、自己免疫疾患の病態が悪化している可能性がある(⑤)。
