要旨
理化学研究所(理研)生命システム研究センター合成生物学研究グループの上田泰己グループディレクター、鳴海良平テクニカルスタッフⅠ、無細胞タンパク質合成研究ユニットの清水義宏ユニットリーダーらの研究チーム※は、質量分析装置を利用した新しいタンパク質定量法「MS-QBiC(MS-based Quantification By isotope-labeled Cell-free product)」を開発し、マウス肝臓における体内時計[1]に関わるタンパク質(体内時計タンパク質)の量を時系列に沿って測定することに成功しました。また、定量結果がマウスの体内時刻を正確に示していたことから、タンパク質定量による体内時刻の測定方法を合わせて確立しました。
細胞内では、さまざまなタンパク質がさまざまな生体システムを形成し、生体機能をつかさどっています。それら生体システムにおけるタンパク質ネットワークの状態は時間経過とともに刻々と変化するため、それぞれのタンパク質の量的・動的な情報を得ることができれば、生体システムの機能や役割の理解へとつながります。こうした背景から近年、質量分析装置によるタンパク質定量を用いて細胞内の状態を調べる研究が数多く行われています。質量分析装置を用いたタンパク質定量では、安定同位体[2]で標識した参照サンプルの利用が一般的です。今回研究チームが開発したMS-QBiCでは、参照サンプルを安価、かつ即座に合成できるため、多種類のタンパク質の定量解析を効率良く行うことができます。
開発した手法をマウス肝臓における体内時計タンパク質の時系列変化の測定に応用したところ、16種類の体内時計タンパク質の定量解析に成功しました。それらのうち、14種類のタンパク質は24時間周期で増減するという結果が得られました。これら14種類の増減するタンパク質の定量結果を「分子時刻表法[3]」へ応用することによって、特定の時刻における体内時計タンパク質の定量結果から、マウスの体内時刻を測定できることを明らかにしました。
成果は、米国科学アカデミー紀要『Proceedings of National Academy of Science of the United States of America (PNAS)』に掲載されるのに先立ち、オンライン版(5月30日の週)に掲載されます。
※研究チーム
理化学研究所 生命システム研究センター
合成生物学研究グループ
グループディレクター 上田 泰己(うえだ ひろき)
テクニカルスタッフⅠ 鳴海 良平(なるみ りょうへい)
テクニカルスタッフⅠ 鵜飼(蓼沼)磨貴(うかい(たでぬま)まき)
元研究員 大出 晃士(おおで こうじ)(現 東京大学大学院医学系研究科機能生物学専攻助教)
基礎科学特別研究員 神田 元紀(かんだ げんき)
特別研究員 篠原 雄太(しのはら ゆうた)
特別研究員 松本 桂彦(まつもと かつひこ)
無細胞タンパク質合成研究ユニット
ユニットリーダー 清水 義宏(しみず よしひろ)
テクニカルスタッフⅠ 佐藤 文(さとう あや)
背景
細胞中に含まれる特定の酵素や因子などのタンパク質の量を正確に測定することは、その細胞が今どのような状態にあり、どのような機能を担っているかを推定する手掛かりになります。しかし、細胞中には数千~数万種類のタンパク質が混在するため、調べたいタンパク質の相対量は極めて少なくなることが多く、正確な定量が困難となることがあります。こうした問題を解決し、細胞中の極微量なタンパク質の量を高感度に測定する方法として、近年、質量分析装置を利用した定量プロテオミクス[4]と呼ばれる手法が発展しています。
タンパク質を消化酵素トリプシンで分解すると、さまざまなペプチド断片が得られます(図1)。定量プロテオミクスでは、それらの断片の中から定量したい目的のタンパク質だけが持つ特異的なペプチド断片(ターゲットペプチド)の濃度を測定することによって、元のタンパク質の定量を行います。定量プロテオミクスの中でも絶対定量法と呼ばれる手法は、あらかじめ濃度が判明している安定同位体で標識したターゲットペプチドを参照サンプルとして用い、質量分析で得られる目的のサンプルと参照サンプルのシグナル強度(質量/電荷)の比較をもとに、目的のサンプルの濃度を決定します(図1)。そのため、濃度が判明している参照サンプルがあれば、さまざまなタンパク質を高感度に定量できます。
そこで、研究チームは質の高い参照サンプルを安価に、かつ即座に合成し、多種類のタンパク質の定量を簡便に行うことができる手法の開発に取り組みました。
研究手法と成果
(1)新しいタンパク質定量法「MS-QBiC」の開発
これまで参照サンプルを調製するには、安定同位体で標識したアミノ酸を基質として用いた化学合成や、同じアミノ酸を含む培地を利用して育てた細胞を利用するなどの工夫がなされてきました。しかし、安定同位体で標識したアミノ酸は高価なため、多種類の参照サンプルの調製にとって障壁となっていました。また、細胞を利用した参照サンプルの調製では、細胞内の代謝酵素によって、安定同位体で標識したアミノ酸が別のアミノ酸に変化することがあるため、正確な定量を行えないなどの問題がありました。
そこで、研究チームは、PUREシステム[5]という手法を参照サンプルの合成に利用することによって、質の高い参照サンプルを安価に、かつ即座に合成することを目指しました。PUREシステムは、細胞内におけるタンパク質合成システムの中から必要な要素(リボソームや翻訳因子など)のみを取り出し、試験管内において再構成する技術です。試験管内にはペプチド分解酵素や代謝酵素などが含まれないため、安定同位体で標識した参照サンプルを高い効率で合成できます。この手法で参照サンプルを合成するには、PCR法[6]によって得られたDNA断片を試験管に添加するだけでよく、少ない液量で複数の参照サンプルを同時に合成できるため、非常に安価に多種類の参照サンプルを調製することが可能です。
研究チームは、PUREシステムで調製した参照サンプルを用いて目的のタンパク質の定量を行うことができることを確認し、構築したタンパク質定量法を「MS-QBiC (MS-based Quantification By isotope-labeled Cell-free product)」と名付けました(図2)。
(2)MS-QBiCによる体内時計タンパク質の量の時系列変化の測定
生物には体内時計と呼ばれる24時間周期を作り出すメカニズムが備わっており、このメカニズムにはさまざまなタンパク質が関与していることが知られています(図3)。細胞内におけるこれら体内時計タンパク質の1日における濃度変化を調べることにより、24時間周期が作り出されるメカニズムをより深く知ることできると考えられます。
研究チームはマウス肝臓由来の20種類の体内時計タンパク質をターゲットにし、120種類の参照サンプルを用いて、MS-QBiCによりそれぞれのタンパク質の24時間における量的変化を解析しました。その結果、47種類の参照サンプルによって16種類の体内時計タンパク質を定量することに成功しました。それら16種類のタンパク質のうち、14種類のタンパク質は24時間周期で増減していることが分かりました。また、体内時計タンパク質をコードするメッセンジャーRNA(mRNA)[7]量の増減と体内時計タンパク質そのものの増減のタイミングが必ずしも一致していないことから、mRNA量だけでなく、タンパク質の量そのものを測定することが体内時計の理解にとって非常に重要であることが示されました。
(3)タンパク質定量結果にもとづくマウスの体内時刻の測定
これまでに、合成生物学研究グループ(上田泰己グループディレクター)では、24時間周期で増減する体内物質の定量結果にもとづいて体内時刻を測定できる「分子時刻表法」を開発してきました。分子時刻表法は、体内においてどの時刻に特定の体内物質がどの程度の量になるかをあらかじめ測定し、分子時刻表を作成することによって、特定の時刻における体内物質の量から体内時刻を測定する技術です。この技術によって、これまでに24時間周期で増減するmRNA量や、代謝産物量の定量結果にもとづいた体内時刻の測定を行ってきました。
研究チームは、MS-QBiCによって得られたタンパク質の定量結果から分子時刻表を作成することによって、特定の時刻における体内時計タンパク質の定量結果からマウスの体内時刻を測定できることを明らかにしました。
今後の期待
MS-QBiCは、体内時計の解析にとどまらず、生体内のさまざまなタンパク質ネットワークの量的・動的な記述によりそれらの定量的な理解へと役立つと期待できます。
また、体内時計タンパク質の1日における量的な変化を詳しく見積もることができるため、データをもとに体内時計の転写・翻訳ネットワークのシミュレーションによる再構築などによって、体内時計のリズムを生み出す原理の解明などへの貢献が期待できます。
さらに、これまでの研究で明らかにされたmRNAおよび代謝産物の量的情報に加え、タンパク質の量的情報も体内時刻を正確に指し示すことが分かったため、これらの情報を複合した、より正確な体内時刻の測定方法の開発などにつながると期待できます。
原論文情報
- Ryohei Narumi, Yoshihiro Shimizu, Maki Ukai-Tadenuma, Koji L. Ode, Genki N. Kanda, Yuta Shinohara, Aya Sato, Katsuhiko Matsumoto, and Hiroki R. Ueda, "Mass spectrometry-based absolute quantification reveals rhythmic variation of mouse circadian clock proteins.", Proceedings of National Academy of Science of the United States of America (PNAS), doi: 10.1073/pnas.1603799113
発表者
理化学研究所
生命システム研究センター 細胞デザインコア 合成生物学研究グループ
グループディレクター 上田 泰己(うえだ ひろき)
テクニカルスタッフⅠ 鳴海 良平(なるみ りょうへい)
生命システム研究センター 細胞デザインコア 合成生物学研究グループ 無細胞タンパク質合成研究ユニット
ユニットリーダー 清水 義宏(しみず よしひろ)
 上田 泰己
上田 泰己
 鳴海 良平
鳴海 良平
 清水 義宏
清水 義宏
報道担当
理化学研究所 広報室 報道担当Tel: 048-467-9272 / Fax: 048-462-4715
補足説明
- 1.体内時計
生体内において24時間周期を作り出すメカニズムを形成するシステム。バクテリアからヒトまで数多くの生物種に存在する。ホルモンの分泌や代謝、睡眠など、24時間周期で起こるさまざまな生理機能に影響を及ぼす。 - 2.安定同位体
陽子と電子の数は同じであるが、中性子の数が異なるため、同じ性質を持つが質量が異なる原子(同位体)のうち、自然界で安定に存在することのできるものを指す。本研究では、原子量が15(通常は14)の窒素原子および原子量が13(通常は12)の炭素原子を持つアミノ酸を利用している。 - 3.分子時刻表法
植物学者・カール・フォン・リンネが考案した「リンネの花時計」にヒントを得て構築した、24時間周期で量が増減する生体内物質量を指標とした体内時刻の測定法。これまでに、細胞中のmRNA量や、血中の代謝物などを指標に体内時刻を測定する技術を開発している。- 2004年8月12日CDBニュース「あなたは今何時?」
- 2009年5月26日プレスリリース「代謝産物から「体内時刻」を簡便かつ定量的に測定する新手法を確立」
- 2012年8月28日プレスリリース「ヒトの血液から簡単に「体内時刻」を調べる手法を確立」
- 4.定量プロテオミクス
質量分析装置などを利用してタンパク質を対象とする大規模な解析を行う研究(プロテオミクス)から派生した技術で、質的な情報だけでなく、量的な情報も含む解析を行う技術。 - 5.PUREシステム
細胞内のタンパク質合成過程を試験管の中で再現する技術である無細胞タンパク質合成システムを応用し、必要な要素のみを1つずつ精製し、試験管内において再構成する技術。DNA分子をPUREシステムに添加することにより、DNAにコードされたタンパク質やペプチドを合成することができる。 - 6.PCR法
ポリメラーゼ連鎖反応法。少量のDNAを鋳型にして、DNA複製酵素および短い単鎖DNAを用いて、鋳型DNAを大量増幅する手法。PCRはPolymerase chain reactionの略。 - 7.メッセンジャーRNA(mRNA)
生物の体内では多くのタンパク質が働いているが、タンパク質は核内のDNA配列の遺伝子にあたる部分がRNAという形でコピーのように写し取られ(転写)、それが読み出される(翻訳)ことで作られる。この転写されたRNAをmRNA(メッセンジャーRNA)と呼ぶ。
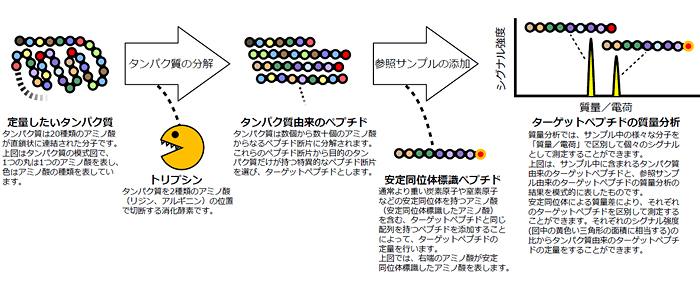
図1 質量分析を利用したタンパク質定量の流れ
定量したいタンパク質をトリプシンで分解し、質量分析装置を用いて参照サンプルと同時に解析することによって、目的のタンパク質の定量を行う。
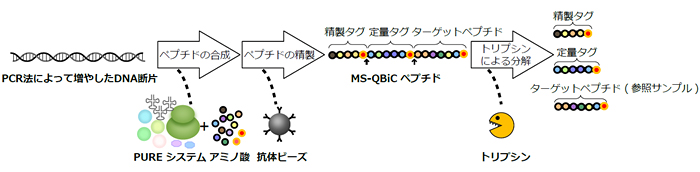
図2 MS-QBiCによるタンパク質定量
PCR法によって増やしたDNA断片にコードされた参照サンプルを含むペプチドを、PUREシステムによって合成する。このとき、安定同位体で標識したアミノ酸を入れておくことで、参照ペプチドに安定同位体で標識したアミノ酸が含まれるようにする。合成したペプチドにある精製タグと抗体ビーズの親和性を利用してペプチドを精製した後、トリプシンによる分解を行い、精製タグ、定量タグ、ターゲットペプチド(参照サンプル)の3者に分離する。得られた定量タグを合成したターゲットペプチドの定量に、ターゲットペプチドを参照サンプルとして用いる。
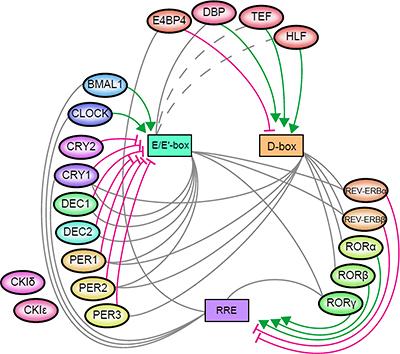
図3 定量解析を行ったマウスの体内時計タンパク質
体内時計システムにおいては、さまざまな体内時計タンパク質が図のように複雑なネットワークを形成している。体内時計タンパク質を合成するための3つの制御配列、朝配列(E/E'-box)、昼配列(D-box)、夜配列(RRE)を体内時計タンパク質自身が活性化(緑色)または不活性化(ピンク色)し、それぞれの制御配列の下流(灰色)にコードされている体内時計タンパク質の合成を制御することによって、24時間周期を作り出すメカニズムを生み出している。また、一部の体内時計タンパク質の活性はCKIδ、CKIεによって制御されている。本研究では、図に示した20種類の体内時計タンパク質について定量解析を行い、16種類の体内時計タンパク質の定量解析に成功した。
