理化学研究所(理研)環境資源科学研究センターバイオ高分子研究チームのヌル・アリア・オクタビアニ特別研究員、沼田圭司チームリーダー、放射光科学研究センターNMR先端応用・外部共用チームの松上明正研究員、林文晶上級研究員らの研究チームは、クモ糸の紡糸過程において、種々のイオンがシルクタンパク質に及ぼす影響を明らかにしました。
本研究成果は、クモ糸の紡糸機構を明らかにする一連の研究や、人工的に強靭なクモ糸を製造する技術開発に貢献すると期待できます。
従来のクモ糸の紡糸過程において、どのようなイオンがシルクタンパク質の構造に寄与しているかは分かっていませんでした。
今回、研究チームは、クモ糸の主成分であるシルクタンパク質が持つ非晶領域と結晶領域の繰り返し配列を遺伝子組換え技術[1]で合成し、クモ糸が形成される直前の溶液状態を試験管内で再現しました。異なるイオンを含む環境下でシルクタンパク質の分子構造を解析した結果、ナトリウムイオンなどのカオトロピックイオン[2]には、シルクタンパク質の分子内および分子間相互作用を抑制し、シルクタンパク質を溶かす効果がある一方、リン酸イオンなどのコスモトロピックイオン[2]は、アミノ酸残基のグリシン[3]を多く含む領域における水素結合の形成を促進し、ベータシート構造[4]の形成に必須であることが分かりました。
本研究は、英国の科学雑誌『Chemical Communications』オンライン版(7月29日付け)に掲載されました。
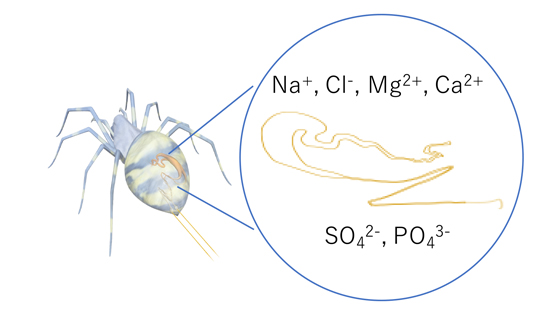
図 クモ糸の紡糸過程における、さまざまなイオンがシルクタンパク質の構造に与える影響
※研究支援
本研究は、革新的研究開発推進プログラム(ImPACT)「超高機能構造タンパク質による素材産業革命(プログラム・マネージャー:鈴木隆領、研究課題責任者:沼田圭司)」の支援を受けて実施されました。
背景
クモやカイコなど一部の生物種が生産する糸には、特異的な物性があります。なかでも、クモが獲物を素早く捕まえるときや、危機に遭遇して逃げるときに命綱として使う「牽引糸(けんいんし)」は、軽量でありながら鉄以上の強靭さがあり、高強度構造材料など幅広い分野への応用が期待されています。
クモ糸の主成分であるシルクタンパク質は、その両末端であるN末端[5]とC末端[5]の構造がつながることで、クモ糸の形成が進行することが知られています(図1)。この紡糸過程の分子構造の変化には、イオンが重要な役割を果たしていると考えられてきましたが、具体的な分子構造やイオンの種類などは報告されていませんでした。
研究手法と成果
研究チームは、まず、シルクタンパク質の硬い結晶領域と柔らかい非晶領域の繰り返し配列を、大腸菌を用いた遺伝子組換え技術により合成し、クモ糸が形成される直前の溶液状態を試験管内で再現しました。そして、シルクタンパク質の分子構造を溶液核磁気共鳴分光法[6]を用いて調べました。特に、イオンの種類と濃度の異なる複数の条件において、シルクタンパク質の分子構造とダイナミクスを評価することで、イオンの効果を明らかにすることを目指しました。
その結果、クモ糸が形成される直前の溶液状態のシルクタンパク質は、カオトロピックイオン(ナトリウムイオン、塩化物イオン、マグネシウムイオン、カルシウムイオンなど)により分子内および分子間相互作用が抑制された結果、疎水性の分子構造を持ち、非常に高濃度で存在するにもかかわらず、クモ体内の水によく溶解することを見いだしました。一方で、コスモトロピックイオン(リン酸イオン、硫酸イオンなど)は、アミノ酸残基のグリシンを多く含む領域における水素結合の形成を促進し、糸を形成する際に生じるベータシート構造の形成に必須であることが明らかになりました(図2)。
今後の期待
本研究では、遺伝子組換え技術で解析に適したシルクタンパク質を合成したため、報告したベータシート構造の形成機構が全てのクモ糸に該当するかについては、さらなる研究が必要です。しかし、イオンがその種類や役目により、クモ糸の形成に大きく関与していることは明らかです。特に、クモの体内で、疎水性のシルクタンパク質が高濃度で可溶状態を維持していることを、イオンの効果によって説明することもできます。従って、本研究成果を強靭な人工クモ糸の分子設計や合成プロセスに生かすことが可能になり、産業への利用も期待できます。
原論文情報
- Nur Alia Oktaviani, Akimasa Matsugami, Fumiaki Hayashi, Keiji Numata, "Ion effects on the conformation and dynamics of repetitive domains of a spider silk protein: implications for solubility and β-sheet formation", Chemical Communications, 10.1039/C9CC03538A
発表者
理化学研究所
環境資源科学研究センター バイオ高分子研究チーム
特別研究員 ヌル・アリア・オクタビアニ(Nur Alia Oktaviani)
チームリーダー 沼田 圭司(ぬまた けいじ)
放射光科学研究センター NMR研究開発部門 NMR応用・利用グループ NMR先端応用・外部共用チーム
上級研究員 林 文晶(はやし ふみあき)
研究員 松上 明正(まつがみ あきまさ)
 ヌル・アリア・オクタビアニ
ヌル・アリア・オクタビアニ
 松上 明正
松上 明正
報道担当
理化学研究所 広報室 報道担当
Tel: 048-467-9272 / Fax: 048-462-4715
お問い合わせフォーム
産業利用に関するお問い合わせ
補足説明
- 1.遺伝子組換え技術
本研究では大腸菌を用いて遺伝子組換えを行った。目的のタンパク質に対応した遺伝子を大腸菌に導入した後に、その大腸菌を培養することで、目的のタンパク質を合成させる。 - 2.カオトロピックイオン、コスモトロピックイオン
カオトロピックイオンは、水分子間の相互作用を減少させることでタンパク質の構造を不安定化させるイオンである。コスモトロピックイオンは、逆に、水素結合の形成などによりタンパク質の構造などを安定化させるイオン。 - 3.グリシン
グリシンはアミノ酸の一つ。クモ糸を構成するシルクタンパク質の場合、非晶領域に多く存在する傾向にある。 - 4.ベータシート構造
ベータシート構造はタンパク質が構築する二次構造の一つで、互い違いに隣り合ったいくつかのポリペプチド鎖が、水素結合により形成する平面状の構造のこと。クモ糸が特性として持つ高強度の由来となる、結晶構造を形成する。 - 5.N末端、C末端
タンパク質はアミノ酸がつながったポリマーであり、隣接するアミノ酸は、それぞれのアミノ基とカルボキシル基がペプチド結合をしている。このポリマーの末端のフリーのアミノ基側をN末端、カルボキシル基側をC末端と呼ぶ。 - 6.溶液核磁気共鳴分光法
核磁気共鳴を利用して水溶液中の分子の構造や運動性を調べる手法。

図1 シルクタンパク質の模式図
シルクタンパク質は、N末端とC末端の間に結晶領域(結晶化した硬い領域=ベータシート構造、グレー)と非晶領域(結晶化していない軟らかい領域、ピンク)が交互に繰り返してできている。N末端とC末端の構造が分子間の相互作用に寄与し、糸の形成が進行することが知られている。
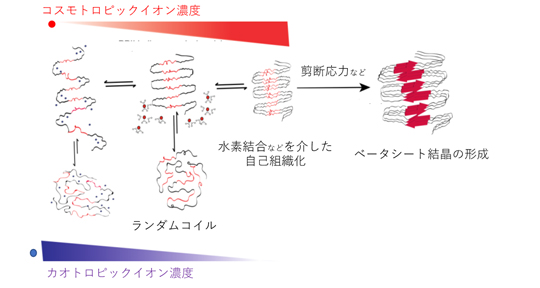
図2 シルクタンパク質の繰り返し構造がイオンから受ける影響の模式図
シルクタンパク質の繰り返し構造は、カオトロピックイオン(ナトリウムイオン、塩化物イオン、マグネシウムイオン、カルシウムイオンなど)により、ランダムコイル(特定の二次構造を示さない状態)として水に可溶な状態を維持している。一方で、紡糸過程が進み、カオトロピックイオンが減少し、コスモトロピックイオン(リン酸イオン、硫酸イオンなど)が増加することで、糸の形成に必要なベータシート構造を形成する。
