理化学研究所(理研)開拓研究本部 染谷薄膜素子研究室の福田 憲二郎 専任研究員(創発物性科学研究センター 創発ソフトシステム研究チーム 専任研究員)、染谷 隆夫 主任研究員(同チームリーダー)の国際共同研究グループは、開発した厚さ約1.3マイクロメートル(μm、1μmは1,000分の1mm)の伸縮可能な導体が皮膚および臓器(神経)へ良好に密着し、生体情報を取得するためのセンサー用電極として使用可能であることを実証しました。
本研究成果は、今後、生体組織に匹敵する柔らかいセンサーを開発することで、伸縮性が高く耐久性に優れた次世代生体適合性エレクトロニクスの応用につながるものと期待できます。
今回、国際共同研究グループは、厚さ約1μmのシリコーンゴム[1]基板上にマイクロクラック構造[2]を持つ金を成膜することで、伸縮性に優れた導体を開発しました。この極薄伸縮性導体は導電性を維持しながら、約300%の引張ひずみ[3]を示し、ヒトの皮膚やラットの神経と良好に密着します。薄いイオン伝導性ポリマー[4]層と組み合わせると、水中でも皮膚に強い接着性を示し、手洗いなどの日常生活や水泳などの激しい運動中でも心電図を安定に計測できました。また、神経へ電気的刺激を与え、生体信号を高い信号対ノイズ比[5]で取得するといった、体内埋め込み型の電極としての可能性も実証しました。
本研究は、科学雑誌『Nature Electronics』オンライン版(11月21日付け)に掲載されました。
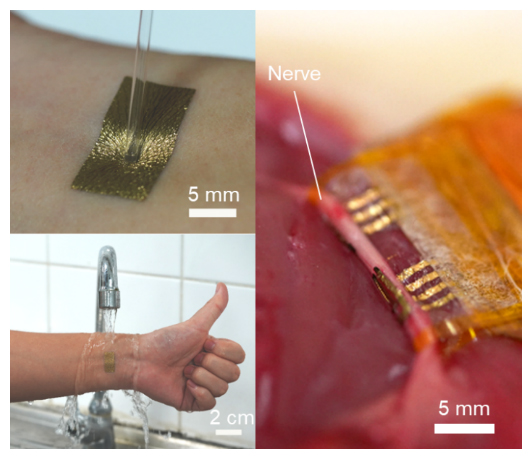
ヒトの皮膚(左)やラットの神経(右)に貼り付けた極薄伸縮性導体(金色の部分)
背景
近年、ウェアラブルおよび体内埋め込み型デバイスの研究開発が急速に進んでいます。そのようなデバイスの究極の目標は通常の活動を妨げることなく、ヒトの健康に必要な計測や治療を長期間提供することです。この目標を達成するには、超薄型かつ伸縮性のセンサーが必要となってきます。ヒトの感覚系では知覚できないほど薄いセンサーであれば、装着負荷を与えずに済みます。高い伸縮性があれば、デバイスの剛性を軟組織の剛性に匹敵するほど小さくすることができ、装着時や計測時に引張ひずみなどの機械的変形を受けて素子が破壊されることを防ぐことができます。
デバイスと組織の間の機械的特性を一致させることで、このような超薄型伸縮性センサーは、体内に埋め込まれても通常と同様の組織応答を誘発すると予想されます。このような皮膚や臓器への適合性や接着性は、神経へ電気刺激を与え生体信号を測定することに重要な役割を果たします。
このようなセンサーに不可欠な部品が、極薄かつ伸縮性のある導体です。皮膚上および体内埋め込み型デバイスの用途では、取り扱い中や使用時の損傷を防ぐために、安定した導電性を維持しながら、引張ひずみ100%以上の伸縮性を提供する必要があります。このような極薄の伸縮性導体作製への有望なアプローチの一つは、薄い弾性基板に金属の「マイクロクラック構造」を作製することです。マイクロクラック構造では表面に微細なクラック(亀裂)が入っており、引張ひずみを加えたときにそのクラックに沿って金属が伸びて、金属破断の発生を防ぎます。しかし、マイクロクラック構造に基づく極薄伸縮性導体の作製ための合理的な設計手法はこれまでありませんでした。
研究手法と成果
国際共同研究グループは、厚さ約1.2マイクロメートル(μm、1μmは1,000分の1mm)のシリコーンゴムのポリジメチルシロキサン(PDMS)基板上に、導電層として厚さ約50ナノメートル(nm、1nmは100万分の1mm)の金を成膜した極薄の弾性導体を設計し、作製しました。この導体の総膜厚は約1.3μmで、導電率を失うことなく最大300%の引張ひずみまで伸ばすことができます(図1)。
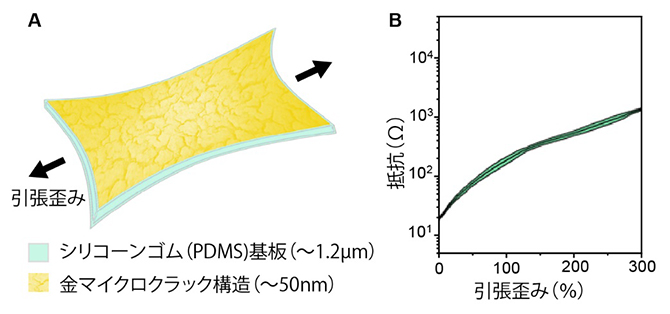
図1 シリコーンゴム(PDMS)と金のマイクロクラック構造に基づく極薄伸縮性導体
- (A)導体の構造図。
- (B)引張ひずみを加えたときの導体の電気抵抗の変化。引張ひずみ300%でも電流が流れる。
この極薄導体の優れた伸縮性の重要な理由は、熱蒸発プロセス中に金のマイクロクラック構造を形成したことです。PDMSと金の熱膨張率の違いにより、金の熱蒸着中にPDMS層は熱膨張して変形し、成膜された金にマイクロクラック構造が形成されることが知られています。この変形は主にPDMS層の厚さに依存し、厚さ約1μmのPDMSでは十分な膨張が発生せず、金マイクロクラック構造は形成されません(図2A、B)。これを解決するために、厚さ約100μmの厚いPDMSサポート層を厚さ約1μmのPDMSの下に挿入し、金を蒸着させる手法を考案しました。薄いPDMS基板と接触している厚いPDMS層によって十分な熱変形が起き、薄いPDMS上に金にマイクロクラック構造を形成することに成功しました(図2C、D)。
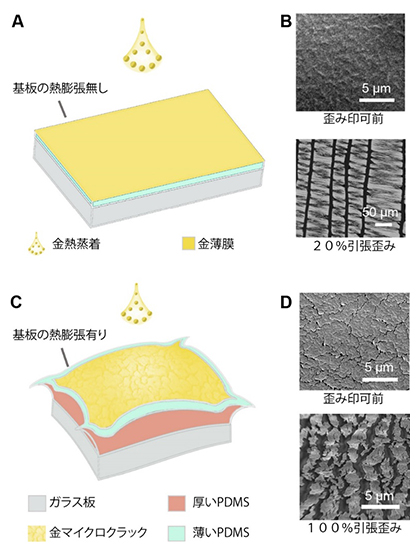
図2 金マイクロクラック構造の形成メカニズム
- (A)厚いPDMSサポート層を使用しない場合、金蒸着中に薄いPDMSに十分な熱膨張が発生せず、マイクロクラック構造は形成されない。
- (B)0%および20%の引張ひずみを加えたときの導体の走査電子顕微鏡(SEM)画像。20%のひずみを加えると、ひずみ方向に垂直の向きに金が破断し、導電性が失われる。
- (C)厚いPDMSサポート層を薄いPDMSの下に挿入し、金蒸着中のPDMSの熱膨張を誘発する。
- (D)0%および100%の引張ひずみを加えたときのSEM画像。金にマイクロクラック構造が形成されているため、100%のひずみを加えても金は破断しない。
次に、極薄伸縮性導体を皮膚上の心電図計測用の電極として利用する実験を行いました。皮膚上で使用するには、デバイスと皮膚が良好に接着することが重要です。金電極表面を薄い粘着性のイオン導電性ポリマー層(p(DM-co-AA-co-MEA):pDAM)でコートすることで、極薄伸縮性導体と皮膚の間の接着性を大幅に改善しました(図3A、B)。その結果、手を洗った後や、ランニングや水泳などの激しい運動の後、8時間連続着用後でも、この極薄伸縮性導体を利用して心電図信号を継続的かつ安定的に記録できました(図3C)。
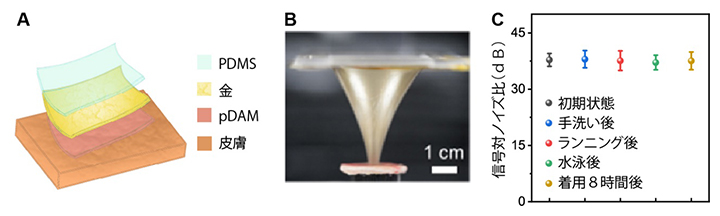
図3 皮膚上の心電図計測用電極としての利用
- (A)構造の概略図。皮膚と金の間に、pDAMというイオン導電性ポリマー層を挿入する。
- (B)下側のブタの皮膚の表面に極薄伸縮性導体を接着させた後、剥がす動作を行っている最中の電極の様子。皮膚と強固に接着しているため、金が大きく引き伸ばされながら接着性を保持している様子が観察された。
- (C)手洗い、ランニング、水泳、長時間の着用など、さまざまな条件で記録された心電図信号の信号対ノイズ比の比較。
最後に、極薄伸縮性導体が体内に埋め込み可能なニューラルインターフェース(ヒトと機械の間で情報をやり取りするためのツール)として利用できるか検証しました。極薄伸縮性導体は、ラットの神経と良好なインターフェースを形成しました(図4A)。
厚い電極および極薄伸縮性導体を用いてラットの神経に電気刺激を与え、刺激された筋肉の生体信号(複合神経活動電位)を計測しました。すると、極薄伸縮性導体の方が厚い電極よりも、筋肉を活性化させるための電気刺激に必要な電流値が有意に低いことが分かりました(図4B)。また、刺激によって発生する生体信号の強度も極薄伸縮性導体の方が大きく、かつ測定した生体信号の信号対ノイズ比が大幅に向上しました(図4C)。これらの結果から、極薄伸縮性導体は神経などの体内の臓器へ隙間なく強固に密着することで、電気刺激伝達や生体信号記録の双方の性能を向上させることが明らかになりました。
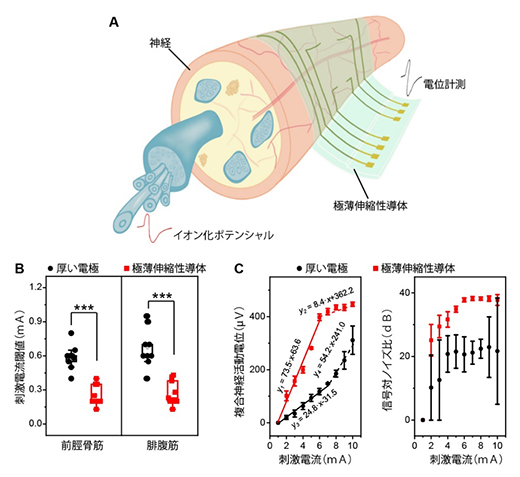
図4 体内埋め込み型ニューラルインターフェース
- (A)神経に接続された極薄伸縮性導体の概略図。薄さと柔らかさのおかげで、極薄伸縮性導体は神経と良好な接触を形成する。
- (B)神経を電気刺激し、筋肉(前脛骨筋、腓腹筋)を活性化するための閾値刺激電流の比較。極薄電極の方が厚い電極よりも有意に低い電流で電気刺激を与えられた。
- (C)極薄電極と厚い電極で記録された生体信号(複合神経活動電位)の強度(左)と信号対ノイズ比(右)の比較。
今後の期待
本研究では、厚さ約1μmという極薄のゴム基板上に伸縮性導体を形成することを可能にしました。この極薄伸縮性導体は、皮膚上で安定に機能する生体信号取得センサーおよび、体内埋め込み可能なニューラルインターフェースとして利用できます。さらに、ソフトロボティクスやMEMS(微小な電子機械システム)などの他の分野においても、有望なアプリケーションを見つけられる可能性があります。
ただし、極薄伸縮性導体の制限の一つは引き伸ばされると電気抵抗が増加する(電流が流れにくくなる)ことであり、これは固体導体に本質的なものです。しかし今後、伸縮性ポリマーや液体金属などを用いた新素材と組み合わせることで、電気抵抗の変化を最小化することが可能です。また、構造工学的手法を利用し機械的特性をさらに改善することで、電子デバイスと生体とのインターフェースがさらに改善されると期待できます。
補足説明
- 1.シリコーンゴム
シリコーンを主成分とする樹脂。液体の状態に触媒を加えると、シリコーンの重合反応により硬化し、ゴム状になる。 - 2.マイクロクラック構造
微小な亀裂を持つ構造のこと。本研究では、このような微小な亀裂が金の表面にあらかじめ形成されることにより、引張ひずみが加わったときに亀裂によって力を分散させ、金属が完全に破断することを防いでいる。 - 3.引張ひずみ
物体を引張る向きに力を加えたときに、その力の方向に生じる変形(ひずみ)のこと。 - 4.イオン伝導性ポリマー
電解質をイオンに解離し、移動させることができる高分子材料。 - 5.信号対ノイズ比
一般的には、測定時のシグナル(信号)とノイズ(雑音)の比率を示す。信号対ノイズ比が大きいほど、精度の高い測定データが得られる。SN比ともいう。
国際共同研究グループ
理化学研究所
開拓研究本部 染谷薄膜素子研究室
専任研究員 福田 憲二郎(フクダ・ケンジロウ)
(創発物性科学研究センター 創発ソフトシステム研究チーム 専任研究員)
主任研究員 染谷 隆夫(ソメヤ・タカオ)
(創発物性科学研究センター 創発ソフトシステム研究チーム チームリーダー、東京大学大学院 工学系研究科 教授)
特別研究員(研究当時)ジャン・ジ(JIANG Zhi)
創発物性科学研究センター 創発ソフトシステム研究チーム
基礎科学特別研究員(研究当時)ゾン・ジュンウェン(ZHONG Junwen)
シンガポール南洋理工大学
教授 チェン・シャオドン(CHEN Xiaodong)
シンガポール国立大学
教授 リウ・シャオガン(LIU Xiaogang)
東京大学大学院 工学系研究科 電気系工学専攻
准教授 横田 知之(ヨコタ・トモユキ)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費助成事業新学術領域研究「弾性グラディエントナノ薄膜を利用した自由変形可能な太陽電池の創成(研究代表者:福田憲二郎)」、同基盤研究(S)「拍動する心筋細胞シートを用いた伸縮性多点電極アレイによる薬物反応の評価(研究代表者:染谷隆夫)」による助成を受けて行われました。
原論文情報
- Zhi Jiang, Nuan Chen, Zhigao Yi, Junwen Zhong, Feilong Zhang, Shaobo Ji, Rui Liao, Yan Wang, Haicheng Li, Zhihua Liu, Yang Wang, Tomoyuki Yokota, Xiaogang Liu, Kenjiro Fukuda, Xiaodong Chen, and Takao Someya, "A 1.3-micrometre-thick elastic conductor for seamless on-skin and implantable sensors", Nature Electronics, 10.1038/s41928-022-00868-x
発表者
理化学研究所
開拓研究本部 染谷薄膜素子研究室
専任研究員 福田憲二郎(フクダ・ケンジロウ)
(創発物性科学研究センター 創発ソフトシステム研究チーム 専任研究員)
主任研究員 染谷 隆夫(ソメヤ・タカオ)
(創発物性科学研究センター 創発ソフトシステム研究チーム チームリーダー、東京大学 大学院工学系研究科 教授)
 福田 憲二郎
福田 憲二郎
 染谷 隆夫
染谷 隆夫
報道担当
理化学研究所 広報室 報道担当
お問い合わせフォーム
