理化学研究所(理研)生命医科学研究センター 粘膜システム研究チームの大野 博司 チームリーダー、柴田 涼平 客員研究員らの共同研究グループは、小児の牛乳アレルギーに対する経口免疫療法[1]において、便中のビフィドバクテリウム科[2]を中心とした細菌群が多いことが、アレルギー反応の抑制の維持(持続的無反応[3]の獲得)と関連することを明らかにしました。
本研究成果は、経口免疫療法の作用メカニズムの解明や、腸内細菌[4]を標的とした併用療法の開発に貢献することが期待されます。
食物アレルギーの基本的な対処法は、アレルゲン[5]の除去のみでした。しかし、近年、経口免疫療法の有効性が報告されています。経口免疫療法はアレルゲンを少量から徐々に増やして摂取することで、免疫寛容[6]を誘導します。また、免疫寛容において腸内環境が重要であることが報告されていましたが、小児の牛乳アレルギーに対する経口免疫療法と腸内環境の関連についての報告はありませんでした。
今回、共同研究グループは、多施設で経口免疫療法を受けた牛乳アレルギーを持つ小児の腸内細菌・便中代謝物[7]のデータから、便中ビフィドバクテリウム科を中心とした細菌群が多いほど牛乳に対する持続的無反応を獲得する可能性が高いことを明らかにしました。
本研究は、科学雑誌『Allergology International』オンライン版(11月1日付:日本時間11月1日)に掲載されました。
背景
牛乳アレルギーは、小児における最も一般的な食物アレルギーの一つです。多くの患児では3~5歳までに自然に治る可能性があります。ただ、そうでない場合、重篤なアレルギー反応の恐れがあるため、牛乳の摂取を避け続けなければなりません。
近年、食物アレルギーの治療法として、経口免疫療法が効果的であることが、臨床試験で示されています。しかし、牛乳アレルギーに対する経口免疫療法は、特に治療中に重篤なアレルギー反応のリスクが高いことが問題となっています。また治療を続けている間、つまり牛乳を摂取している間はアレルギー反応が抑制されますが、治療終了後にアレルギー反応の抑制状態である免疫寛容を維持すること(持続的無反応を獲得すること)は、他の食物アレルギー(鶏卵・ピーナッツなど)に比べて難しいことが分かってきました。
最近の研究で、食物アレルギーに対する耐性の獲得において、腸内環境(腸内細菌および便中代謝物)の重要性が報告されています。しかし、経口免疫療法における腸内環境に関する報告は限られていました。
そこで本研究では、牛乳アレルギーを持つ5~15歳の小児32人を対象に、経口免疫療法と腸内環境要因、持続的無反応の獲得との関連性を評価しました。
研究手法と成果
共同研究グループはまず、経口免疫療法中の臨床因子の評価を行いました。本研究の対象とした、経口免疫療法を受けた小児32人のうち、4人が重篤な副作用などにより治療を中止し、残り28人が13カ月間の治療を終了しました。治療中、牛乳または牛乳に多く含まれるたんぱく質であるカゼインに対する特異的IgE値[8]など、牛乳アレルギーのマーカーの値は改善していました。しかし、その後に2週間牛乳の摂取を中断した後に受けた食物負荷試験[9]で目標値を超える牛乳を摂取できた、つまり持続的無反応を獲得したのは7人のみでした。
次に、経口免疫療法中の腸内環境の評価を行いました。経口免疫療法を受けた小児の便中から細菌を検出し、これを腸内細菌の指標としました。変動パターンが似ている腸内細菌や便中代謝物をモジュールというグループにまとめて解析したところ、経口免疫療法中に腸内細菌モジュールおよび代謝物モジュールは大きく変動しており、その変動は特に治療初期に大きいことが分かりました。また、腸内細菌はバクテロイデス科を中心としたモジュール、便中代謝物は脂肪酸を中心としたモジュールの変動が大きいことが分かりました。
続いて、臨床因子と腸内環境因子のうち、経口免疫療法による持続的無反応の獲得に関連する因子を評価しました。治療前の小児の臨床因子では、アトピー性皮膚炎または喘息の治療を併せて受けていることと、牛乳およびカゼイン特異的IgE値が高いと、持続的無応答の獲得率が低い傾向にあることが分かりました。一方、腸内環境因子では、治療開始前のビフィドバクテリウム科を中心としたモジュールの豊富さと、持続的無反応の高い獲得率が関連していました(図左)。また、治療開始3カ月後、13カ月後、および牛乳摂取中止2週間後の時点での牛乳・カゼイン特異的IgE値およびビフィドバクテリウム科を中心としたモジュールの豊富さに対しても、持続的無反応の獲得との関連性が認められました。さらに、ビフィドバクテリウム科を中心とした腸内細菌モジュールは、持続的無反応を獲得している群で、治療中に増加する傾向にありました(図右)。
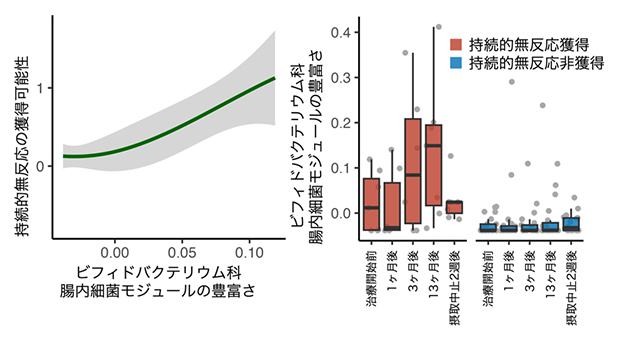
図 腸内細菌モジュールと持続的無反応獲得の関連性
- (左)治療開始前のビフィドバクテリウム科腸内細菌モジュールが豊富なほど、牛乳に対する持続的無反応獲得の可能性が高かった。
- (右)持続的無反応獲得群では、治療中にビフィドバクテリウム科腸内細菌モジュールが増加する傾向にあった。
最後に、経口免疫療法による持続的無反応の獲得および持続的無反応の獲得に関連していた因子が、他の腸内環境モジュールとどのような関係にあるかを評価しました。これらの持続的無反応の獲得に関連する因子は、腸管保護的な役割や糖類の産生に関わる他の腸内環境モジュールとの関係性が強いことが分かりました。
今後の期待
本研究は、牛乳アレルギーを持つ小児において、経口免疫療法中の腸内環境の変化および持続的無反応に関連する腸内環境因子を明らかにしました。この成果は、経口免疫療法が免疫寛容を誘導するメカニズムの解明や、経口免疫療法における腸内細菌をターゲットとした併用療法の開発に貢献すると期待されます。
補足説明
- 1.経口免疫療法
アレルギーの原因となる物質を少量から経口摂取し、徐々に増量することで、アレルギー反応を起こしづらくする治療で、主に食物アレルギーに対して行われる。 - 2.ビフィドバクテリウム科
いわゆるビフィズス菌と言われるBifidobacterium属を含む細菌の分類。疾患の予防や改善との関連性が多く報告されている。 - 3.持続的無反応
経口免疫療法実施中、つまりアレルギーの原因となる物質の経口摂取中だけではなく、その摂取を一定期間中断した後も、アレルギー反応の起きにくい状態を維持できている状態。治癒とは異なる。 - 4.腸内細菌
ヒトの消化管内には多種類・多数の細菌が存在して腸内細菌叢を形成し、免疫システムの調節などの機能があり、健康の維持や疾患の発症に大きく関与していることが報告されている。 - 5.アレルゲン
アレルギー反応を引き起こす原因物質のこと。小児の食物アレルギーにおいては牛乳をはじめ鶏卵、ピーナッツなどが代表的なアレルゲンである。 - 6.免疫寛容
自己と非自己、生体にとって必要なものと不要なものを識別し、食物アレルギーにおいてはアレルゲン、自己免疫疾患においては自己抗原と呼ばれる自分の体の構成成分に対して免疫反応を起こさないようにする仕組みのこと。 - 7.便中代謝物
消化管内での食物の消化や、腸内細菌の活動によって生成される物質のこと。腸内細菌そのものと同様、免疫システムの調節などの機能があり、健康の維持や疾患の発症に大きく関与していることが報告されている。 - 8.特異的IgE値
IgEは、異物に対して体が作り出すタンパク質(抗体)の一種で、特にアレルギー反応に関与する抗体。IgEのうち、特定のアレルゲンに対して体が産生するタンパク質のことを特異的IgEという。牛乳アレルギーにおいては牛乳特異的IgEやカゼイン特異的IgEが知られており、この値が高いほど牛乳アレルギーである可能性や重篤なアレルギー反応を起こす可能性などが高くなる。 - 9.食物負荷試験
食物アレルギーの原因となるアレルゲンを摂取することで実際にアレルギー反応が引き起こされるかを確認する試験で、食物アレルギーの診断や、患者が安全に摂取できる量を判定するために行われる。
共同研究グループ
理化学研究所 生命医科学研究センター
粘膜システム研究チーム
チームリーダー 大野 博司(オオノ・ヒロシ)
客員研究員 柴田 涼平(シバタ・リョウヘイ)
研究員 中西 裕美子(ナカニシ・ユミコ)
専門技術員 加藤 完(カトウ・タモツ)
マイクロバイオーム研究チーム
チームリーダー(研究当時)服部 正平(ハットリ・マサヒラ)
副チームリーダー 須田 亙(スダ・ワタル)
国立病院機構神奈川病院 小児科
医師 伊藤 直香(イトウ・ナオカ)
国立病院機構三重病院 小児科
特別診療・研究役 藤澤 隆夫(フジサワ・タカオ)
臨床研究部長 長尾 みづほ(ナガオ・ミヅホ)
東京家政大学 子ども学部
教授 岩田 力(イワタ・ツトム)
千葉大学大学院 医学研究院
小児外科学
教授(研究当時)吉田 英生(ヨシダ・ヒデオ)
小児病態学
特任教授 下条 直樹(シモジョウ・ナオキ)
研究支援
本研究は、厚生労働科学研究費補助金 疾病・障害対策研究分野 免疫アレルギー疾患等予防・治療研究「食物アレルギーにおける経口免疫療法の確立と治癒メカニズムの解明に関する研究(研究代表者:岩田力)」、日本医療研究開発機構(AMED)免疫アレルギー疾患等実用化研究事業(免疫アレルギー疾患実用化研究分野)「アレルギー疾患の発症・病態に関わる皮膚・腸管の細菌・真菌叢の解析(研究代表者:下条直樹)」、同革新的先端研究開発支援事業(AMED-CREST)「疾患における代謝産物の解析および代謝制御に基づく革新的医療基盤技術の創出(研究総括:清水孝雄)」「オミクス解析に基づくアレルギー発症機構の理解と制御基盤の構築(研究代表者:大野博司)」による助成を受けて行われました。
原論文情報
- Ryohei Shibata, Naoka Itoh, Yumiko Nakanishi, Tamotsu Kato, Wataru Suda, Mizuho Nagao, J-OIT group, Tsutomu Iwata8, Hideo Yoshida, Masahira Hattori, Takao Fujisawa, Naoki Shimojo, Hiroshi Ohno., "Gut microbiota and fecal metabolites in sustained unresponsiveness by oral immunotherapy in school-age children with cow's milk allergy", Allergology International, 10.1016/j.alit.2023.10.001
発表者
理化学研究所
生命医科学研究センター 粘膜システム研究チーム
チームリーダー 大野 博司(オオノ・ヒロシ)
客員研究員 柴田 涼平(シバタ・リョウヘイ)
 大野 博司
大野 博司
 柴田 涼平
柴田 涼平
報道担当
理化学研究所 広報室 報道担当
お問い合わせフォーム
